Los progresivos avances de la Medicina han propiciado un envejecimiento de la población en los países desarrollados.
Este fenómeno epidemiológico es especialmente relevante en nuestro país,
donde el porcentaje de personas mayores de 65 años alcanzará el 20% para el año 2020 (1).
La consecuencia de este envejecimiento para la asistencia sanitaria es un importante incremento de determinadas patologías,
entre ellas,
la enfermedad cerebrovascular.
Hoy en día,
esta enfermedad constituye la segunda causa de muerte y la primera causa de incapacidad en los países desarrollados.
De este modo,
la tasa de mortalidad anual es de 27 por 100.000 habitantes,
con una incidencia entre 150 a 200 casos por 100.000 habitantes y una prevalencia que asciende a 500-600 casos por 100.000 habitantes.
A estos datos,
que dan buena cuenta de la magnitud del problema en nuestro país (2),
hay que añadir la tremenda incapacidad de los pacientes que sobreviven a un ictus.
Se calcula que 2/3 de los pacientes que han sufrido un ictus y han sobrevivido,
tienen secuelas.
Las limitaciones físicas o psíquicas son variables pero,
en muchos casos de enorme trascendencia y gran invalidez.
En líneas generales se puede afirmar que,
tras el primer evento cerebrovascular agudo,
el 30% de los pacientes tiene deterioro cognitivo y el 25% precisa ayuda para cualquier actividad básica de la vida diaria.
Además de la transcendencia socio-sanitaria de esta patología,
el ictus consume una parte muy importante del gasto sanitario de la mayoría de países occidentales (alrededor del 4%).
La estenosis carotídea es una de las causas más importantes del ictus isquémico,
siendo responsable del 20-25% de ellos.
Además,
el riesgo de ictus recurrente en pacientes con estenosis carotídea grave es aproximadamente de un 28% a los 2 años.
El tratamiento precoz de las estenosis carotídea sintomática superior al 70%,
bien mediante endarterectomía o mediante la angioplastia más endoprótesis carotídea,
permite una prevención secundaria muy eficaz,
con reducciones relativas del riesgo de ictus ipsilateral cercanas al 50% y reducciones absolutas de hasta el 20% (3).
1.
ENFERMEDAD ARTERIOSCLERÓTICA CAROTÍDEA.
La afectación arteriosclerótica de la arteria carótida interna es una importante causa de enfermedad cerebrovascular.
A continuación repasamos la fisiopatología,
manifestaciones clínicas,
diagnóstico y el tratamiento de revascularización.
FISIOPATOLOGÍA.
La fisiopatología de la enfermedad arteriosclerótica en arteria carótida es similar a la descrita en otros territorios arteriales.
La lesión inicial es la acumulación de lipoproteínas en la íntima de pared arterial,
las cuales se oxidan participando en la elaboración de citoquinas que facilitan la migración de monocitos hacia el interior de la pared arterial.
Los monocitos se transforman,
por acúmulo de lipoproteínas,
en macrófagos cargados de lípidos o células espumosas que liberan más citoquinas,
oxidantes y metaloproteinasas.
Las células de músculo liso migran desde la capa media a la íntima,
proliferando y elaborando una matriz extracelular.
Los lípidos extracelulares se acumulan formando un núcleo central rodeado por una capa de tejido conectivo,
casquete fibroso,
que en placas evolucionadas se calcifica.
A medida que la placa continua creciendo,
estrecha la luz arterial causando estenosis de la misma.
La disrupción de la placa y la formación de trombo contribuyen al estrechamiento progresivo de la luz y a la aparición de eventos isquémicos.
La disrupción de la placa incluye la erosión superficial,
la rotura del casquete fibroso y la erosión del polo calcificado.
El contacto de los elementos de la sangre con componentes de la placa promueve la formación de trombos (4).
La hemorragia intraplaca si bien se ha asociado a aumento del riesgo de eventos isquémicos a corto plazo,
también se encuentra presente en placas severas de pacientes asintomáticos,
por lo que el volumen de placa condiciona un marcador más fiable de la evolución de la placa y del riesgo de eventos isquémicos (5,6).
Las placas arterioscleróticas tienden a asentar en bifurcaciones donde el flujo arterial es turbulento,
es por ello que muestran predilección por la bifurcación carotídea.
Suelen afectar a la pared posterior del la carótida interna y extenderse caudalmente hacia la arteria carótida común (4,7).
La isquemia cerebral puede producirse por múltiples mecanismos relacionados con la enfermedad carotídea extracraneal,
entre ellos: embolismo arterio-arterial de un trombo formado en la placa,
embolismo de cristales de colesterol u otros detritus ateromatosos,
oclusión trombótica aguda debida a rotura de la placa,
disección o hematoma subimtimal y disminución de la perfusión cerebral secundaria a estenosis crítica u oclusión debida al crecimiento progresivo de la placa.
Esta última causa representa una proporción relativamente pequeña de los eventos isquémicos,
ya que para ello debe coexistir un polígono de Willis insuficiente.
A favor del mecanismo embolígeno está la evidencia angiográfica de oclusión de ramas distales a la estenosis.
El compromiso de la vasorreactividad cerebral es un factor importante en el desarrollo y pronóstico de pacientes con ictus isquémico (4).
CLÍNICA.
Las estenosis carotídeas pueden ser sintomáticas o asintomáticas.
Las manifestaciones clínicas de la estenosis carotídeas vienen determinadas por los eventos isquémicos.
El soplo carotídeo es un signo exploratorio que podemos encontrar en estos pacientes (4).
Se define como el soplo que se puede escuchar sobre la estenosis cartotídea.
En pacientes asintomáticos neurológicamente es un pobre indicador de estenosis carotídea (8).
Algunos médicos experimentados pueden según las características del soplo dar una aproximación sobre la localización y severidad de la estenosis.
Un soplo focal sugiere una estenosis de la arteria carótida interna.
Un sonido estridente sugiere aumento de la velocidad de flujo sanguíneo al paso por la estenosis.
Un soplo de larga duración sugiere una estenosis grave.
Síntomas isquémicos.
La amaurosis fugax es una ceguera monocular transitoria causada por una disminución del flujo sanguíneo retiniano que ocasiona una brusca pérdida de visión.
La causa más frecuente es la enfermedad arteriosclérotica de la carótida ipsilateral.
El riesgo de ictus en el estudio NASCET (North American Symptomatic Carotid Endarterectomy Trial) fue menor en los pacientes con amaurosis fugax que en aquellos con accidente isquémico transitorio (AIT) (9).
El AIT fue clásicamente definido como una disfunción neurológica focal atribuible al territorio de una única arteria cerebral cuyos síntomas duran menos de 24 horas (10,11).
No obstante esta definición presenta algunas limitaciones; la duración de 24 horas es arbitraria y probablemente excesiva,
ya que la mayoría de los AIT duran de 5 a 10 minutos,
las connotaciones erróneas de benignidad que pueden aportar la definición clásica y en último lugar,
tampoco tienen en cuenta a los pacientes que además de AIT presentan lesiones cerebrales establecidas previas.
Es por ello que el TIA Working Group redefine al AIT como un episodio breve de disfunción neurológica con síntomas clínicos que duran menos de una hora,
sin evidencia de lesión isquémica en los estudios de neuroimagen (11).
Los AITs son un importante predictor de ictus,
especialmente en la primera semana. El reconocimiento precoz de los AITs y la modificación de los factores de riesgo son importantes medidas en la prevención de ictus (12).
Los ictus isquémicos se definen como el déficit neurológico que persiste durante más de 24 horas debido a la disminución del aporte arterial a un territorio encefálico (10,11).
Según su perfil evolutivo se pueden clasificar en (11):
- Ictus progresivo o en evolución: las manifestaciones clínicas iniciales evolucionan hacia el empeoramiento, bien por incremento de la focalidad neurológica,
por aparición de nuevos síntomas y signos neurológicos,
o debido a ambas circunstancias.
- Ictus con tendencia a la mejoría o con secuelas mínimas: sigue un curso regresivo,
siendo la recuperación de la focalidad neurológica ,a las tres semanas del inicio de la sintomatología,
igual o superior al 80% del total.
- Ictus estable: el déficit neurológico inicial no se modifica.
En los infar- tos del territorio carotídeo deben transcurrir al menos 24 horas sin modificación del cuadro clínico para considerar que éste es estable.
En el territorio vertebrobasilar deben pasar un mínimo 72 horas.
El significado de los síntomas no focales ha sido menos estudiado.
Ante síntomas puramente sensoriales (dolor,
parestesias,
insensibilidad) deben considerarse entre las causas: radiculopatías,
neuropatías,
afectación cerebral microvascular,
patología espinal o infartos lacunares.
Algunos pacientes con estenosis carotídea ≥90% pueden presentar pérdida de memoria,
dificultad para el habla y la audición debido a hipoperfusión del hemisferio cerebral dominante (4).
DIAGNÓSTICO.
Las técnicas de imagen no invasivas como la ecografía,
Tomografía Computarizada (TC) y Resonancia Magnética (RM),
pueden proporcionar la información requerida para el manejo de los pacientes con estenosis carotídeas.
Aunque la angiografía con substracción digital se considera la prueba estándar,
solo es necesaria para el diagnóstico en los casos en los que exista discordancia entre las pruebas no invasivas (4).
La ecografía- Doppler constituye la prueba inicial de estudio en los pacientes con estenosis carotídeas sintomáticas o asintomáticas. Es una técnica no invasiva,
segura y relativamente económica (4,7).
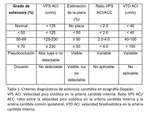
Mediante ecografía no se mide directamente el diámetro de la arteria sino que se realiza una estimación del grado de estenosis en función de la velocidad del flujo sanguíneo (4).
Los parámetros de velocidad que mejor se correlacionan con el porcentaje de estenosis medido en angiografía son: la velocidad pico sistólica en la arteria carótida interna (VPS ACI) y el cociente velocidad pico sistólica en la arteria carótida interna con respecto a la arteria carótida común ipsilateral (ratio VPS ACI/ACC).
Otros parámetros son la velocidad telediastólica en la arteria carótida interna (VTD ACI) y la estimación de la placa arteriosclerótica y la estenosis de luz que produce en modo-B y en Doppler Color (4,7,13). La Society of Radiologists in Ultrasound en una conferencia de consenso llevada a cabo en San francisco en 2002 establecieron unos criterios diagnósticos en ecografía para la estenosis carotídea que se exponen en la Tabla 1 (13). No obstante existen algunas limitaciones a estos criterios,
una de ellas es el solapamiento que existen en los valores de la PSV en la arteria carótida interna para diversos grados de estenosis,
medidos en angiografía convencional según criterios NASCET (4,13).
Otra es la variabilidad dependiente del operador y del ecógrafo,
por ello cada centro debería correlacionar sus valores de velocidad en ecografía con los grados de estenosis en angiografía,
para así establecer sus propios umbrales de velocidad.
Es por ello que se crearon programas de acreditación por la Intersocietal Commission for the Accreditation of Vascular Laboratories (ICAVL) (4,13).
También existen simuladores que dificultan el diagnóstico como las mayores velocidades en mujeres con respecto a hombres y velocidades aumentadas en pacientes con oclusión de la arteria carótida contralateral.
La ecografía además puede presentar limitaciones a la hora de diferenciar oclusiones completas de estenosis subtotales (4).
La angio-RM es una técnica de imagen no ionizante capaz de proporcionar una información anatómica precisa del arco aórtico y las arterias cervicales y cerebrales,
incluyendo la bifurcación carotídea,
así como de detectar estenosis carotídeas de alto grado,
siendo de gran utilidad para la planificación de la revascularización (4).
Se pueden usar dos secuencias diferentes; la Time of Flight (TOF) angio-RM y la angio-RM con gadolinio intravenoso.
La RM tiende a sobrestimar el grado de estenosis así como tampoco discierne entre oclusiones totales y pseudooclusiones,
estas limitaciones son mayores en las secuencias sin contraste intravenoso (14).
La RM no será apta para pacientes obsesos,
portadores de implantes incompatibles,
incapaces de permanecer en decúbito supino o claustrofóbicos (4).
La angio-TC proporciona una adecuada imagen anatómica arterial desde el cayado aórtico hasta el polígono de Willis,
permitiendo reconstrucciones multiplanares y la evaluación directa de la luz arterial.
Limitaciones a esta técnica pueden ser placas muy calcificadas,
implantes metálicos cervicales así como pacientes no colaboradores (4).
La angiografía con sustracción digital (DSA) es la prueba de imagen de referencia en arterias carótidas.
Se debe cateterizar selectivamente la arteria carótida estudiándola en al menos dos proyecciones.
La angiografía permite la evaluación de la carótida en toda su extensión aportando además información sobre posibles lesiones en tándem,
la morfología de la placa y la existencia de circulación colateral (15).
Entre sus desventajas se encuentra su naturaleza invasiva,
su alto coste y el riesgo de complicaciones neurológicas e incluso muerte,
siendo la incidencia de ictus,
cuando la angiografía la realiza personal experimentado,
inferior al 1% (4,16).
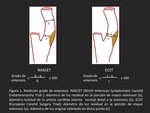
La medición del porcentaje de estenosis se puede realizar mediante dos métodos principalmente,
el North American Symptomatic Carotid Endarterectomy Trial (NASCET) y el European Carotid Surgery Trial (ECST),
siendo el NASCET el de uso más extendido.
El método NASCET mide el diámetro de luz residual en la porción de mayor estenosis y la compara con el diámetro luminal de la arteria carótida interna normal,
distal a la estenosis (17).
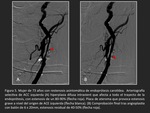
El método ECST compara el diámetro luminal residual en el punto de mayor estenosis con respecto al diámetro de luz original estimado en dicho punto (Figura 1).
El método ECST asume cuál es el diámetro original de la luz,
estando sujeto a una mayor variabilidad interobservador y además tiende a sobrevalorar el porcentaje de estenosis (18).
2.
REVACULARIZACIÓN.
El objetivo del tratamiento de revascularización es la prevención de eventos isquémicos (4,19).
Las recomendaciones de la “Guideline on the Management of Patients with Extracranial Carotid and Vertebral Artery Disease” aconsejan (4):
- Tratar mediante endarterectomía a los pacientes con un riesgo quirúrgico bajo que presentan ictus isquémicos no invalidantes o síntomas isquémicos cerebrales transitorios en los últimos 6 meses,
si el diámetro luminal en la arteria carótida interna ipsilateral está reducido en más del 70% según métodos no invasivos (nivel de evidencia A,
grado de recomendación I) o más del 50% en angiografía (nivel de evidencia B,
grado de recomendación I),
siendo el riesgo anticipado de ictus periprocedimiento o muerte inferior al 6%.
En estos casos la colocación de endoprótesis puede ser una alternativa a la cirugía (nivel de evidencia B,
grado de recomendación I).
- Razonable elegir el tratamiento endovascular con endoprótesis en pacientes con anatomía cervical desfavorable para la realización de endarterectomía (nivel de evidencia B,
grado de recomendación IIa),
como en pacientes con antecedentes de cirugía o radioterapia cervical,
así como también en pacientes con comorbilidades severas como las enfermedades pulmonares o cardíacas clínicamente significativas,
la oclusión carotídea contralateral y la parálisis del nervio laríngeo contralateral.
Conocer la morfología del arco aórtico,
las arterias cervicales proximales y la arteria carótida distal a la estenosis es esencial antes de proceder al tratamiento endovascular para asegurar la viabilidad del procedimiento (4).
TRATAMIENTO ENDOVASCULAR.
El tratamiento endovascular de las estenosis carotídeas generalmente se realiza mediante acceso vascular en arteria femoral común.
Se suele realizar angioplastia con balón en el área estenótica previa a la colocación de la endoprótesis.
Actualmente las endoprótesis que se usan son autoexpandibles.
La dilatación posterior con balón de angioplastia se valorará individualmente en cada caso (20).
El uso de sistemas de protección distales durante el procedimiento puede disminuir el riesgo de ictus isquémico cuando el riesgo de daño vascular es bajo y es realizado por operadores experimentados (4).
En el manejo de estos pacientes se debe antiagregar al menos tres días antes de la intervención con doble antiagregación con aspirina (81-325mg/día) y clopidogrel (75mg/día),
manteniéndose la doble antiagregación durante 30 días después del procedimiento y la aspirina de forma indefinida.
En pacientes intolerantes al clopidogrel se pueden administrar 250mg de ticlopidina dos veces al día (nivel de evidencia C,
grado de recomendación I) (4,19-23).
En la evaluación previa al procedimiento se debe estudiar cuidadosamente es el estado neurológico del paciente en las 24 horas previas,
así como las patologías concomitantes que puedan influir en el resultado de la intervención (4,
20).
Durante el tratamiento el paciente estará sedado aunque consciente,
se anticoagulará con heparina no fraccionada para conseguir tiempos de ACT entre 250-300 segundos y se controlarán los parámetros hemodinámicos (electrocardiograma,
frecuencia cardíaca,
tensión arterial) y el estado neurológico de manera continuada.
En la valoración neurológica durante la colocación de la endoprótesis deben evaluarse repetidamente el nivel de conciencia,
el habla y las habilidades motoras.
Si existiese un fallo neurológico,
el manejo dependerá de las posibilidades de rescate neurológico,
de las alternativas terapéuticas disponibles y del momento a lo largo del procedimiento en el que ocurra; si fuera precoz sería prudente parar el procedimiento,
no obstante si ocurriese hacia el final de la intervención pudiera ser más recomendable terminar rápidamente el tratamiento e inmediatamente hacer una valoración neurológica y angiográfica buscando las posibles causas.
La hipotensión durante la revascularización no es infrecuente por ello es recomendable asegurar una buena hidratación y ajustar el tratamiento antihipertensivo justo antes de la intervención.
Así mismo se puede administrar atropina (0,5-1mg intravenoso) durante la angioplastia y colocación de la endoprótesis para evitar una posible bradicardia (4).
En el postoperatorio inmediato se deben incluir cuidados del punto de acceso vascular,
monitorización hemodinámica y control del estado neurológico,
debiéndose realizar una valoración neurológica completa en las primeras 24 horas post-intervención.
Los pacientes neurológicamente asintomáticos podrán ser dados de alta en el primer día postoperatorio (4).
En el seguimiento a largo plazo deben realizarse evaluaciones neurológicas y controles mediante ecografía-Doppler al mes,
a los 3,
6 meses,
al año y a partir de dicho momento anualmente en busca de posibles restenosis o estenosis contralaterales (4,
20-25).
Complicaciones.
Pueden clasificarse en complicaciones cardiovasculares y neurológicas (4).
Cardiovasculares:
- Infarto de miocardio.
El riesgo reportado en la literatura es de aproximadamente un 1% (4).
- Hemodinámicas: hipotensión,
bradicardia,
asistolia y sincopes.
Ocurren en un 5-10% de los casos (4).
La mayoría son transitorios y no requieren continuar el tratamiento una vez finalizado el procedimiento .
- Disección y trombosis arterial.
El riesgo asociado en arteria carótida interna es inferior al 1% (4).
- Vasospasmo transitorio.
Ocurre en un 10-15% de los pacientes,
siendo más frecuente en fumadores e hipertensos (4).
Neurológicas:
- AIT.
Incidencia reflejada en la literatura entre 1-2% (4).
- Hemorragia intracraneal y síndrome de hiperperfusión.
El riesgo publicado es menor al 1% (4).
- Ictus isquémico.
En los resultados del Carotid Revascularization Endarterectomy Versus Stenting Trial (CREST) la incidencia de ictus en el periodo periprocedimiento de los pacientes tratados mediante endoprótesis fue 4,1% (21,
22).
- Complicaciones asociadas a los dispositivos (error en la colocación de la endoprótesis,
deformación o migración de la misma tras la colocación).
Son infrecuentes,
aconteciendo en menos de un 1% de los casos (4).
- Complicaciones relacionadas con el punto de punción.
Ocurren en un 5% de los pacientes,
las más frecuentes son dolor y hematoma autolimitados.
Los pseudoaneurismas se producen en un 1-2% de las intervenciones.
Las infecciones representan menos del 1% (4).
COMPARACIÓN ENTRE ENDARTERECTOMÍA Y TRATAMIENTO ENDOVASCULAR CON ENDOPRÓTESIS.
Se han realizado diversos ensayos aleatorizados comparando el tratamiento endovascular frente a la endarterectomía (CAVATAS,
SAPPHIRE,
SPACE,
EVA-3S,
ICSS,
CREST),
habiéndose también comparado la revascularización endovascular frente al tratamiento médico.
La falta de experiencia de los operadores que realizaron el tratamiento endovascular ha sido una crítica repetida a estos estudios.
Así mismo,
otra limitación la constituye la evolución del tratamiento endovascular a lo largo de los años en los que estos ensayos se realizaron; angioplastia con colocación de endoprótesis frente a angioplastia aislada,
incorporación de las endoprótesis autoexpandibles frentes a las endoprótesis balón-expandibles,
uso de sistemas de protección de émbolos distales (4).
El Carotid Revascularization Endarterectomy Versus Stenting Trial (CREST) es un ensayo clínico multicéntrico,
aleatorizado en el que se compara la endarterectomía frente al tratamiento endovascular con colocación de endoprótesis en pacientes de riesgo convencional con estenosis carotídea,
sintomáticos y asintomáticos.
El objetivo primario es determinar la incidencia de ictus,
infarto de miocardio o muerte durante el periodo periprocedimiento (30 días) y el ictus ipsilateral en los primeros 4 años tras la intervención (4,21,22,25).
En el análisis de los resultados no se encontraron diferencias estadísticamente significativas en el objetivo primario entre endarterectomía y tratamiento endovascular,
siendo de 6,8% en el grupo quirúrgico y de 7,2% en el grupo tratado con endoprótesis (HR 1.11; IC 95% 0.81-1.51; p= 0.51).
No obstante sí existieron diferencias en la distribución de los eventos en el periodo periprocedimiento; el ictus fue más frecuente en pacientes tratados endovascularmente (4,1% frente a 2,3%,
p= 0,012) y el infarto de miocardio se produjo con mayor frecuencia en aquellos tratados mediante endarterectomía (2,3% frente a 1,1%,
p= 0,032).
En el seguimiento más allá del periodo periprocedimiento los resultados entre ambos métodos de revascularización también fueron similares,
siendo la incidencia de ictus ipsilateral de 2,4% para el grupo quirúrgico y de 2% en los pacientes con endoprótesis (p= 0,85).
No se apreciaron diferencias significativas en análisis por subgrupos en cuanto a género (p= 0,34) y estado sintomático (p=0,84).
El análisis por edad,
sí mostro diferencias (p=0,02); el tratamiento endovascular presentó resultados más favorables en el grupo de pacientes menores de 70 años,
mientras que la endarterectomía favorecía a aquellos mayores de 70 años (4,21,22).
3.
RESTENOSIS.
DEFINICIÓN E INCIDENCIA.
La definición de la restenosis en arteria carótida extracraneal difiere según autores y el grado de estenosis residual tras la colocación de endoprótesis primaria que se considera aceptable.
El éxito angiográfico tras colocación de una endoprótesis primaria viene definido por una estenosis residual igual o inferior al 30-40%,
con flujo anterógrado normal (26,27).
Se consideran restenosis significativas aquellas iguales o mayores al 80% de la luz (28-31).
Existen controversias respecto a las restenosis moderadas,
algunos autores consideran que es aquella comprendida entre 50-79 % (29,30),
otros entre 40-79% (28) mientras que existen algunos autores que la definen como restenosis iguales o mayores al 60% de la luz (31).
Las restenosis de las endoprótesis carotídeas representan una complicación infrecuente,
con una incidencia reportada en la literatura del 3-5,8% (4,28-34).
No obstante el porcentaje difiere según se consideren todas las restenosis o solo aquellas significativas,
así Lal et al refieren una incidencia a los 5 años de seguimiento del 42,7%,
16,4% y 6,4% para restenosis ≥40%,
≥60% y ≥80% respectivamente (28,35).
Loa autores del CREST han publicado recientemente sus resultados a los dos años en relación con la incidencia de restenosis,
oclusión y repetición del procedimiento de revascularización (34).
Entre los 2191 pacientes con estenosis carotídea incluidos (1105 tratados mediante endarterectomía y 1086 tratados con angioplastia y endoprótesis),
113 desarrollaron restenosis; 48 (5,8%) pertenecían al grupo tratado endovascularmente y 57 (5,8%) al grupo quirúrgico.
En cuanto a la oclusión arterial,
se registraron 8 casos; 3 (0,3%) en el grupo endovascular y 5 (0,5%) en el quirúrgico.
Se realizaron 43 procedimientos repetidos de revascularización (20 en el bloque tratado mediante angioplastia y endoprótesis y 23 en el grupo tratado mediante endarterectomía),
28 de ellos en pacientes con restenosis.
Las diferencias en ninguno de los tres campos alcanzó diferencias estadísticamente significativas.
En cuanto a la significación clínica,
en estos dos años,
sólo se registraron 13 ictus isquémicos ipsilaterales; 4 en el grupo endovascular (1 de ellos tras el diagnóstico de restenosis) y 9 en el bloque quirúrgico (5 en pacientes diagnosticados previamente de restenosis).
La incidencia de restenosis de endoprótesis es mayor en otros territorios arteriales (29,30).
La incidencia de restenosis coronaria oscilaba con las endoprótesis clásicas entre 16% hasta alcanzar incluso 59% (30,36,37).
La introducción de los stents farmacoactivos ha logrado reducir la incidencia de restenosis coronaria de manera significativa con respecto a las endoprótesis clásicas,
siendo en algunos ensayos clínicos inferior al 10%,
si bien la tasa de restenosis se incrementa en lesiones complejas (38,39).
FISIOPATOLOGÍA.
La restenosis es una respuesta biológica al daño vascular secundario a la angioplastia y colocación de endoprótesis (32).
Existen dos mecanismos fisiopatológicos subyacentes; las restenosis precoces son debidas a hiperplasia miointimal (30,40),
mientras que las que se producen de manera tardía se deben a la progresión de la propia enfermedad arteriosclerótica (4,26,28,32,41).
El periodo de tiempo considerado “precoz” difiere según los distintos autores,
siendo para algunos los primeros 6 meses tras el tratamiento (26,32),
para otros el tiempo comprendido hasta los 2 años (4,41) mientras que otros autores fijan el límite a los 3 años tras el tratamiento (28).
Señalando a la hiperplasia miointimal como principal mecanismo de restenosis,
De Borst et al publican una serie de 4 pacientes con restenosis de la endoprótesis carotídea que se trataron mediante endarterectomía y retirada de la endoprótesis,
a las cuales se les realizó estudio anatomopatológico (40).
El análisis histológico demostró hiperplasia intimal con proliferación de células de músculo liso en todos los casos,
sin que se evidenciara proceso inflamatorio específico en la pared del vaso.
Las endoprótesis inducen cambios permanentes en la pared arterial,
existiendo por un lado el “remodelamiento positivo” debido a la expansión del stent y por el otro,
el “remodelamiento negativo” ocasionado por la hiperplasia miointimal (27,32).
Willfort-Ehringer et al realizaron seguimiento mediante ecografía durante dos años a 109 procedimientos de endoprótesis carotídea extracraneal.
En sus resultados indican que la máxima expansión de la endoprótesis ocurre hacia el tercer mes postratamiento,
enlenteciéndose desde ese momento,
pero manteniéndose cierto grado de expansión continua durante los dos años que duró el seguimiento de estos pacientes,
especialmente debido a la sobredimensión de la endoprótesis con respecto al diámetro de la arteria lo cual genera una alta presión radial sobre la pared de la misma.
La expansión es mayor en la región media de la endoprótesis,
estando en dicha zona influenciada por la composición de la placa arteriosclerótica tratada. Las placas fueron clasificadas según el estudio “Asymptomatic Carotid Stenosis and Risk of Stroke” en blandas,
fibrosas y calcificadas,
siendo la expansión mayor en las placas blandas que en las fibrosas y en estas últimas mayor que en las calcificadas (32).
Estos mismos autores remarcan que la hiperplasia miointimal alcanza su máximo crecimiento hacia el sexto mes tras el procedimiento,
ralentizándose su progresión hasta el duodécimo mes y permaneciendo estable durante todo el segundo año,
esto genera un aumento de las velocidades pico sistólica y telediastólica en las arterias tratadas con endoprótesis.
En sus conclusiones,
señalan que el remodelamiento negativo predomina durante el primer año,
siendo el remodelamiento positivo predominante durante el segundo año (32).
FACTORES DE RIESGO.
Diversos estudios señalan como único factor predictivo significativamente estadístico para el desarrollo de restenosis el antecedente de restenosis post-endarterectomía carotídea tratada mediante angioplastia y colocación de endoprótesis (26,28-33).
No se han encontrado asociaciones significativas con factores relacionados con restenosis en otros territorios arteriales,
como son: edad del paciente,
diabetes mellitus,
dimensiones de la placa arteriosclerótica,
tipo y material del stent (23,26,28-33).
Los resultados del CREST a los dos años muestran mayores tasas de restenosis en ciertos grupos: mujeres,
pacientes con diabetes mellitus y pacientes con dislipemia (34).
Un estudio prospectivo realizado en un único centro en el que se llevo a cabo seguimiento a largo plazo a pacientes con estenosis carotídea tratada mediante angioplastia y colocación de endoprótesis,
señala como otros posibles factores predictores de restenosis,
la presencia de oclusión de la arteria carótida contralateral y el hallazgo en ecografía-Doppler de una PSV elevada tras el procedimiento (≥120 cm/s) indicando estenosis residual de bajo grado (23).
CLÍNICA.
La mayoría de los pacientes que desarrollan restenosis carotídeas permanecen clínicamente asintomáticos,
diagnosticándose casualmente en los controles de ecografía-Doppler (26,28-31).
En las series publicadas la mayor parte de los que presentaron clínica neurológica,
ésta consistió en episodios de AIT (26,31).
Reimers et al (26) publican una serie de 32 restenosis carotídeas en 31 pacientes,
7 de los cuales presentaron síntomas neurológicos,
siendo todos ellos AIT.
El potencial embólico de las restenosis carotídeas se considera menor al de las lesiones arterioscleróticas primarias (35).
No obstante,
el riesgo embolígeno existe; Reimers et al publican una serie de 32 restenosis revascularizadas mediante angioplastia en las que durante el procedimiento se emplearon sistemas de protección de émbolos distales,
entre ellos 31 filtros de los cuales 17 fueron analizados histológicamente,
en 12 de los cuales se evidenció material embólico macróscópico (71%). El estudio histológico reveló fragmentos de tejido fibroso asociado a cestas de fibrina con eritrocitos,
leucocitos y plaquetas atrapados en ellas.
A diferencia del material embólico encontrado en los filtros tras angioplastia primaria,
en el estudio de estos casos de angioplastia secundaria por restenosis no se detectaron cristales de colesterol,
células espumosas ni calcificaciones (26).
DIAGNÓSTICO.
El diagnóstico de las restenosis carotídeas ocurre generalmente,
de manera incidental en el curso del seguimiento de estos pacientes al realizarles controles de ecografía-Doppler (26,28-31).
Como ya hemos expuesto previamente,
las endoprótesis generan cambios permanentes en la pared arterial secundarios al “remodelamiento positivo" por la expansión de la endoprótesis y “remodelamiento negativo” debido a la hiperplasia miointimal (27,32).
Estas modificaciones provocan una discordancia entre la complianza de la pared arterial nativa y el segmento arterial tratado mediante endoprótesis así como una menor distensibilidad del segmento con endoprótesis con respecto a la misma arteria sin la endoprótesis y a la arteria carótida contralateral (42).
Todo ello induce alteraciones hemodinámicas en el comportamiento del flujo arterial a su paso por la endoprótesis,
implicando valores de velocidad mayores en el interior de la misma comparativamente con la arteria nativa (27).
Debido a esto,
los valores de velocidad empleados en ecografía-Doppler en arterias carótidas nativas no son válidos en arterias con endoprótesis (27,28,31,43).
A medida que las estenosis alcanzan un mayor grado,
la velocidad pico sistólica (VPS) se incrementa (13,27),
no obstante no existen valores de velocidad estandarizados para las arterias con endoprótesis,
ya que estos dependen del equipo de ultrasonidos empleado y la técnica del operador que realiza la ecografía,
por ello se acepta que cada laboratorio debe establecer unos criterios de velocidad personalizados y validados para su propio centro (27,28,31).
Setacci et al realizan un estudio prospectivo de seguimiento mediante ecografía-Doppler de 814 estenosis carotídeas tratadas con endoprótesis para determinar potenciales umbrales de velocidad en ecografía-doppler que permitan diagnosticar diferentes grados de restenosis y su correlación con angiografía (27).
Para ello al finalizar el procedimiento terapeútico determinan mediante angiografía el grado de estenosis residual,
considerando estenosis iguales o mayores al 30% (medidas según criterios NASCET),
un fracaso del tratamiento.
En las primeras 48 horas tras la colocación de la endoprótesis se realiza un primer control ecográfico para establecer las características basales de velocidad a partir de las cuales se contabilizarán las posibles variaciones.
Se realizan sucesivos controles ecográficos a los 30 días,
3,
6 y 12 meses,
pasando a ser posteriormente anuales.
Los autores remarcan la importancia de realizar todos los controles en el mismo laboratorio,
con el mismo equipo ecográfico y los mismos parámetros técnicos.
Se miden las siguientes variables: flap neointimal o presencia de trombo intravascular; velocidad pico sistólica en arteria carótida interna (VPS ACI) próxima,
media y distal de la endoprótesis y en áreas de estenosis visibles en ecografía modo-B; velocidad telediastólica en la arteria carótida interna (VTD ACI) y el cociente velocidad pico sistólica en la arteria carótida interna con respecto a la arteria carótida común ipsilateral (ratio VPS ACI/ACC).
En los casos en los que la VPS en la arteria carótida interna fue igual o mayor a 200cm/s o se elevó tres o más veces por encima del valor establecido como basal para el paciente,
se realizó una angiografía para verificar el grado de restenosis.
Las restenosis iguales o mayores al 70% fueron subsidiarias de tratamiento endovascular.
Setacci et al proponen unos umbrales potenciales de velocidad en ecografía-Doppler que se correlacionan con grados de restenosis medidos mediante angiografía con sustracción digital según criterios NASCET.
Ellos proponen como criterios para el diagnóstico de restenosis iguales o mayores al 70% la presencia de VPS ACI igual o mayor de 300cm/s,
VTD ACI igual o mayor de 140cm/s y una ratio VPS ACI/ACC igual o mayor de 3,8,
la combinación de estos tres parámetros alcanza una sensibilidad del 98% con una especificidad del 99% (Tabla 2).
No obstante,
los autores señalan que estos criterios tan solo son válidos para su propio laboratorio y equipo,
remarcando la importancia de que cada laboratorio use unos valores de velocidad personalizados y validados para su propio centro (27).
El papel de la angiografía convencional en el diagnóstico de las restenosis queda relegado a la confirmación de las sospechas de restenosis diagnosticadas mediante ecografía (26-28,30,31,35,43).
CLASIFICACIÓN.
Mehran et al (44) clasifican las restenosis coronarias en base a los hallazgos morfológicos en angiografía convencional.
Definen cuatro clases (Figura 2):
Clase I: “Focal”.
Lesiones menores o iguales a 10 mm de longitud,
localizadas en zonas de unión o articulación,
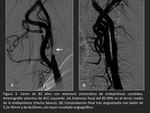
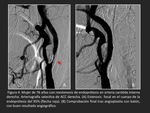
cuerpo de la endoprótesis (Figuras 3 y 4),
margen proximal o distal (pero no ambos),
o una combinación de dichas localizaciones (restenosis multifocal) .
Clase II: “Intrastent difusa”.
Lesiones mayores de 10 mm de longitud pero confinadas al interior de la endoprótesis sin extenderse más allá de sus márgenes (Figura 5).
Clase III: “Proliferativa difusa”.
Lesiones mayores de10 mm de longitud que se extiende más allá de los márgenes de la endoprótesis.
Clase IV: Restenosis con “oclusión total”.
Ausencia de flujo a través de la lesión.
En el trabajo de Mehran et al,
clases más severas de restenosis se asocian a mayor prevalencia de diabetes mellitus y número de episodios de restenosis previos.
El patrón de restenosis,
junto con la presencia de diabetes mellitus y episodios previos de restenosis recurrentes son factores predictores a largo plazo de la necesidad de revascularización.
Lal et al (35) establecen una clasificación de las restenosis carotídeas basada en los hallazgos ecográficos,
distinguiendo cinco tipos que representan un espectro creciente de hiperplasia miointimal como respuesta a la endoprótesis (Figura 6):
Tipo I: “focal en los márgenes de la endoprótesis”.
Lesiones menores o iguales a 10mm,
localizadas en los extremos proximal o distal de la endoprótesis (pero no ambos). Cuando la afectación es de ambos márgenes,
proximal y distal,
se clasifica como tipo I marginal multifocal.
Tipo II: “focal intrastent”.
Lesiones menores o iguales a 10mm confinadas al interior del stent sin extenderse más allá de los márgenes del mismo. Dos o más lesiones menores o iguales a 10mm localizadas en el interior de la endoprótesis,
se define como tipo II intrastent multifocal.
Tipo III: “difusa intrastent”.
Lesiones mayores de 10mm limitadas al interior de la endoprótesis sin sobrepasar sus extremos.
Tipo IV: “difusa proliferativa”.
Lesiones mayores de 10mm que se extienden por fuera de los márgenes de la endoprótesis.
Tipo V: “oclusión total”.
No se identifica flujo en el interior de la lesión ni luz arterial.
Según Lal et al,
las únicas variables que predicen la necesidad de revascularización son grados mayores de restenosis según el patrón ecográfico propuesto y la presencia de diabetes mellitus.
TRATAMIENTO.
El tratamiento idóneo de las restenosis carotídeas no está consensuado (4,40,41,43).
En la literatura se ha documentado el uso de diferentes modalidades terapeúticas,
incluyendo pequeñas series de pacientes tratados quirúrgicamente mediante endarterectomía y extracción del stent,
si bien los procedimientos terapeúticos más frecuentemente empleados son los endovasculares; angioplastia simple,
angioplastia con “cutting-balloon”,
angioplastia con endoprótesis o combinación de varios métodos (4,26,28-31,40,41,43,45).
La técnica empleada con mayor frecuencia es la angioplastia con balón (26,28-30,43).
Van Haaften et al realizan una revisión de la literatura publicada acerca del manejo terapeútico de las restenosis carotídeas (43).
Revisan un total de 100 restenosis carotídeas en 96 pacientes,
de las cuales,
la mayoría fueron tratadas mediante angioplastia; 31 mediante angioplastia simple y 23 mediante angioplastia con “cutting-balloon”.
En 31 de los pacientes se colocó una nueva endoprótesis,
sin que existiera uniformidad en el tipo de endoprótesis empleada por los distintos autores,
habiéndose utilizado tanto endoprótesis montadas en balón,
como los stents Palmaz (28,30) como endoprótesis autoexpandibles,
tipo Wallstents (26).
La colocación de una nueva endoprótesis queda reservada según algunos autores para aquellos casos en los que tras la angioplastia secundaria queda una estenosis residual significativa,
definida como tal una estenosis ≥20% (28),
≥30% (29) o ≥40% (26). Otras indicaciones recogidas en la literatura incluyen el compromiso del flujo anterógrado o la evidencia de disección carotídea (26).
En lo que respecta a las indicaciones para tratar las restenosis carotídeas,
existe acuerdo generalizado para revascularizar las restenosis sintomáticas,
no obstante,
no existe consenso sobre la necesidad de revascularización en aquellos casos asintomáticos (4,26,41,43).
Algunos autores recomiendan tratar las restenosis hemodinámicamente significativas (≥80%) independientemente de la presencia o no de síntomas asociados (28,30,43).
En la “Guideline on the Management of Patients With Extracranial Carotid and Vertebral Artery Disease” publicada en 2011 por el Journal of American College of Cardiology los autores afirman que las restenosis son generalmente una condición benigna que no requiere revascularización,
excepto en determinadas circunstancias como restenosis sintomáticas o restenosis severas con progresión a enfermedad preoclusiva (4).
PRONÓSTICO.
En la literatura publicada,
los procedimientos de revascularización secundarios presentaron un excelente pronóstico a corto plazo,
sin que se registraran eventos en los 30 primeros días (26,28-31,43).
Reimers et al consideran eventos periprocedimiento los ictus,
AITs y muerte que se producen en los primeros 30 días (26).
Con respecto al pronóstico a medio plazo,
todos los pacientes permanecieron asintomáticos desde el punto de vista clínico (26,28-31,43).
Reimers et al definen la restenosis recurrente como aquella que acontece después de que la restenosis inicial haya sido tratada (26).
Los estudios de Setacci et al así como el de Chakhtoura et al no registraron ninguna restenosis recurrente durante un seguimiento medio de 12,4 meses (rango 3,5-30,7 meses) y 10±6 meses (rango 1-14 meses),
permaneciendo todos los pacientes clínicamente asintomáticos (29,30).
Por el contrario,
Lal et al registran 2 restenosis recurrentes asintomáticas durante un seguimiento medio de 24 meses que fueron tratadas mediante angioplastia simple (28).
Zhou et al publican otros 2 casos de restenosis recurrentes,
también asintomáticas,
a lo largo de un seguimiento medio de 12 meses (rango 3-37 meses),
que se revascularizaron mediante angioplastia con “cutting-balloon” (31).
Reimers et al presentan un único caso de restenosis recurrente asintomática durante un seguimiento medio de 17±5 meses (rango 12-28 meses),
que se trató mediante angioplastia simple (26).
Se ha postulado una menor incidencia de restenosis recurrente tras angioplastia con “cutting-balloon” al compararla con angioplastia simple,
si bien esta diferencia dista mucho de ser estadísticamente significativa (43).
Setacci et al proponen como probable mecanismo causante de la menor tasa de restenosis recurrentes en las angioplastias realizadas con “cutting-balloon” el hecho de que las hojas de éste provocan una disrupción de la continuidad fibroelastica del anillo de hiperplasia miointimal (29).
Una limitación a estos estudios la constituye la no disponibilidad aún de resultados a largo plazo.