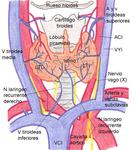
La glándula tiroides tiene dos lóbulos conectados por el istmo.
Se localiza en el cuello por delante de la tráquea,
en el espacio infrahioideo,
entre el cartílago tiroides y la escotadura supraesternal.
Normalmente en la región posterior de cada uno de los cuatro polos del tiroides se localiza una glándula paratiroides.

Fig. 1: Localización de la glándula tiroides y su relación con las estructuras vecinas.
El tiroides es una de las glándulas más importantes del cuerpo ya que su campo de actuación se extiende al aparato cardiovascular,
sistema digestivo,
SNC,
otras glándulas endocrinas y estimula el crecimiento y el metabolismo basal.
Además,
su patología es relativamente frecuente,
por lo que el control de los hallazgos mediante analíticas,
exploración física y métodos de imagen es de especial importancia.
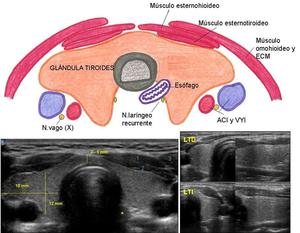
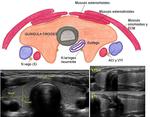
Fig. 2: Glándula tiroides normal en una paciente de 27 años y su correlación con la anatomía.
Se observan con claridad los planos musculares anteriores a la glándula (1 y 2) que corresponden al músculo esternotiroideo y esternohioideo, así como el ECM (3) más lateral.
El esófago también es fácil de identificar (*).

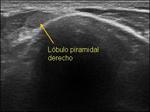
Fig. 3: Entre un 15-75 % de los adultos presentan un lóbulo piramidal como variante normal.
El aumento en el uso de pruebas de imagen y la mejora técnica experimentada en los últimos años,
han provocado un gran incremento de incidentalomas debido a la alta incidencia de nódulos tiroideos.
La prueba indicada para la valoración de la glándula tiroides es la ecografía,
ya que proporciona una alta sensibilidad y permite realizar punciones diagnósticas si fuesen necesarias.
Existen enfermedades tiroideas difusas en las que existirá una alteración en la ecoestructura y tamaño de la glándula (bocio) y en el patrón de vascularización,
y otras en las que existirán uno o varios nódulos que habrá que estudiar en función de unos patrones,
y que en muchos casos presentarán características diferentes entre ellos.
1- Las enfermedades difusas son: tiroiditis linfocítica autoinmune (Hashimoto),
bocio adenomatoso o coloide y enfermedad de Graves.
En estos casos el diagnóstico no será ecográfico pero permitirá estudiar crecimientos asimétricos y realización de PAAF si existieran nódulos asociados.

Fig. 4

Fig. 5: En la primera imagen se muestra un bocio en un bebé de 3 meses.
En la foto inferior, se ve un importante aumento de espesor a nivel del istmo.

Fig. 6: Imagen ecográfica típica de la enfermedad de Hashimoto. Se observa el parénquima grosero con los pseudonódulos hipoecogénicos y finos tabiques hiperecoicos entre ellos, con una importante vascularización.

Fig. 7: En la enfermedad de Hashimoto es frecuente la presencia de pequeñas adenopatías reactivas periglandulares.

Fig. 8: En las imágenes 1 y 2 se observa un tiroides de tamaño normal, con cierta inhomogeneidad de su parénquima y un quiste coloide situado en el medio del LTD.
3 y 4: Se ve la marcada vascularización de todo el parénquima, típico de esta enfermedad y también conocido como "infierno tiroideo".
2- En cuanto a los nódulos,
debemos tener en cuenta que la incidencia en la población de los mismos es muy alta y que su prevalencia aumenta con la edad.
Así encontramos que son palpables en un 4-8 % de los adultos,
demostrables ecograficamente en un 10-41% y aparecen hasta en un 50% de las autopsias.
A pesar de todo esto,
únicamente el 3-7% de todos ellos se pueden clasificar como malignos.
Lo más importante en estos casos será conocer los diferentes patrones que nos orienten hacia benignidad o malignidad para poder orientar el clínico en la toma de decisiones terapéuticas.

Fig. 9
Los criterios ecográficos usados para la discriminación de los nódulos y su categorización como benignos o malignos incluyen diferentes aspectos que hacen referencia a su ecoestructura,
morfología,
vascularización,
etc.
Los más importantes son la forma,
el margen (liso o especulado),
la ecogenicidad y la presencia o no de calcificaciones que podrán ser centrales o periféricas.
En cuanto al tamaño,
debemos tener en cuenta que marcará la precisión del diagnóstico,
pero no será criterio de clasificación.
La presencia de al menos un hallazgo ecográfico sugestivo de malignidad reporta un 83,3% de SS (sensibilidad) y un 74% de E (especificidad) y en función de estos hallazgos el nódulo deberá ser biopsiado,
sometido a seguimiento ecográfico o a observación clínica.
Sin embargo la combinación de varios de estos hallazgos proporciona una mejor aproximación diagnóstica,
ya que ninguna de las características proporciona por sí misma un 100% de SS y E,
es decir,
no existe un hallazgo patognomónico de malignidad.
Es importante que el radiólogo sepa que los hallazgos pueden ser afectados y sesgados por
- Diferencias en las características técnicas de los equipos utilizados.
- Experiencia del radiólogo y diferencias interobservador inevitables.
- Problemas con la falta de estandarización del léxico a la hora de caracterizar y describir los nódulos tiroideos.
CRITERIOS DE CLASIFICACIÓN:
1.
Tamaño: > 1cm
1 cm o < 1cm
El tamaño de los nódulos no es un dato predictivo de malignidad ya que la probabilidad de desarrollar cáncer a partir de un nódulo tiroideo no se modifica en función del tamaño del mismo (4.).
2.
Contenido Predominantemente sólido (>50%)
Predominantemente quístico (>50%)
(En algún artículo se habla hasta de 5 tipos: sólido,
predominantemente sólido,
mixto,
predominantemente quístico y quístico).
3.
Apariencia espongiforme.
(Múltiples microquistes que ocupan más de la mitad del nódulo).
4.
Forma.
Redondo-ovoideo (diámetro AP menor o igual
que el transversal)
Más alto que ancho (diámetro AP>transversal)
Irregular (ninguno de los otros dos)
5.
Margen.
Bien definido
Espiculado
Mal definido
6.
Ecoestructura: homogénea o grosera.
7.
Ecogenicidad de la porción sólida (respecto al parénquima normal y la musculatura)
Marcadamente hipoecoico
Hipoecoico
Isoecoico
Hiperecoico
8.
Calcificaciones (clasificadas según tamaño)
Microcalcificaciones (<1mm)
Macrocalcificaciones (>1 mm)
En anillo / cáscara de huevo

Fig. 10: Arriba: Calcificaciones en cáscara de huevo. Benignas.
Abajo: Microcalcificaciones. Criterio de malignidad.
Microcalcificaciones: el VPP más alto (41-94 %) pero baja sensibilidad (solo aparecen en el 26-59% de todos los tumores).
Están en relación con cuerpos de psamoma calcificados y no dejan sombra acústica posterior por su pequeño tamaño.
Es importante no confundirlas con los focos ecogénicos con artefacto “en cola de cometa” típicos de los quistes benignos.
En muchos estudios (2.) se utiliza también el patrón de vascularización intrínseca respecto al parénquima circundante como criterio de caracterización de nódulos,
siendo en principio criterio de malignidad la existencia de registro Doppler central en lugar de periférico.
La invasión directa de partes blandas adyacentes y las metástasis de uno o más ganglios (3.) siempre indican un comportamiento agresivo de la lesión.
Se habla de 10 PATRONES:
- Espongiforme sin hipervascularización (patrón más común).
B
- Quístico con contenido coloide avascular.
B
- Patrón con áreas / bloques hiperecogénicos separados por finas bandas hipoecoicas.
B
- Hiperecogenicidad uniforme.
B
- Hipervascularidad intensa.
- Hipoecogenicidad
- Isoecogenicidad sin halo
- Isoecogenicidad con halo
- Nódulo con intensa vascularización periférica
- Patrón mixto.
(1-4: Benignos,
5-10: Impredecibles)

Fig. 11: Nódulo sólido-quístico (1), hiperecogénico uniforme (*) respecto al parénquima adyacente y quístico con artefactos en “cola de cometa” (flecha).

Fig. 12: Nódulos en ambos lóbulos tiroideos de características benignas.
La media de tamaño de los nódulos malignos es inferior a la de los benignos.
La mayoría de los nódulos tanto benignos como malignos tienen un contenido predominantemente sólido (hasta un 87% de los B y un 98% de los M).
Algunos hallazgos no muestran diferencias significativas: forma irregular,
margen mal definido,
ecoestructura,
hiperecogenicidad y calcificaciones en cáscara de huevo.
Los nódulos benignos >1 cm con más frecuencia son isoecogénicos y con bordes mejor definidos que aquellos B de menor tamaño.
La hipoecogenicidad da gran SS pero poca E.
El resto de hallazgos son E xo poco SS.
Es decir ninguna característica ecográfica tiene por sí misma alta SS y E,
por lo que hay que combinar hallazgos para aumentar la eficacia dx.
En particular,
un nódulo predominantemente sólido con microcalcificaciones tiene un 31,6 % de probabilidades de ser cáncer (4.).
OJO: En los nódulos de menor tamaño (<1 cm) aumentan el número de falsos positivos.
PUNCIONES TIROIDES
Son económicas,
seguras y mínimamente invasivas,
por lo que se realiza a pacientes ambulantes.
El resultado de la PAAF es operador dependiente (Las PAAF deben ser realizadas por pocas personas que realicen al menos 1-5 procedimientos/mes) Si >15% de muestras no satisfactorias,
entrenamiento.
Se repetirá: muestra insuficiente o inadecuada,
crecimiento del nódulo,
recurrencia del quiste,
sospecha de malignidad a pesar de un resultado negativo.
INDICACIONES:
Lesiones > o =1 cm con microcalcificaciones o >1,5 cm nódulos sólidos o con calcificaciones groseras.
(Es decir,
el tamaño de corte se elegirá en función de las características ecográficas del nódulo y será menor en aquellos con mayor riesgo).
La asociación americana de endocrinología recomienda PAAF de nódulos incluso <1cm si tienen alguna característica sospechosa de malignidad.
La presencia de múltiples nódulos (en función de las características ecográficas y no del tamaño ya que en 1/3 de los casos el tumor asienta sobre un nódulo no dominante (4.)),
aunque existe el mismo riesgo de M si un único nódulo o múltiples (menor por cada uno,
pero globalmente igual).
Nódulo que haya crecido sustancialmente (no hay consenso respecto a cuánto) respecto a eco previa aunque tenga una PAAF negativa.

Fig. 13: Nódulo sólido aparentemente bien definido con gran vascularización tanto central como periférica, del que se realizó una PAAF con guía ecográfica para la obtención de muestras.
Tiroiditis de Hashimoto cuando aparece con patrón nodular,
para descartar linfoma y carcinoma papilar (pueden coexistir).
Crecimientos rápidos del tiroides sobre todo en mayores de 50 años para descartar linfoma,
carcinoma anaplásico y mets.
Hay más FN en punciones sin eco que en las guiadas con US.
Técnica:
- Aspirar mientras se mueve la aguja.
- Mover la aguja sin aspirar,
sobre todo en nódulos hipervasculares para evitar la hemodilución de la muestra.
Se toman las células que queden en la aguja.
Algunos autores dicen que esta técnica es mejor (menos traumática) y que se debería empezar por ella.
La otra si esta falla.
Al menos hacer 2 aspiraciones de diferentes sitios del nódulo (lo ideal es entre 1 y 5),
viendo en todo momento la aguja (20-27 G).
Algunos autores dicen que cuanto más fina la aguja mejor (lesiones hipervasculares),
porque con mayores grosores sangra más el nódulo y dificulta el análisis AP.
Es importante dx los carc tiorideos <1cm porque pueden manifestarse como metástasis.
A menudo el material obtenido de estos nódulos es mejor que en nódulos mayores en los que hay más vascularización y necrosis o areas quísticas.

Fig. 14
GANGLIOS (4.): Si son de aspecto patológico se deben biopsiar (exceptuando los submandibulares).
El aspecto patológico dependerá de: tamaño (sospechosos a partir de 7 mm en el eje corto,
aunque es un criterio menos valorable que el resto),
forma (redondos),
vascularización y ecoestructura (heterogéneos,
con calcificaciones y áreas quísticas).

Fig. 15: Paciente con antecedente de cáncer de páncreas, que se palpa un bulto en el cuello. En la ecografía de cuello se evidenció esta adenopatía de características patológicas.

Fig. 16: En el paciente anterior, se decidió completar el estudio ecográfico con PAAF guiada con ecografía que confirmó el diagnóstico de metástasis de su adenocarcinoma de páncreas.
EVITAR AREAS QUISTICAS,
DE FIBROSIS Y CALCIFICACIONES.
(aspirar contenido quístico y luego muestrear el polo sólido).

Fig. 17

Fig. 18: En este tipo de adenopatías necrosadas, la punción para la obtención de una muestra válida debe hacerse del polo sólido de la misma.
El screening no está indicado debido a la alta prevalencia y el buen pronóstico de los nódulos tiroideos.
Sólo se justifica en grupos de alto riesgo: Irradiación de cabeza o cuello durante la infancia,
MEN o AF de carcinoma tiroideo.
ANATOMIA PATOLOGICA:
- Nódulos benignos: coloides,
hiperplásicos y tiroiditis.
No bx. Seguimiento: Por imagen (no PAAF) si tamaño estable,
siguiente control en más tiempo.
- Nódulos sospechosos: neoplasias foliculares y céls de Hurthle.
Bx y hemitiroidectomía o total recomendada.
Tras la Qx 30-65% se confirmará el cáncer.
- Carcinoma/hallazgos malignidad (lo mas frecuente: ca papilar).
Bx y Qx porque los FP son raros (<1%).
- No dx (15-20%).
BX:
- Nódulos hipoecogénicos con microcalcificaciones.
- Nódulos hipoecoicos con calcificaciones groseras.
- Nódulos sólidos,
ovoideos y bien definidos con fino halo hipoecoico.
- Masa sólida con sombra de sus bordes,
sugestiva de fibrosis.
FR para ca de tiroides (alrededor del 10% de los nódulos):
- AF.
- Irradiación de cabeza y cuello.
- Sexo masculino.
- < 30 (<20 en 4.) años o > 60 años.
- AP de MEN2.
- EF que aumenta las probabilidades de malignidad: firmeza del nódulo,
crecimiento rápido,
fijación a estructuras adyacentes,
parálisis de cuerda vocal y aumento de adenopatías regionales.

Fig. 19: Tiroidectomía en paciente con antecedente de cáncer de tiroides. Control.