¿ Que es la imagen BOLD?
La imagen BOLD se basa en el efecto que las moléculas paramagnéticas tienen en los campos locales produciendo variaciones locales de la fase de la imagen que se traduce en una caída de la señal en secuencias eco de gradiente ponderadas en T2* (FFE-T2*) [Ogawa,
Brain magnetic resonance imaging with contrast dependent on blood oxygenation.
Proc Natl Acad Sci U S A,
1990.
87(24): p.
9868-72].
Puesto que la deoxihemoglobina,
al contrario de lo que ocurre con las oxihemoglobina,
tiene propiedades paramagnéticas,
un cambio en la saturación de la hemoglobina como reflejo de la oxigenación se puede evaluar como cambios en el T2* del tejido.
Esta propiedad se ha explotado principalmente en estudios de activación neuronal donde las neuronas hiperactivadas por la realización de una tarea,
producen un desequilibrio entre oxihemoglobina y deoxihemoglobina que permite ser caracterizado mediante secuencias (GE-T2*).
La conexión entre los cambios BOLD y la oxigenación del tejido se explica a través de las relación existente entre el oxigeno y la hemoglobina en la sangre.
La deoxihemoglobina cuenta con un átomo de hierro que influye directamente en los campos magnéticos locales produciendo una caída de la señal.
La sangre que fluye a través de las arterias cuenta con un alto porcentaje de oxígeno libre o ligado a hemoglobina.
Cuando la sangre pasa al tejido,
el oxígeno es liberado por la hemoglobina y absorbido por el tejido,
reduciéndose el porcentaje de oxígeno en los vasos y aumentando los niveles relativos de de deoxihemoglobina [Prasad,
P.V.,
et al.,
Breath-hold R2* mapping with a multiple gradient-recalled echo sequence: application to the evaluation of intrarenal oxygenation.
J Magn Reson Imaging,
1997.
7(6): p.
1163-5.].
Como consecuencia del aumento relativo de los niveles de deoxihemoglobina (con propiedades paramagnéticas) se produce una reducción de la relajación T2*.
Estos cambios de T2* se han asociado a cambios en los correspondientes cambios en la presión de oxígeno (pO2) [Glover,
G.H.,
et al.,
Decomposition of inflow and blood oxygen level-dependent (BOLD) effects with dual-echo spiral gradient-recalled echo (GRE) fMRI.
Magn Reson Med,
1996.
35(3): p.
299-308][ Speck,
Functional imaging by I0- and T2*-parameter mapping using multi-image EPI.
Magn Reson Med,
1998.
40(2): p.
243-8].
La tasa de desfase de los espínes,
R2*,
se puede considerer un índice de la oxigenación tisular (R2*=1/T2*).
Aunque esta afirmación en la actualidad está muy debatida,
ya que los cambios T2* se relacionan también con el flujo sanguíneo,
el nivel hematocrito y microestructura tisular (ya que dependen del componente férrico del mismo: por ejemplo la R2* está aumentada de forma basal en la hiperplasia benigna de próstata debido a su alto componente fibrótico o en los ligamentos de Cooper de la mama,
al igual que en la mioglobina muscular...).
En los tumores pueden existir tres tipos de hipoxia:
1ª La debida a la disminución de la perfusión o hipoxia aguda,
consecuencia de las anomalias funcionales y estructurales de la neovascularización tumoral.
Esta es la que se se puede cuantificar con técnica BOLD.
2ª La que depende de la falta de difusión de O2 en los tejidos o hipoxia crónica,
debido a que el O2 no puede "viajar más allá de 70-100 micras de distancia del capilar,
por lo que células tumorales a mayor distancia presentan hipoxia.
3ª Hipoxia anémica,
que se debe a la reducción en la capacidad de transporte de O2 por la hemoglobina en sangre,
normalmente debido por el estado tumoral o al tratamiento.
Estas dos últimas formas de hipoxia no son cuantificables mediante imagen BOLD,
por lo no se puede cuantificar la pO2 en los tejidos de forma basal pero sí los cambios en la misma tras estímulos fisiológicos o farmacocinéticos.
De tal forma que si el flujo sanguíneo es realtivamente alto y la tasa de saturación de la hemoglobina es relativamente corta,
entonces la R2* sólo refleja el flujo sanguíneo en ese tejido.
Si encontramos un tejido perfundido con área con una R2* alta con respecto a otro área del mismo tejido e las mismas circunstancias fisiológicas,
entonces ese aumento de R2* se debe a que en ese área existe una mayor hipoxia.
¿Cómo adquirimos la secuencia y cómo realizamos la cuantificación de R2*?
Como hemos expuesto con anterioridad,
el objetivo de los estudios BOLD es valorar las variaciones del nivel de oxigenación del tejido a través de las variaciones en los valores de T2*.
Para analizar estas variaciones de forma cuantitativa se realizan estudios con secuencias eco de gradiente en las que se adquieren distintos tiempos de eco con el fin de poder estimar mapas paramétricos de T2* del tejido.
En nuestra experiencia la adquisición es mucho más homogénea en campos magnéticos de 3T,
ya que el tiempo de adquisición es mucho más corto y la relación señal/ruido es mayor que en campos magnéticos de 1,5T.
Para una correcta medida de las variaciones de T2* en el tejido es conveniente adquirir todos los TE posibles con el objetivo de tener una mejor estimación de la caída de señal del T2*.
Por otro lado,
para evitar errores en la estimación de los mapas de T2* debidos a la presencia de grasa es conveniente adquirir todos los TE en fase o en fuera de fase,
para reducir en la medida de lo posible los artefactos de desplazamiento químico.
Las adquisiciones tienen que ser en apnea para aquellas zonas sensibles a los movimientos respiratorios como,
por ejemplo,
en estudios hepáticos o renales.
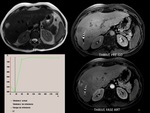
Una vez adquiridos las imágenes es necesario ajustar la señal de los diferentes TE a un modelo monoxponencial (Eq 1) del que se obtienen los valores de T2*:
STE=SOe-Te/T2*
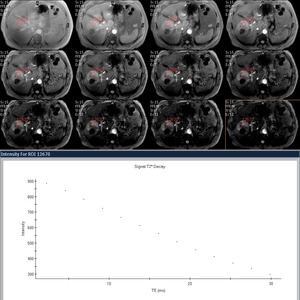
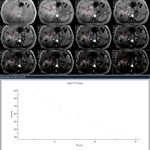
Fig. 1
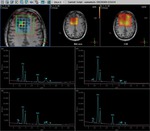
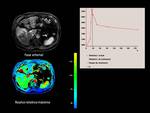
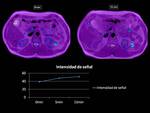
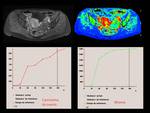
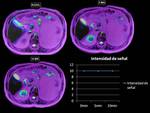
En la Fig.1 se muestran las imágenes de un estudio hepático en un paciente con un hepatocarcinoma,
en el que se adquieren 11 tiempos de eco diferentes durante la misma apnea.
En el gráfico de la Fig.1 se muestra la caída de la señal en la periferia del HCC a medida que aumenta el TE para una región de interés debido a los efectos de la caída de señal T2*.
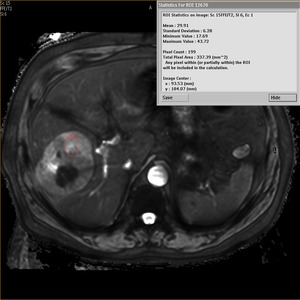
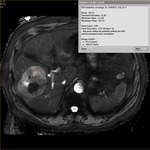
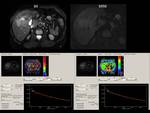
Fig. 2
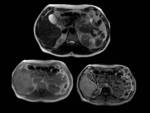
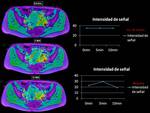
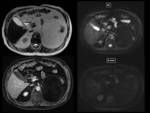
Finalmente,
en la Fig.2 se muestra el mapa paramétrico después de ajustar la señal de cada pixel a un modelo monoexponencial de donde se obtienen los valores de T2*.
Para estudiar la variación de los valores de T2* en función de los niveles de oxigenación es preciso establecer un nivel basal en el que el paciente respire aire de forma convencional.
Bajo estas circunstancia se adquiere un estudio multi-eco eco de gradiente que se utilizará para establecer el nivel inicial de los valores de T2*.
Posteriormente,
en nuestro centro,
se hace respirar al paciente oxigeno puro,
aunque existen estudios realizados bajo la inhalación de carbogen (95% de O2 y 5% de CO2),
Perfluorocan o ambos asociados y se repite la misma adquisición bajo esta nueva situación.
En este caso se asocian variaciones en los mapas de T2* a variaciones del nivel de oxigenación del tejido.
¿Cuales son las diferencias provocadas con la administración de distintos gases?.
-La mayor diferencia entre los estados inducidos de hiperoxia e hipercapnia,
es que la inhalación de gases como el carbogen provoca un aumento del flujo sanguíneo y de oxigenación en sangre,
ya que consigue un importante efecto vasodilatador,
mientras que la sóla administración de O2 a altas concentraciones tan solo aumenta la concentración de O2 en sangre,
por lo tanto las variaciones en la señal T2* van ser mayores al realizar el estudio con hipercapnia que con hiperoxia.
En un estudio de Al-Hallaq et al. se demostró que el aumento de ΔR2* tras la administración de carbogen en tumores cerebrales es del 1,1%,
mientras que en los mismos pacientes el aumento de ΔR2* tras la administración de Perfluorocan y aire es de un 3,3%,
existiendo un incremento significativo cuando se administraban los dos gases en conjunto (6,5%).
- Existe una importante limitación a la hora de utilizar hipercapnia y es que la inhalación de gases como el Carbogen,
tiene unas altas tasas de distress respiratorio (entre un 25 y un 35%),
por lo que en la actualidad se realizan ensayos utilizando concentraciones mucho menores de CO2,
existiendo estudios experimentales en ratas con concentraciones tan solo del 1% de CO2.
¿ Cuáles son las principales aplicaciones clínicas de la imagen BOLD en los distintos órganos y sistemas?
1.
SNC
EN el SNC el uso de la hiperoxigenación ha sido utilizado tanto para la valoración de la perfusión cerebral, como de lesiones tumorales,
en concreto para el análisis de la radiosensibilidad de lesiones neoplásicas sometidas a radioterapia,
ya que se ha demostrado que una mayor perfusión tisular de O2 aumenta el efecto de la misma.
Aunque algunos estudios (Christen et ak,
Radiology 2012) afirman que las secuencias T2 *,
susceptibles al efecto BOLD por los cambios en la concentración de hemoglobina oxigenada,
no son lo suficientemente robustos "per se" para evaluar la perfusión tisular; si se tienen cuenta otros valores como el tiempo de relajación transversal (T2),
Fracción de Volumen sanguíneo y las inhomogeneidades del campo magnético, estas secuencias pueden ser útiles para valorar las áreas de oxigenación intratumorales,
definiendo las zonas probablemente viables y,
a su vez,
más sensibles a la radioterapia.
En el estudio realizado por Rauscher et al.
(Rofo, 2005) concluye que los gliomas de bajo grado muestran caida de R2*,
mientras que los gliomas de alto grado muestran aumento de R2*.
Esto puede ser debido a que en el interior de los gliomas más agresivos exite un flujo vascular caótico y un metabolismo mixto aeróbico y anaeróbico ,
lo que puede provocar que existan áreas con mal aporte de oxígeno por disminución de la vascularización y con bajos niveles de glucosa que impidan el paso de O2 a los tejidos,
lo cual provoca estos cambios contrarios a lo que cabría esperar en cuanto a la señal T2* (exista una subida del R2*,
siendo esperable un descenso del mísmo).
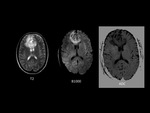
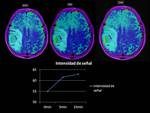
Así en el siguiente ejemplo,
que se trata de una paciente de 30 años con una tumoración frontal que cruza la línea media,
con importante edema asociado,
que presenta marcada restricción de la difusión
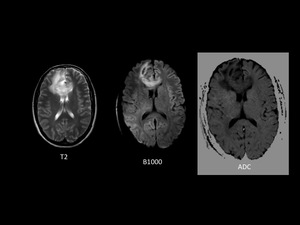
Fig. 3
Fig.3,
con una ratio de volumen cerebral máximo relativo 6 veces mayor que en la sustancia blanca sana,
indicativo de marcada neoangiogénesis
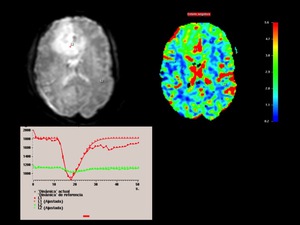
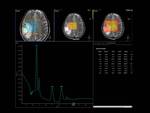
Fig. 5
Fig.4 y una ratio Cho/Cr de 2 en el estudio espectroscópico,
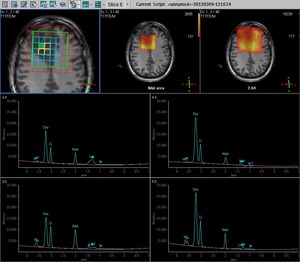
Fig. 4
Fig.5,
lo que indica la posibilidad de una gliomatosis cerebri.
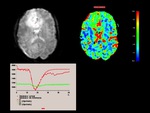
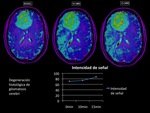
En la secuencia BOLD,
demuestra una caida de la señal R2* tras la administración de O2 a los 10 y 15 min
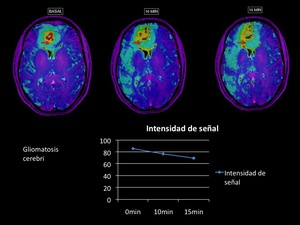
Fig. 6
Fig.6,
confirmando una lesión glial de bajo grado,
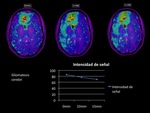
objetivando en un corte más apical (figura 7),
la presencia de un área que presenta aumento de la intensidad de señal R2* lo que indica una zona de degeneración maligna
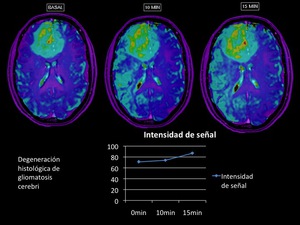
Fig. 7
Fig.7.
El estudio de Müller et al (Eur Radiol 2011),
demostró que los tumores del SNC muestran una respuesta heterogénea e individuo-dependiente ante la hiperoxia e hipercapnia,
ya que los meningiomas muestran una importante caída de la señal T2*,
en las áreas de realce,
tanto con la hiperoxia como con la hipercapnia, mientras que los tumores de alto grado si bien son heterogéneos,
parecen presentar igualmente áreas de caída de señal T2*,
que se correlacionan mayoritariamente con las más perfundidas en las secuencias con gadolinio iv.
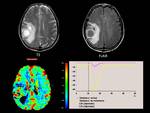
Por tanto en el siguiente estudio que refleja un glioma de alto grado en un varón de 58 años,
que presenta una masa frontoparietal derecha,
con importante edema perilesional,
con una ratio de volumen sanguíneo cerebral relativo 14 veces superior al de la sustancia blanca sana
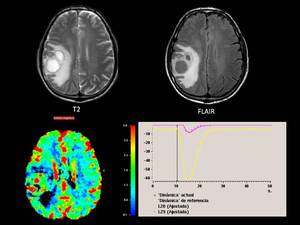
Fig. 8
Fig.8,
con una ratio Cho/Cr superior a 4
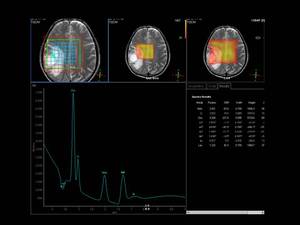
Fig. 9
Fig.9,
presenta un aumento de la señal R2*
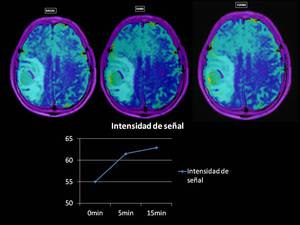
Fig. 10
Fig.10,
lo que indica un aumento de la oxigenación en la lesión, indicativo de área radiosensible en un glioma de alto grado.
2.
Hígado:
Una de las principales aplicaciones de la imagen BOLD con hiperoxia en hígado,
es la capacidad de discernir entre lesiones hiperoxigenadas por alto flujo sanguíneo y con alta tasa de intercambio gaseoso,
lo cual es potencialmente útil para discernir entre lesiones benignas y malignas.
En el siguiente ejemplo visualizamos una lesión ocupante de espacio en segmento 8 hepático,
multilobulada,
marcadamente hipeintensa en T2,
hipointensa en T1,
con un importante realce nodular periférico en fase arterial y permanencia del contraste en fases tardías,
lo que es sugerente de hemangioma
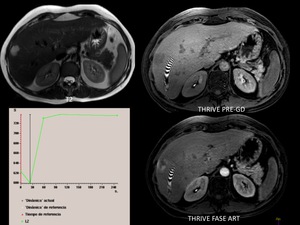
Fig. 11
Fig.11.
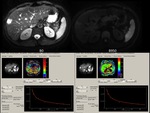
La lesión presenta una mínima hiperintensidad de señal en la secuencia de difusión con b 950 s/mm2,
pudiendo comprobar cómo esa hiperintensidad de señal es debida a la perfusión y no a la difusión de la lesión,
representado en una importante caida de la curva del modelo bicompartimental de la difusión con valores b bajos (inferiores a b 150)
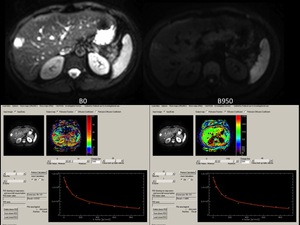
Fig. 12
Fig.
12.
En las imagenes fusionadas de mapas de T2*+ Balanced FE con supresión de la grasa,
como aumenta la señal R2* en los primeros 10min,
aunque de manera no muy significativa,
lo que se debe a un aumento en el flujo sanguíneo de la lesión (aumento de la señal R2*),
aunque probablemente con una baja tasa de transferencia de gases,
al estar formados los hemangiomas por lagos vasculares y septos fibrosos y escasa celularidad
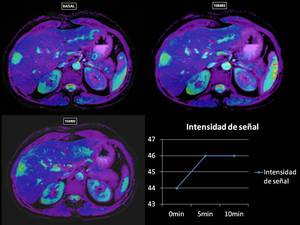
Fig. 13
Fig.13.
Otra lesión benigna hepática es la hiperplasia nodular focal (HNF),
que se muestra típicamente isointensa en T2 con cicatriz central hiperintensa,
con realce intenso en fase arterial en la mayor parte de la lesión,
aunque con ausencia de realce de la cicatriz en esta fase.
El tumor presenta posterior lavado con realce de la cicatriz en fases tardías.
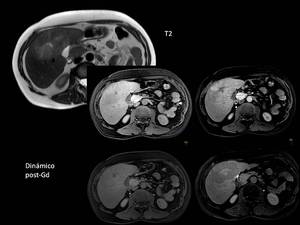
Fig. 14
Fig.
14.
Presentan una mínima restricción de la difusión ,
presentando una caida leve de la curva en el modelo bicompartimental (IVIM),
para los valores b bajos,
con una caída paulatina para b altos,
lo que indica que la ligera restricción de la difusión se debe a su alta celularidad y ocuapción del intersticio.
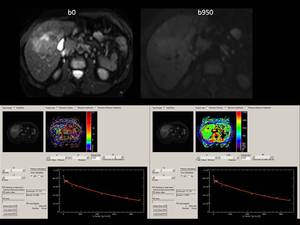
Fig. 15
Fig.15.
En la imagen BOLD vemos como existe un aumento relativo de la señal R2* tras la administración de O2 a los 10min,
aumque no muy significativa,
objetivando valores basales R2* inferiores a los objetivados en el estudio anterior,
lo que indica que el grado de oxigenación de la lesión es mayor en la HNF,
aunque no existe un alto intercambio oxi-desoxiHb,
que aumente la señal,
dato sugerente de lesión de característica benignas.
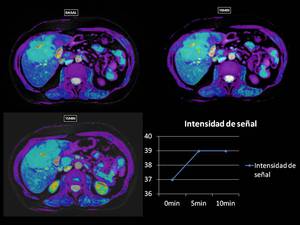
Fig. 16
Fig.16
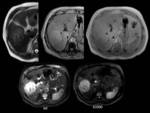
El hepatocarcinoma suele aparecer como masas isointensas en T2,
que pueden presentar áreas de sangrado o necrosis en su interior.
Es típica la pérdida de señal en fase opuesta con respecto a la secuencia en fase si presenta contenido graso, así como una marcada restricción de la difusión.
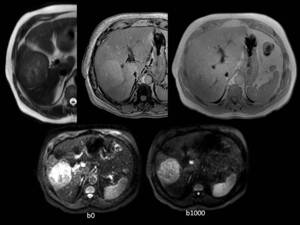
Fig. 17
Fig17.
Su comportamiento vascular patogneumónico es el de una marcada captación en fase arterial y posterior lavado en fase portal- de equilibrio,
con realce periférico capsular tardío.
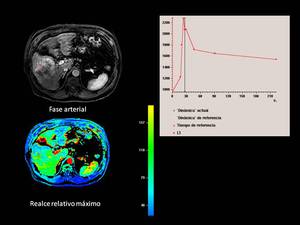
Fig. 18
Fig.18
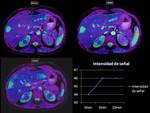
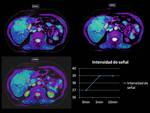
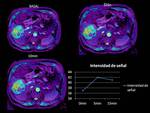
En los mapas de T2*,
podemos visualizar como en este ejemplo aumenta la señal R2* de forma muy importante a los 5 minutos de la administración de O2, incrementando en 5 unidades la intensidad de señal,
lo cual indica que la lesión presenta un aumento de la oxigenación debido probablemente al aumento de la vascularización y de la celularidad,
con aumento de la tasa metabólica tumoral,
como suele ocurrir en la mayoría de las tumoraciones malignas.
Existie un descenso de la intensidad de señal R2* a los 15 minutos,
debido a la saturación de O2 de los tejidos,
impidiendo el intercambio gaseoso oxi-deoxiHb,
visualizando que este fenómeno ocurre en todas lesiones hepáticas estudiadas en nuestro centro a los 15 minutos tras la administración de O2.
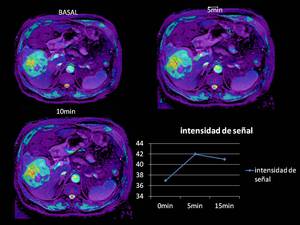
Fig. 19
Fig 19.
3.
Riñón:
La aplicación oncológica más importante de la imagen BOLD con hiperoxia en riñón es la de poder diferenciar entre lesión benigna y maligna,
de tal forma en el siguiente ejemplo se visualiza una lesión quística multitabicada,
hiperintensa en T2,
isointensa en T1,
sin pérdida de señal en fase opuesta con respecto a fase.
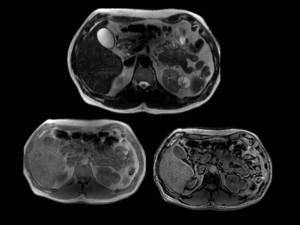
Fig. 20
Fig.20
Que presenta un importante realce en fase arterial y relativo lavado de la misma en fases tardías.
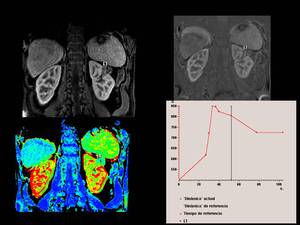
Fig. 21
Fig.21.
Que presenta un incremento marcado de la intensidad de señal R2*,
de al menos 10 unidades,
tras la administración de O2 a los 5 minutos y posterior incremento a los 15 minutos,
lo que indica la alta oxigenación que presenta la lesión ,
indicado probable aumento de la perfusión pero también un importante aumento del consumo de O2,
típico de lesiones tumorales malignas,
como son los carcinomas de células renales.
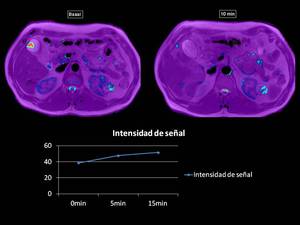
Fig. 22
Fig.
22.
4.
Sistema gastrointestinal:
Aunque la calidad de la imagen de las secuencias BOLD es difícil de conseguir debido al peristaltismo propio de todos los segmentos del tracto digestivo,
que provocan que los cortes adquiridos en los distintos tiempos no sean exactamente iguales,
intentamos reducirlos con la administración de fármacos como el glucagón o butilbromuro de hioscina que provocan una disminución de la peristalsis o realizando las mediciones en los mapas de T2* del volumen tumoral y no de un vóxel,
como en el siguiente ejemplo que se trata de un adenocarcinoma de sigma,
que presenta un importante aumento del R2* a los 10 minutos tras la administración de O2,
existiendo también saturación de O2 de las células tumorales ,
bajando así la señal a los 15 minutos.
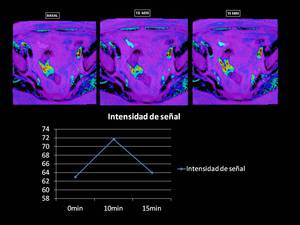
Fig. 23
Fig.
23
Otra importante limitación en este tipo de estudios es la presencia de artefactos de susceptibilidad magnética provocados por las burbujas aéreas en el interior de las asas.
El siguiente caso que mostramos es un segundo ejemplo de lesión tumoral maligna,
en el que visualizamos una tumoración anal,
con extensión al tercio inferior y medio rectal,
con invasión de la zona periférica prostática y con adenopatías en la grasa mesorectal.
Se trataba de un adenocarcinoma mucinoso de ano con extensión rectal.
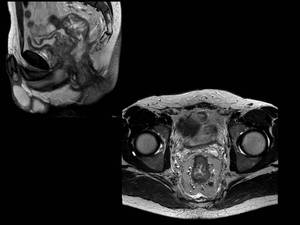
Fig. 24
Fig.
24
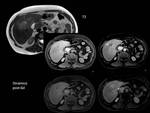
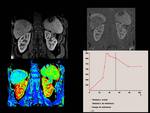
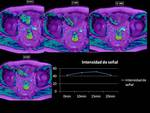
La imagen BOLD muesta un aumento de la intensidad de señal en el mapa T2* tras la administración de O2 significativo a los 5 minutos,
siendo mucho más paulatino en el tiempo restante,
no produciendose en este caso la saturación celular de O2 a los 15 minutos si no a los 20 minutos tras la administración de O2.
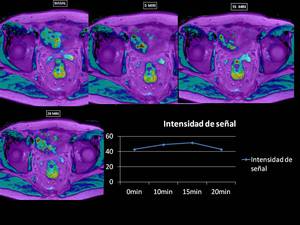
Fig. 25
Fig.25
5.
Pelvis femenina:
Existe escasa literatura que se ocupe de las aplicaciones clínicas del BOLD en pelvis femenina,
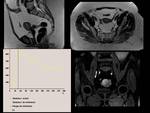
aunque en el siguiente ejemplo visualizamos una paciente con un útero polimiomatoso y un a masa anexial derecha,
que aunque es bien definida presenta un área central de necrosis e importante restricción de la difusión.
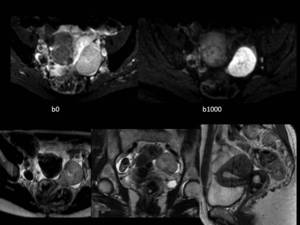
Fig. 26
Fig.26.
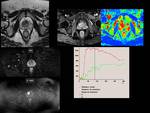
Visualizamos una escasa captación tras la administración de gadolinio de la lesión ovárica,
correspondiente a un carcinoma de ovario,
mientras que se objetiva una importante captación progresiva en el interior del mioma.
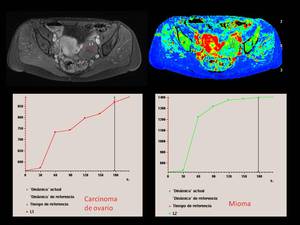
Fig. 27
Fig.
27.
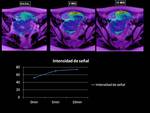
No visualizamos cambios en la intensidad de señal en mapas de T2*,
en la lesión ovárica,
lo que puede indicar su baja tasa de oxigenación y por lo tanto radioresistencia.
De forma contraria visualizamos un discreto aumento de la señal R2* a los 5 minutos tras la administración de O2,
provocandose saturación celular de O2 muy temprana,
a los 10minutos,
provocando disminución en la señal.
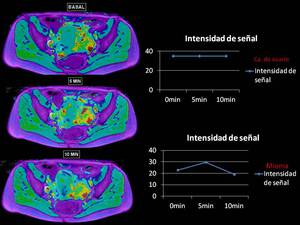
Fig. 28
Fig.
28.
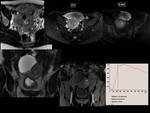
Otro ejemplo,
en este caso un cistoadenocarcinoma mucinoso de ovario izquierdo,
en el que visualizando una gran masa mixta dependiente del ovario izquierdo,
con importante restricción de la difusión del polo sólido y captación en fases tempranas y posterior lavado relativo del mismo.
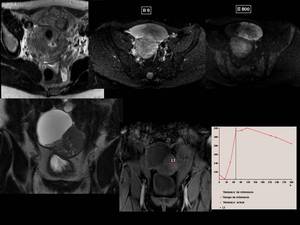
Fig. 33
Fig.
29.
En la imagen BOLD vemos como sube la intensidad de señal R2* de forma importante tras la administración de O2 a los 5 minutos,
siendo más paulatina a los 10 minutos. Indicativo una vez más de tumor muy oxigenado, indicativo de malignidad.
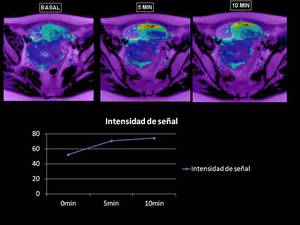
Fig. 34
Fig.
30.
También se comporta como el resto de lesiones tumorales con cierto grado de malignidad el carcinoma de endometrio,
visualizando en el siguiente ejemplo una pequeña masa ligeramente hiperintensa en secuencias potenciadas en T2 en la cavidad endometrial,
que invade la práctica totalidad del miometrio,
sin sobrepasarlo.
La lesión presenta una curva de perfusión ascendente en fase arterial,
con posterior lavado de la misma.
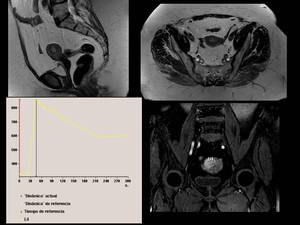
Fig. 31
Fig 31.
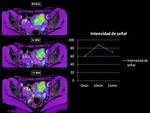
En imagen BOLD visualizamos un aumento paulatino de la señal R2* tras la administración de O2,
lo que indica lesión maligna endometrial ,
en paciente que presenta un adenocarcinoma de endometrio bien diferenciado.
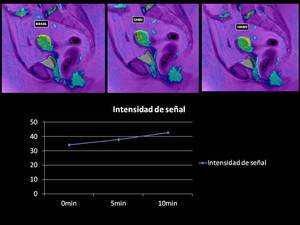
Fig. 32
Fig.32.
7.
Pelvis masculina:
Una de las aplicaciones más validadas de la imagen BOLD es el mapeo de radioresistencia en carcinoma de próstata,
siendo muy importante en estos pacientes conocer las áreas tumorales con bajos niveles de O2,
ya que estos pacientes se beneficiarán de una combinación de radioterapia y tratamientos angiogénicos.
También se ha comprobado que los tumores más hipoxicos presentan peores resultados tras tratamiento a los 8 años con respecto a los que tenían altos niveles de O2,
por lo que es también un factor pronóstico.
Según Padhani et al.
altos valores de señal R2* se asocian a hipoxia,
mientras que bajos valores R2* no se asocian a la misma.
En el siguiente ejemplo visualizamos una tumoración en la zona central,
que invade mínimamente a la zona periférica,
en la región apical,
medioglandular derecha,
que presenta una curva de perfusión tipo 3 (importante captación incicial y lavado posterior de la misma),
con una relación Cho/Cr muy aumentada,
por lo tanto sugerentes de malignidad y marcada restricción de la difusión con un valor b:2000.
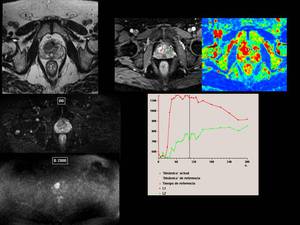
Fig. 29
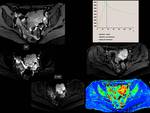
Fig.33En la imagen BOLD objetivamos un aumento en la intensidad de señal R2* hasta los 10 minutos tras la administración de O2,
existiendo estabilidad de la misma a los 15 minutos por saturación de O2 celular, indicando que el tumor presenta incremento de la oxigenación con la hiperoxia en relación con un tumor maligno de alto grado y probablemente mínimamente radiosensible,
ya que el aumento de señal no es muy significativo,
aunque sí se podría beneficiar de fármacos radiosensibilizadores.
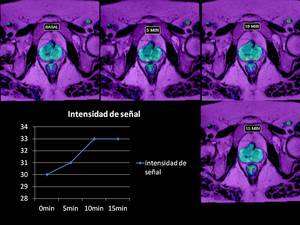
Fig. 30
Fig.34
8.
Otras lesiones:
En el siguiente ejemplo objetivamos una gran masa retroperitoneal izquierda con contenido de grasa macroscópica,
con bordes engrosados,
con restricción de la difusión de los últimos y realce periférico,
compatible con liposarcoma retroperitoneal.
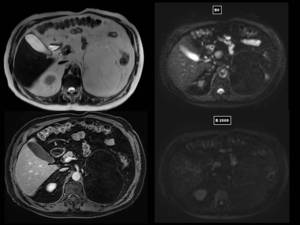
Fig. 35
Fig.
35
En la imagen BOLD vemos como no varía la señal R2*,
debido a que existe escasa celularidad.
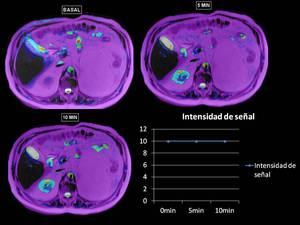
Fig. 36
Fig.36 El último ejemplo,
se trata de una masa pélvica mulltilobulada,
sólida,
que presernta una importantísima restricción de la difusión e importante captación tras la administración de gadolinio en fase arterial y posterior lavado de la misma.
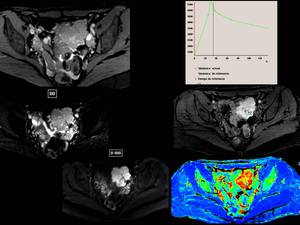
Fig. 37
Fig.
37.
La masa presenta un importante aumento de la señal R2* de hasta 24 unidades a los 10 minutos tras la administración de O2,
lo que indica una importantísima oxigenación tumoral,
en relación con la alta vascularización y celularidad que presentan los linfomas,
patología que presentaba la paciente.
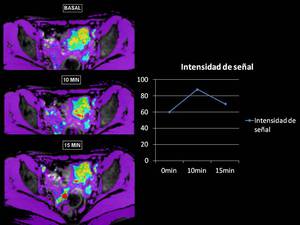
Fig. 38
Fig.
38.