♦ INTRODUCCIÓN
El aporte arterial sistémico al pulmón puede desarrollarse de forma congénita o en relación con procesos patológicos adquiridos,
dentro de un amplio espectro que abarca entidades con muy variada etiología pero una característica común: la irrigación por una o más arterias sistémicas de una parte del pulmón,
sano o patológico,
que en circunstancias normales estaría nutrido por arterias pulmonares.
El reconocimiento de estos vasos es relevante porque son fuente potencial de hemoptisis,
en algunos casos masiva.
En esto casos el angio-TC es una herramienta útil para identificar el origen de la hemoptisis antes de la angiografía intervencionista con intención terapéutica.
Además la identificación y descripción de las arterias sistémicas asiste al cirujano en la planificación de la técnica quirúrgica,
en en caso de secuestro pulmonar o cuando el AAS tiene lugar en el contexto de cardiopatías congénitas.
Tradicionalmente la descripción de las arterias anormales que irrigan al pulmón requería angiografía convencional,
que es un método invasivo que utiliza contraste endovenoso.
Actualmente la angiografía por TC o RM permite obviar aquel procedimiento cuando tiene intención exclusivamente diagnóstica,
y no terapéutica (embolización).
♦ CLASIFICACIÓN
AAS al pulmón se clasifica en normal o anomal según los vasos responsables del mismo: 1) arterias bronquiales; 2) conducto arterioso persistente,
considerado anormal tras el nacimiento; 3) colaterales aortopulmonares mayores (CAPM); 4) origen directo de las arterias pulmonares desde la aorta; 5) otras conexiones entre las arterias sistémicas y las arterias pulmonares,
como las fistulas coronario-pulmonares.
También se clasifica de acuerdo con la naturaleza congénita o adquirida de la entidad asociada al AAS.
♦ AAS AL PULMÓN EN ENFERMEDAD PULMONAR ADQUIRIDA
Muchas patologías pulmonares adquiridas pueden recibir irrigación de arterias sistémicas,
generalmente arterias bronquiales,
aunque otras arterias sistémicas pueden estar implicadas.
Con mayor frecuencia observamos este fenómeno en bronquiectasias,
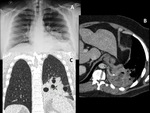
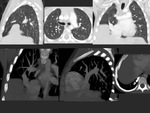
secuelas de tuberculosis pulmonar [FIGURA 1,
FIGURA 2] ,
otras infecciones pulmonares,
así como enfermedad pulmonar obstructiva crónica (EPOC) [FIGURA 3,
FIGURA 4].
También es frecuente la asociación con tromboembolismo pulmonar [FIGURA 5],
y pueden asociarse a otras causas de obstrucción arterial crónica [FIGURA 6],
como la arteritis de Takayasu,
que a menudo afecta la arteria pulmonar al igual que la aorta y sus ramas.
Menos frecuentemente se ha descrito AAS en otras patologías del pulmón y la pleura,
como linfomas y neoplasias [FIGURA 7].
Las arterias bronquiales aportan flujo sistémico al pulmón desde el nacimiento,
y son responsables de entre el 1% y 5% del flujo arterial al pulmón en condiciones normales.
Irrigan las paredes arterias pulmonares y las estructuras de soporte de la vía aérea. La anatomía de las arterias bronquiales ha sido suficientemente descrita pero tiene una amplia variabilidad.
Caldwell et al describieron cuatro patrones de origen y ramificación clásicos,
que representan alrededor del 93% de los casos [FIGURA 8].
Normalmente son una o dos arterias que nutren a cada pulmón,
y nacen de forma independiente desde la aorta o desde un tronco común.
En general en el lado derecho está presente un tronco intercostobronquial con origen en el margen posterointerno de la aorta descendente,
al que sigue un trayecto vertical en sentido craneal antes de ramificarse en arterias intercostales posteriores y una arteria bronquial derecha [FIGURA 3,
FIGURA 6].
Esta arteria es la que se identifica con mayor fiabilidad en la angiografía (80% de los individuos).
En el 70% de los casos hay dos arterias bronquiales izquierdas y además del tronco intercostobronquial derecho.
En el 70% de la población general las arterias bronquiales las arterias bronquiales nacen de la aorta descendente,
en general entre los niveles T5 y T6.
Las que toman origen en otros niveles son consideradas anómalas.
Estos orígenes anómalos pueden ser el arco aórtico,
la arteria mamaria interna [FIGURA 9],
el tronco tirocervical,
arteria subclavia,
tronco costocervical,
arteria braquiocefálica,
pericardiofrénica,
frénica inferior o aorta abdominal.
Las arterias bronquiales en general son vasos pequeños (<2 mm de diámetro) pero se pueden hipertrofiar para reemplazar a la circulación pulmonar en condiciones patológicas,
cuando el flujo arterial pulmonar se reduce o interrumpe en el nivel de las arteriolas pulmonares por vasoconstricción hipóxica,
trombosis intravascular y vasculitis.
El flujo arterial bajo presión sistémica puede desencadenar hemoptisis.
Las arterias bronquiales son las responsables del sangrado en el 90% de los casos de hemoptisis que requieren embolización o cirugía.
Las arterias bronquiales hipertrofiadas se reconocen como vasos tortuosos que realzan,
de al menos 2-3 mm de diámetro,
en el seno del tejido blando del mediastino,
generalmente retrotraqueal,
retroesofágico,
pared posterior del bronquio principal,
ventana aortopulmonar,
que discurre hacia los pulmones y sigue trayectorias paralelas a los bronquios centrales.
El curso predominante es perpendicular al plano axial por lo que aparecen muchas veces como agrupaciones de nódulos que realzan intensamente en mediastino posterior,
en general bajo el nivel del arco aórtico [FIGURA 1,
FIGURA 3,
FIGURA 4].
Además las arterias sistémicas no-bronquiales se pueden dilatar e hipertrofiar para proveer de flujo colateral a tejido pulmonar patológico a través de anastomosis transpleurales con las arterias pulmonares.
Esto sucede en general cuando se dan adherencias pleurales secundarias a inflamación.
Estas arterias no-bronquiales pueden tomar origen desde arterias frénicas,
intercostales,
mamarias internas,
tirocervical y otras ramas de las arterias subclavias y axilares [FIGURA 1].
Estas arterias sistémicas no-bronquiales se pueden distinguir de arterias bronquiales anómalas anatómica y angiográficamente porque se introducen en el pulmón a través de la pleura o el ligamento pulmonar,
además su trayecto no es paralelo al de los bronquios,
al contrario de lo que sucede con las arterias bronquiales.
El reconocimiento de estas arterias no-bronquiales y de las arterias bronquiales con origen anómalo [FIGURA 9] es esencial para el éxito de la embolización percutánea en caso de hemoptisis.
♦ AAS AL PULMÓN asociado a enfermedad CONGÉNITA
El aporte arterial sistémico anómalo al pulmón ya establecido al nacimiento puede estar asociado a cardiopatías congénitas,
enfermedad pulmonar congénita o,
de forma poco frecuente,
puede irrigar a parénquima pulmonar normal.
- AAS AL PULMÓN EN CARDIOPATÍAS CONGÉNITAS
Las vías potenciales de irrigación arterial al pulmón desde el circuito sistémico en caso de enfermedad cardiaca congénita incluyen: a) el origen de las arterias pulmonares directamente desde la aorta (truncus arteriosus); b) conducto arterioso persistente; y c) arterias colaterales aortopulmonares mayores (CAPMs).
En ciertas cardiopatías congénitas las arterias bronquiales u otras arterias sistémicas no-bronquiales normales pueden hipertrofiarse tras el nacimiento para irrigar a parénquima hipoperfundido por la vía arterial pulmonar correspondiente.
Por tanto,
en sentido estricto,
esta vía de AAS no sería congénita,
pues no está establecida intraútero,
sino que la consideración de congénita se aplica a la cardiopatía que da origen al desarrollo de estas vías de AAS por vasos normalmente desarrollados,
que posteriormente se hipertrofian [FIGURA 10].
Las colaterales aortopulmonares mayores (CAPMs) son una fuente potencial de flujo colateral en algunas cardiopatías congénitas,
como sucede en aproximadamente el 50% de los casos de atresia pulmonar con comunicación intraventricular (CIV) [FIGURA 11],
[FIGURA 12] y [FIGURA 13].
Existe cierta controversia sobre el origen embriológico de estas arterias.
En general se acepta la hipótesis de que suponen la anormal persistencia de alguna de las arterias que forman los siete pares de arterias post-branquiales que nutren las yemas pulmonares primitivas antes del desarrollo de la arteria pulmonar desde el sexto arco aórtico.
Sin embargo hay hipótesis que sostienen que se derivan de arterias bronquiales dilatadas,
dado que comparten características anatómicas similares.
En contra de esta afirmación algunos arguyen que las CAPMs ya están presentes en el nacimiento,
al contrario que las arterias bronquiales y otras sistémicas,
que se hipertrofian después.
Las CAPMs son arterias de calibre relativamente grande que típicamente se originan en aorta descendente,
aunque también pueden salir desde el arco o los troncos braquiocefálicos [FIGURA 13].
El patrón de estos vasos en cuanto a trayecto,
conexiones y cambios de calibre es muy variable.
Es frecuente la disminución abrupta de calibre por proliferación intimal en el nivel de la anastomosis con las arterias pulmonares o algo proximal a ésta [FIGURA 11].
Dicha anastomosis con las arterias intrapulmonares tiene lugar de forma característica en el hilio o cerca del mismo en lugar de en la periferia.
- AGENESIA O INTERRUPCIÓN PROXIMAL DE LA ARTERIA PULMONAR DERECHA O IZQUIERDA
Esta entidad es una alteración congénita muy infrecuente de la que resulta que el pulmón unilateral a la anomalía dependa casi por completo de la irrigación arterial sistémica.
Aunque la arteria pulmonar termina en el hilio como un muñón ciego,
se prefiere el término interrupción dado que las arterias pulmonares distales a ella suelen estar intactas y permeables.
Esta anomalía afecta con mayor frecuencia a la arteria pulmonar derecha y en general se trata de una anomalía aislada [FIGURA 14].
Por el contrario,
cuando afecta a la arteria pulmonar izquierda en general se asocia a enfermedad cardiaca congénita,
usualmente tetralogía de Fallot,
y de no ser así el arco aórtico casi siempre derecho.
Estos pacientes suelen desarrollar hipertensión pulmonar,
infecciones pulmonares y hemoptisis causada con la circulación colateral.
El AAS al pulmón en estos casos procede de rica circulación bronquial colateral adquirida durante la infancia.
También puede desarrollarse circulación transpleural a partir de ramas de arterias intercostales,
mamaria interna,
subclavia e innominada.
Esta circulación transpleural puede ser tan prominente que se haga visible como engrosamiento pleural y muescas costales en la radiografía de tórax.
El pulmón ipsilateral generalmente tiene menor tamaño y mayor densidad de lo normal.
Los vasos hiliares del otro pulmón normalmente aumentan de calibre mientras que en el hilio ipsilateral a la anomalía son muy pequeños o incluso aparentemente ausentes.
- ENFERMEDAD PULMONAR CONGÉNITA
Entre las alteraciones congénitas del pulmón solo el secuestro pulmonar y el síndrome venolobar pulmonar congénito se han asociado sistemáticamente a una alta prevalencia a irrigación arterial sistémica desde la aorta a travé de ramas anormales,
denominadas aberrantes,
que se consideran remanentes de las ramas aórticas primitivas que originalmente irrigan a la yema pulmonar en la vida fetal,
por tanto pueden también considerarse arterias colaterales aortopulmonares mayores (CAPMs),
arriba descritas.
El secuestro pulmonar generalmente se define como parénquima pulmonar no funcionante que no está en normal comunicación con el árbol traqueobronquial,
y que recibe su aporte arterial a partir de vasos sistémicos.
La arteria aberrante,
no relacionada con cardiopatía congénita,
normalmente tiene 6 o 7 mm de diámetro y se origina en la aorta descendente torácica baja o en la abdominal alta.
También puede originarse en una rama principal de la aorta abdominal,
como el tronco celíaco [FIGURA 15].
Típicamente ingresa al pulmón vía ligamento pulmonar.
En el 15% a 20% de los casos las arterias son múltiples [FIGURA 16].
Es frecuente que tras la infancia aparezcan cambios ateromatosos sobre ellas [FIGURA 17],
[FIGURA18].
La mayoría de los secuestros son intralobares (75% de los casos),
es decir,
que el parénquima secuestrado comparte revestimiento pleural visceral con el lóbulo pulmonar sano,
al contrario de lo que sucede en el tipo extralobar.
El drenaje venoso en los secuestros intralobares es normal,
a través de las venas pulmonares en aurícula izquierda.
Suelen localizarse en los lóbulos inferiores,
con mayor frecuencia en el pulmón izquierdo.
Es característica la presencia de uno o más quistes en el parénquima secuestrado [FIGURA 18].
El bronquio secuestrado puede estar distendido por tapones de moco [FIGURA 16].
Son frecuentes los cambios inflamatorios secundarios a infección que incluso se cronifica,
debido al mal drenaje de estas áreas.
También hemos observado en nuestros casos hiperclaridad del parénquima secuestrado,
que muy probablemente traduce atrapamiento aéreo [FIGURA 16].
Una arteria aberrante puede irrigar a parénquima pulmonar normal.
esta entidad se denomina arterialización sistémica anómala a segmentos pulmonares basales normales.
El parénquima que recibe la irrigación anómala tiene comunicación normal con el árbol traqueobronquial,
a diferencia del parénquima secuestrado.
El síndrome venolobar pulmonar congénito está compuesto por una serie de alteraciones,
cada uno de los cuales representa una anomalía congénita del tórax claramente diferenciada,
con entidad propia.
Entre las principales o esenciales se incluyen el pulmón hipogenético (o hipoplásico),
drenaje venoso pulmonar anómalo parcial,
secuestro pulmonar,
irrigación por arteria aberrante sistémica a parénquima no secuestrado,
ausencia de vena cava inferior,
duplicación del diafragma,
incluso agenesia de una arteria pulmonar.
Cuando el pulmón hipogenético coexiste con drenaje venoso anómalo parcial la entidad se conoce como síndrome de la cimitarra,
que casi exclusivamente afecta al pulmón derecho.
La imagen de la cimitarra simulando una espada turca se configura por la vena anómala que drena,
parcial o totalmente,
el pulmón derecho en la vena cava inferior,
justo encima o debajo del diafragma [FIGURA 19].
Este pulmón hipogenético en el síndrome de la cimitarra también puede recibir aporte desde la aorta por una arteria aberrante [FIGURA 15],
que puede irrigar áreas de pulmón secuestrado.