El cГЎncer colorrectal es una importante causa de morbilidad y mortalidad en los paГӯses desarrollados de forma que supone la segunda causa de muerte por cГЎncer y es el mГЎs frecuente si consideramos ambos sexos en conjunto.
El cГЎncer de recto alcanza hasta un 30% de los casos y tiene peor pronГіstico por su mayor frecuencia de recidiva local y metГЎstasis.
En los Гәltimos aГұos la historia natural de la enfermedad se ha visto modificada por un cambio en el abordaje terapГ©utico en los casos localmente avanzados,
con la generalizaciГіn del empleo de tratamiento neoadyuvante prequirГәrgico con quimio y radioterapia (QRT) y el refinamiento de la cirugГӯa con la instauraciГіn de la excisiГіn total del mesorrecto (ETM) como tГ©cnica quirГәrgica estГЎndar.
Esto ha permitido mejorar la resecabilidad con resultados postquirГәrgicos mГЎs funcionales gracias a la preservaciГіn del complejo esfinteriano,
un mejor control local de la enfermedad disminuyendo las tasas de recidiva local y sobretodo un aumento de la supervivencia libre de enfermedad.
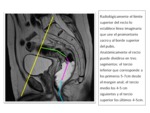
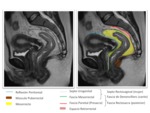
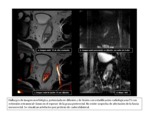
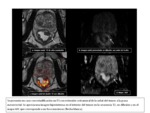
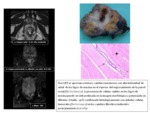
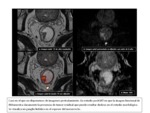
La resonancia magnГ©tica (RM) de alta resoluciГіn aporta una excelente definiciГіn de las marcas anatГіmicas importantes para la cirugГӯa del cГЎncer de recto,
siendo una herramienta esencial en la planificaciГіn quirГәrgica,
tanto en aquellos casos en los que se plantea como tratamiento inicial como en los que han recibido neoadyuvancia con QRT (Fig.
1 - 3).
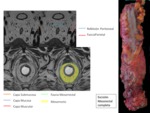
La ETM se basa en la resecciГіn en bloque de la grasa mesorrectal incluyendo la vГӯa de drenaje linfГЎtico y vascular del recto,
estableciendo como plano quirГәrgico la fascia mesorrectal que lo envuelve y que debe extraerse Гӯntegra.
Debe sospecharse una invasiГіn histolГіgica de la fascia cuando la extensiГіn del tumor se aproxima a 1-2 mm de la misma en el estudio de RM,
lo que supondrГӯa que no es posible conseguir un margen quirГәrgico libre de enfermedad.
Aunque tradicionalmente se ha empleado el tГ©rmino margen de resecciГіn circunferencial (MRC) para referirse a la proximidad o invasiГіn de la fascia mesorrectal por el tumor,
puesto que Г©sta es el plano de la ETM,
recientemente se ha propuesto no usar este tГ©rmino en el futuro y describir los hallazgos en relaciГіn a las estructuras anatГіmicas adyacentes dado que existen casos en los que se realiza una resecciГіn quirГәrgica mГЎs amplia,
especialmente en los tumores de recto bajo.
Se ha demostrado que el empleo de un mayor nГәmero de secuencias no mejora la precisiГіn diagnГіstica del estudio de RM y la administraciГіn de contraste no aporta informaciГіn adicional.
En nuestro centro,
una vez que el paciente tiene la confirmaciГіn histolГіgica de cГЎncer de recto,
empleamos un protocolo de estudio que consta de dos secuencias FSE T2 en el plano sagital y axial,
una secuencia FSE T2 de alta resoluciГіn en el plano axial al tumor a la que se aГұade un plano coronal al canal anal en caso de tratarse de un recto bajo y finalmente una secuencia eco planar potenciada en difusiГіn en plano axial (Tabla 1).
Se indica la administraciГіn de un enema de limpieza tres horas antes y se introducen 50 ml de gel ecogrГЎfico por vГӯa rectal mediante una cГЎnula inmediatamente antes de la exploraciГіn con el fin de conseguir una adecuada distensiГіn y mejorar en contraste entre el tumor y la luz rectal.
Disponemos de una unidad Avanto Siemens de 1,5T.
A lo largo del texto y en las figuras emplearemos la nomenclatura propuesta por MorГЎn y cols.
de forma que el tГ©rmino mrT corresponde a la categorГӯa T del tumor antes de QRT,
el tГ©rmino ymrT corresponde a la categorГӯa T del tumor despuГ©s de QRT y el tГ©rmino ypT corresponde a la categorГӯa T del tumor en la evaluaciГіn histolГіgica tras QRT.
La RM juega un papel esencial en la evaluaciГіn de los pacientes con cГЎncer de recto.
En la actualidad la RM de alta resoluciГіn estГЎ considerada la tГ©cnica de imagen mГЎs precisa para establecer la estadificaciГіn local prequirГәrgica gracias a su capacidad para identificar varios factores pronГіsticos como la profundidad de la extensiГіn tumoral extramural,
la presencia de adenopatГӯas metastГЎsicas,
la invasiГіn venosa extramural y la amenaza del margen de resecciГіn circunferencial.
Aunque la ecografГӯa endoanal ha demostrado una precisiГіn diagnГіstica comparable en la valoraciГіn de la afectaciГіn de la pared (T) y la presencia de adenopatГӯas patolГіgicas (N) tiene importantes limitaciones como la dependencia del operador y lesiones estenosantes o alejadas del margen anal y ademГЎs no permite una evaluaciГіn adecuada del margen de resecciГіn circunferencial o de la invasiГіn venosa extramural.
Aunque estudios recientes muestran una aceptable concordancia de la TC multidetector en la evaluaciГіn de la extensiГіn tumoral,
la fascia mesorrectal y las adenopatГӯas locales no existe la suficiente correlaciГіn con los hallazgos de RM que le permitan sustituirla.
Existen estudios que demuestran que la selecciГіn del tratamiento mГЎs adecuado en pacientes con cГЎncer de recto se consigue en grupos multidisciplinares sobre la base de las imГЎgenes de RM que permiten identificar aquellos que se beneficiarГЎn de un tratamiento de QRT neoadyuvante y los que no.
En nuestro centro se realiza un comitГ© multidisciplinar semanal donde se determinan aquellos pacientes con estadio radiolГіgico mrT3 con sospecha de infiltraciГіn de la fascia mesorrectal,
mГәsculos elevadores o plano esfinteriano,
estadio mrT4 y N1 para un tratamiento de ciclo largo de QRT.
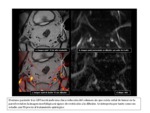
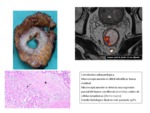
La identificaciГіn y estadiaje del cГЎncer de recto en RM convencional se basa en las diferencias de intensidad de seГұal en la secuencia potenciada en T2 entre el tumor y las capas de la pared rectal.
El tumor tiene una intensidad de seГұal intermedia entre la alta seГұal de la capa submucosa y el tejido graso y la baja seГұal de la mucosa y la capa muscular.
La secuencia de RM potenciada en difusiГіn es una modalidad de imagen funcional emergente que explora el movimiento aleatorio de las molГ©culas de agua en los tejidos biolГіgicos modificado y limitado por la interacciГіn con membranas celulares y macromolГ©culas.
Los tumores debido a su hipercelularidad de forma general muestran restricciГіn a la difusiГіn.
La imagen se obtiene aplicando gradientes en los tres planos del espacio sobre la base de una secuencia potenciada en T2 en la que la intensidad del pulso aplicado se representa por el valor de b.
Empleando varios valores de b es posible realizar un anГЎlisis cuantitativo mediante el cГЎlculo de mapas de coeficiente de difusiГіn aparente (ADC).
Deben evaluarse las imГЎgenes con valor alto de b (800 o 1000 s/mm2) junto con las imГЎgenes del mapa ADC para evitar errores en la interpretaciГіn por tejidos con alta seГұal en secuencias T2 y como consecuencia de ello en la secuencia de difusiГіn ("efecto T2").
El potencial valor de la secuencia potenciada en difusiГіn con alto valor de b en la detecciГіn del cГЎncer colorrectal se ha comunicado en estudios recientes.
Debido a la baja relaciГіn seГұal-ruido en dicha secuencia la fusiГіn de la misma con la imagen potenciada en T2 permite una mejor detecciГіn del tumor y las adenopatГӯas locales.
Puesto que el tratamiento neoadyuvante de QRT permite alcanzar elevadas tasas de respuesta completa (30%) y de respuesta parcial con disminuciГіn del estadiaje inicial (60%),
lo que se asocia con un mejor pronГіstico,
algunos grupos han comunicado excelentes resultados a largo plazo incluso en ausencia de tratamiento quirГәrgico posterior,
lo que pone en cuestiГіn la necesidad un abordaje quirГәrgico agresivo en casos seleccionados.
Sobre la base de este hecho,
una estrategia de вҖңesperar y verвҖқ o resecciones quirГәrgicas menos extensas como la excisiГіn local transanal podrГӯa contemplarse en pacientes con buena respuesta clГӯnica.
Para ello es necesario disponer de una herramienta precisa en la evaluaciГіn tras el tratamiento de QRT.
A pesar de la gran exactitud diagnГіstica de la RM en el estudio previo al tratamiento,
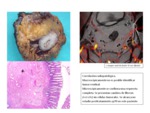
la aplicaciГіn de criterios morfolГіgicos tiene una utilidad limitada en la imagen postratamiento para diferenciar entre tumor viable,
tejido fibrГіtico y reacciГіn inflamatoria condicionando generalmente una sobreestadificaciГіn del paciente,
especialmente en la variedad de adenocarcinoma mucinoso.
Este tipo de tumores muestran una alta intensidad de seГұal tras neoadyuvancia con pocos cambios morfolГіgicos que puede interpretarse errГіneamente como persistencia tumoral cuando histolГіgicamente sГіlo se detectan lagos de mucina sin tumor activo.
Se detectan casos de diferenciaciГіn mucinosa tras QRT sin que esto parezca ser un factor pronГіstico en sГӯ mismo.
Aunque recientemente se ha comunicado que la combinaciГіn del volumen tumoral inicial y la reducciГіn del mismo tras QRT puede predecir un estadio postquirГәrgico ypT0-2,
su correlaciГіn con la disminuciГіn del estadio histolГіgico estГЎ en discusiГіn.
AdemГЎs la reducciГіn de volumen del tumor no permite predecir precozmente la respuesta al mismo durante el tratamiento.
Si bien la existencia de diferencias en la microcirculaciГіn puede hipotГ©ticamente permitir que estudios de perfusiГіn sean capaces de diferenciar cГ©lulas malignas viables de las no viables,
la complejidad en el postprocesado de los mismos y la inconsistencia de sus resultados no han permitido su generalizaciГіn en la prГЎctica clГӯnica diaria.
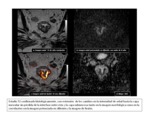
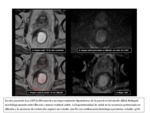
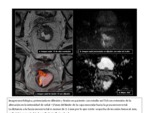
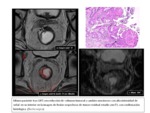
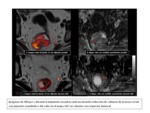
En cambio existe una evidencia creciente en la literatura que sugiere que la suma de imГЎgenes potenciadas en difusiГіn a imГЎgenes potenciadas en T2 mejora la precisiГіn diagnГіstica hasta un 80-85% en los casos de respuesta completa,
con una predicciГіn de ausencia de infiltraciГіn de la fascia mesorrectal del 89-93% con el valor aГұadido de una excelente correlaciГіn interobservador (Fig.
4-14).
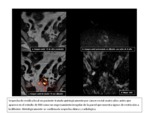
En cuanto a la evaluaciГіn del cГЎncer de recto durante el tratamiento neoadyuvante de QRT,
varios trabajos han demostrado la capacidad de la imagen de RM potenciada en difusiГіn en la evaluaciГіn de la respuesta terapГ©utica incluso de una forma tan temprana como a la semana del inicio del mismo mediante la detecciГіn de un incremento significativo en el valor del mapa ADC del tumor (Fig.
15).
La determinaciГіn de un valor bajo del mapa ADC previo al tratamiento podrГӯa correlacionarse igualmente con una buena respuesta posterior al tratamiento.
Los cambios morfolГіgicos en cambio se producen tardГӯamente en el curso del tratamiento por lo que no son Гәtiles en la monitorizaciГіn precoz del tratamiento de QRT.
La posibilidad de detectar precozmente aquellos pacientes no respondedores puede permitir la intensificaciГіn del tratamiento o un cambio en la decisiГіn terapГ©utica inicial.
Por otro lado aunque la recomendaciГіn habitual es operar al paciente a las 6-8 semanas tras finalizar el ciclo de QRT,
que se basa en antiguos estudios de radiaciГіn vesical seguidos de cistectomГӯa,
se han comunicado casos de persistencia en la respuesta que llegan hasta las 12 semanas despuГ©s del tratamiento.
Esto sugiere que quizГЎ en un futuro deba replantarse el momento adecuado del tratamiento quirГәrgico tras neoadyuvancia.
En aquellos casos de sospecha clГӯnica de recidiva local,
que suele localizarse en la regiГіn perianastomГіtica,
presacra o en el suelo de la pelvis,
existe indicaciГіn de estudio de RM para identificar dicha recidiva y valorar su extensiГіn,
pero no estГЎ justificada de forma rutinaria como parte del seguimiento postquirГәrgico del cГЎncer de recto (Fig.16).
REFERENCIAS
Sauer R,
Becker H,
Hohenberger W,
et al.
Preoperative versus postoperative Chemoradiotherapy for rectal cancer.
N.Engl J.Med 2004;351:1731-40
NCCN Clinical guidelines TM v 1.2012,
Rectal cancer.
Available at  www.nccn.org
www.nccn.org
Brown G,
Daniels IR,
Richardson C et al.
Techniques and trouble-shooting in high spatial resolution thin slice MRI for rectal cancer.
Br J Radiol.
2005 Mar;78(927):245-51.
Kim SH,
Lee JM,
Lee MW,
Kim GH,
Han JK,
Choi BI.
Sonography transmission gel as endo-rectal contrast agent for tumor visualization in rectal cancer.
AJR Am J Roentgenol 2008;191(1): 186вҖ“189.
Brown G,
Kirkham A,
Williams GT et al.
High-resolution MRI of the anatomy important in total mesorectal excision of the rectum.
AJR Am J Roentgenol.
2004 Feb;182(2):431-9.
Taylor FG,
Swift RI,
Blomqvist L,
Brown G.
A systematic approach to the interpretation of preoperative staging MRI for rectal cancer.
AJR Am J Roentgenol 2008;191(6):1827вҖ“1835.
Barbaro B,
Fiorucci C,
Tebala C,
et al.
Locally advanced rectal cancer: MR imaging in prediction of response after preoperative chemotherapy and radiation therapy.
Radiology 2009;250(3): 730вҖ“739.
Allen SD,
Padhani AR,
Dzik-Jurasz AS,
Glynne-Jones R.
Rectal carcinoma: MRI with histologic correlation before and after chemoradiation therapy.
AJR Am J Roentgenol 2007;188(2):442вҖ“451.
Ichikawa T,
Erturk SM,
Motosugi U,
et al.
High-B-value diffusion-weighted MRI in colorectal cancer.
AJR Am J Roentgenol 2006;187(1):181вҖ“184.
Torkzad MR,
Pahlman L,
Glimelius B.
Magnetic resonance imaging (MRI) in rectal cancer: a comprehensive review.
Insights Imaging.
2010;1:245-67.
Figueiras RG,
Goh V,
Padhani AR,
Naveira AB,
Caamano AG,
Martin CV.
The role of functional imaging in colorectal cancer.
AJR Am J Roentgenol 2010; 195: 54вҖ“66.
Rao SX,
Zeng MS,
Chen CZ,
et al.
The value of diffusion-weighted imaging in combination with T2-weighted imaging for rectal cancer detection.
Eur J Radiol 2008;65:299вҖ“303.
Dresen RC,
Beets GL,
Rutten HJ,
et al.
Locally advanced rectal cancer: MR imaging for restaging after neoadjuvant radiation therapy with concomitant chemotherapy.
I.
Are we able to predict tumor confined to the rectal wall? Radiology 2009;252(1): 71вҖ“80
Lahaye MJ,
Beets GL,
Engelen SME,
et al.
Locally advanced rectal cancer: MR imaging for restaging after neoadjuvant radiation therapy with concomitant chemotherapy.
II.
What are the criteria to predict involved lymph nodes? Radiology 2009;252(1): 81вҖ“91.
Lambregts DM,
Vandecaveye V,
Barbaro B,
et al.
Diffusion-weighted MRI for selection of complete responders after chemoradiation for locally advanced rectal cancer: a multicenter study.
Ann Surg Oncol.
doi:10.1245/s10434-011-1607-5.
Curvo-Semedo L,
Lambregts DM,
Maas M,
et al.
Rectal cancer: assessment of complete response to preoperative combined radiation therapy with chemotherapy-conventional MR volumetry versus diffusion-weighted MR imaging.
Radiology.
2011 Sep; 260(3):734-43.
Park MJ,
Kim SH,
Lee SJ et al.
Locally advanced rectal cancer: added value of diffusion-weighted MR imaging for predicting tumor clearance of the mesorectal fascia after neoadjuvant chemotherapy and radiation therapy.
Radiology.
2011 Sep;260(3):771-80.
Kim SH,
Lee JM,
Hong SH et al.
Locally advanced rectal cancer: added value of diffusion-weighted MR imaging in the evaluation of tumor response to neoadjuvant chemo- and radiation therapy.
Radiology.
2009 Oct;253(1):116-25.
Sun YS,
Zhang XP,
Tang L et al.
Locally advanced rectal carcinoma treated with preoperative chemotherapy and radiation therapy: preliminary analysis of diffusion-weighted MR imaging for early detection of tumor histopathologic downstaging.
Radiology.
2010 Jan;254(1):170-8.
Habr-Gama A,
Perez RO,
Nadalin W,
et al.
Operative versus nonoperative treatment for stage 0 distal rectal cancer following chemoradiation therapy: long-term results.
Ann Surg 2004; 240(4): 711вҖ“717; discussion 717вҖ“718.
O'Neill BD,
Brown G,
Heald RJ et al.
Non-operative treatment after neoadjuvant chemoradiotherapy for rectal cancer.
Lancet Oncol.
2007 Jul;8(7):625-33