Los tumores de hombro son muy infrecuentes,
por lo que su caracterizaciÃģn y diagnÃģstico diferencial puede suponernos un reto en nuestra prÃĄctica diaria.
Sin embargo,
estos van a presentar caracterÃsticas similares a las encontradas en los tumores musculoesquelÃĐticos de otras localizaciones,
lo cual nos ayuda a su diagnÃģstico.
Vamos a enumerar las caracterÃsticas mÃĄs representativas de los tumores Ãģseos primarios y de partes blandas mÃĄs frecuentes,
dentro de su rareza,
que nos podemos encontrar en el hombro.
TUMORES ÃSEOS
Vamos a referir el rango de edad de apariciÃģn mÃĄs frecuente de estos tumores,
pero no debemos olvidar que podemos encontrarlos en pacientes de otras edades.
1.
QUISTE ÃSEO SIMPLE.
Hasta los 20 aÃąos es mÃĄs frecuente en hombres.
A partir de esa edad no hay diferencia en cuanto al sexo.
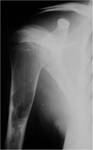
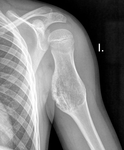
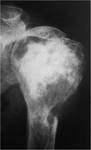
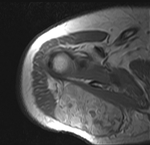
LesiÃģn osteolÃtica de bordes bien definidos,
ovalada,
expansiva que abomba y adelgaza la cortical.
Sabremos que estÃĄ activo cuando la lesiÃģn tiene su base en relaciÃģn con la fisis (FIGURA 1).
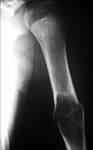
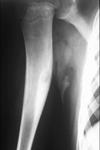
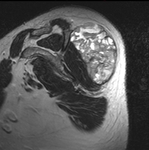
Sin embargo,
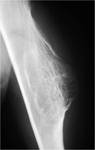
cuando estÃĄ separada de la fisis significa que es un quiste latente (FIGURA 2).
El quiste Ãģseo simple puede asociar una fractura patolÃģgica.
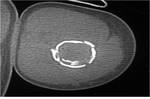
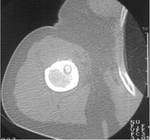
En estos casos se puede observar un fragmento Ãģseo flotando dentro de la cavidad medular,
el cual se coloca en la posiciÃģn mÃĄs declive.
Esto se conoce como el "signo del fragmento caÃdo" (FIGURA 2 Y 3).
La Resonancia MagnÃĐtica (RM) confirma el diagnÃģstico al mostrar una lesiÃģn intramedular homogÃĐnea e hiperintensa en secuencias potenciadas en T2.
2.
QUISTE ÃSEO ANEURISMÃTICO.
Edad: 5-20 aÃąos.
Hombre (H) - Mujer (M)= 1:1.
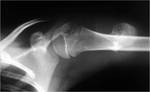
Son grandes cavidades llenas de contenido hemÃĄtico.
Pueden ser primarios o secundarios.
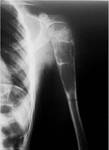
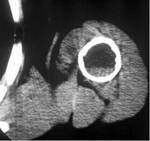
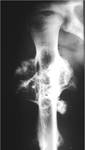
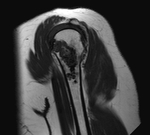
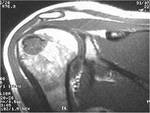
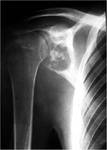
Se trata de una lesiÃģn lÃtica de carÃĄcter geogrÃĄfico o permeativo que se expande o destruye la cortical y que puede acompaÃąarse de masa de partes blandas (FIGURA 4).
Puede presentar dos fases.
En la primera va a tener un crecimiento rÃĄpido con caracterÃsticas radiolÃģgicas de agresividad; mientras que en la segunda fase sufre una encapsulaciÃģn progresiva y osificaciÃģn.
El hallazgo caracterÃstico son los niveles lÃquido-lÃquido intralesionales (FIGURA 5).
En ocasiones el diagnÃģstico diferencial entre quiste Ãģseo simple y quiste Ãģseo aneurismÃĄtico puede ser difÃcil.
3.
GRANULOMA EOSINÃFILO.
Edad: 5-10 aÃąos.
H:M = 4:3.
LesiÃģn osteolÃtica,
expansiva,
que provoca adelgazamiento o erosiÃģn de la cortical y reacciÃģn periÃģstica.
En ocasiones es necesario realizar el diagnÃģstico diferencial con las metÃĄstasis debido a que los bordes no son totalmente lisos y no hay un borde con anillo esclerÃģtico.
4.
DISPLASIA FIBROSA.
MonostÃģtica: 15-50 aÃąos.
H=M.
PoliostÃģtica: 2-30 aÃąos.
H<M.
LesiÃģn no neoplÃĄsica en la que la cavidad medular es reemplazada por material fibroso,
tejido Ãģseo y cÃĐlulas fusiformes (FIGURA 6). La transformaciÃģn maligna es rara.
Es una lesiÃģn medular expansiva radiolÚcida.
El grado de radiotransparencia depende de la cantidad de osteoide,
pudiendo ser o bien lesiones lÃticas o esclerÃģticas.
Este Último se conoce como apariencia en vidrio esmerilado.
Las lesiones lÃticas a menudo tienen bordes esclerÃģticos.
Debido al hecho de que es una lesiÃģn expansiva,
causa abombamiento y reducciÃģn de la cortical.
Es muy importante tener en cuenta que la displasia fibrosa puede fingir una gran cantidad de lesiones Ãģseas.
5.
OSTEOCONDROMA.
Edad: 10-35 aÃąos.
H:M = 2:1.
Es una proliferaciÃģn Ãģsea cubierta por cartÃlago hialino.
Pueden ser sÃĐsiles o pediculados.
Los sÃĐsiles tienen una base de implantaciÃģn ancha (FIGURA 7); mientras que los pediculados presentan un tallo fino de uniÃģn al hueso (FIGURA 8).
Lo hallazgo mÃĄs caracterÃstico es la continuidad de la cortical y la cavidad medular entre la lesiÃģn y el hueso de origen.
El cartÃlago hialino puede calcificarse con morfologÃa de arcos y anillos (FIGURA 8).
La RM es la tÃĐcnica de elecciÃģn para valorar el recubrimiento condral.
La transformaciÃģn maligna ocurre en menos del 1% de los casos.
Debemos sospecharlo cuando el casquete condral tiene un grosor mayor a 1'5 cm,
si vemos irregularidad o destrucciÃģn del contorno Ãģseo,
o crecimiento de la lesiÃģn.
En la FIGURA 9 vemos un osteocondroma de la escÃĄpula con mineralizaciÃģn en arcos y anillos en la porciÃģn mÃĄs perifÃĐrica y medial.
Rodeando dicha mineralizaciÃģn hay una masa de tejidos blandos.
Estamos,
por tanto,
ante un condrosarcoma secundario a un osteocondroma.
En la FIGURA 10 presentamos una imagen de anatomÃa patolÃģgica.
En la FIGURA 11 tenemos un ejemplo de exostosis hereditaria mÚltiple.
En estos casos existe mayor riesgo de transformaciÃģn maligna.
6.
ENCONDROMA.
Edad: 15-40 aÃąos.
H=M.
LesiÃģn lÃtica endomedular de aspecto polilobulado con calcificaciones condrales en su matriz.
FIGURAS 12 y 13.
La mineralizaciÃģn del tejido cartilaginoso muestra la tÃpica forma de arcos y anillos.
No produce destrucciÃģn cortical,
reacciÃģn periÃģstica ni masa de partes blandas.
En ausencia de fractura,
un encondroma doloroso debe ser considerado maligno hasta que se demuestre lo contrario,
pues puede ser indistinguible de un condrosarcoma de bajo grado.
7.
CONDROBLASTOMA.
Edad: 5-25 aÃąos.
H>M.
Tumor de tejido cartilaginoso,
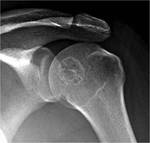
siendo normalmente lesiones osteolÃticas redondeadas u ovaladas.
La mayorÃa miden 2-3 cm de diÃĄmetro.
En la radiografÃa de la FIGURA 14 vemos una lesiÃģn bien definida con mÃĄrgenes esclerÃģticos y una matriz condroide con las tÃpicas calcificaciones en arcos y anillos.
Cuando veamos una lesiÃģn con estas caracterÃsticas en la epÃfisis o en el trocÃĄnter del hÚmero,
tenemos que sospechar en primer lugar que se trate de un condroblastoma.
La FIGURA 15 corresponde a una TomografÃa Computarizada de este mismo paciente.
En la RM de la FIGURA 16 observamos una lesiÃģn de borde esclerÃģtico hipointenso en T1.
Presenta edema rodeando la lesiÃģn,
que tambiÃĐn lo vamos a ver hipointenso en T1.
El cartÃlago hialino lo vemos con una intensidad de seÃąal intermedia.
Dentro del cartÃlago hay ÃĄreas hipointensas en arcos y anillos que se corresponden con la mineralizaciÃģn condroide.
8.
CONDROSARCOMA.
Edad: 30-60 aÃąos.
H=M.
La mayorÃa de ellos son centrales,
es decir,
se originan en la cavidad medular.
Suelen tener un crecimiento lento y un bajo potencial metastÃĄsico.
En los huesos largos vemos una lesiÃģn osteolÃtica con bordes bien definidos.
Debido a su lento crecimiento,
van a producir expansiÃģn con adelgazamiento de la cortical.
Las calcificaciones "en palomita de maÃz" son caracterÃsticas de estas lesiones.
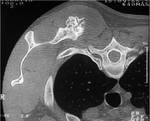
En los huesos planos,
generalmente la escÃĄpula,
predomina el componente tumoral extraÃģseo con las calcificaciones condrales tÃpicas en su interior.
FIGURA 17. Imagen con las caracterÃsticas tÃpicas que lo definen,
es decir,
mineralizaciÃģn de la matriz condroide,
destrucciÃģn Ãģsea,
reacciÃģn periÃģstica y pequeÃąas lesiones lÃticas correspondientes a un patrÃģn permeativo,
el cual es propio de las lesiones malignas.
En la RM tras la inyecciÃģn de contraste se observa una captaciÃģn caracterÃstica en anillos y arcos alrededor de los lÃģbulos tumorales y los tabiques que los separan.
9.
OSTEOMA OSTEOIDE.
Edad: 10-35 aÃąos.
H:M = 2:1.
LesiÃģn lÃtica de 1-2cm llamada nidus rodeada por una zona de esclerosis de mayor tamaÃąo que el tumor (FIGURA 18).
La mayorÃa de ellos son intracorticales,
localizados en la metÃĄfisis o diÃĄfisis de huesos largos.
El nidus con frecuencia presenta una calcificaciÃģn central muy caracterÃstica,
como podemos ver en la FIGURA 19.
10.
OSTEOBLASTOMA.
Edad: 10-35 aÃąos.
H:M = 2:1.
LesiÃģn lÃtica de contornos bien definidos mayor de 2cm.
que puede causar adelgazamiento y expansiÃģn de la cortical,
pero rara vez afecta a partes blandas.
Son frecuentes las calcificaciones de la matriz tumoral.
Presenta las mismas caracterÃsticas que el osteoma osteoide,
pero con un nidus mayor de 2cm.
En la FIGURA 20 podemos ver una radiografÃa de un osteoblastoma de la escÃĄpula.
11.
OSTEOSARCOMA.
Existen varios esquemas de clasificaciÃģn.
SegÚn el desarrollo pueden ser primarios o secundarios; por ubicaciÃģn pueden ser superficial,
intramedular o extraesquelÃĐtico; por matriz puede ser osteoblÃĄstico,
condroblÃĄstico o fibroblÃĄstico; por la diferenciaciÃģn pueden ser de bajo,
moderado o alto grado; y por las caracterÃsticas especÃficas.
El osteosarcoma central o intramedular supone el 75%.
Edad: 10-20 aÃąos.
H=M.
Suele ser mayor de 6cm.
Es una lesiÃģn agresiva,
destructiva y de lÃmites mal definidos.
Presenta ÃĄreas lÃticas y ÃĄreas esclerosas,
rara vez tienen un patrÃģn puro.
Provoca una interrupciÃģn de la cortical con afectaciÃģn de las partes blandas adyacentes.
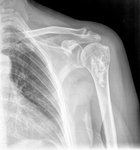
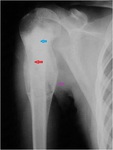
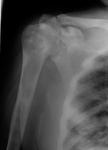
En la FIGURA 21 tenemos una radiografÃa de un osteosarcoma del extremo proximal del hÚmero.
La flecha azul corresponde a matriz osteoide mineralizada como nubes dentro de la cavidad medular.
La flecha roja seÃąala la destrucciÃģn osteolÃtica,
y la flecha lila la reacciÃģn periÃģstica laminar.
En los extremos vemos los triÃĄngulos de Codman,
correspondientes al levantamiento del periostio.
La RM permite establecer con precisiÃģn los lÃmites del tumor.
AdemÃĄs,
facilita la detecciÃģn de focos tumorales intraÃģseos separados del tumor primario por hueso normal,
muy caracterÃstico del osteosarcoma.
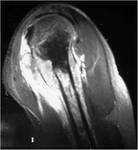
La FIGURA 22 corresponde a una RM de este mismo paciente,
donde vemos que el tumor estÃĄ invadiendo los tejidos adyacentes.
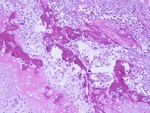
En la FIGURA 23 presentamos una imagen de anatomÃa patolÃģgica.
Dentro de los osteosarcomas perifÃĐricos,
el mÃĄs frecuente es el osteosarcoma paraostal. Edad: 25-40 aÃąos. H<M.
Es menos agresivo que el convencional.
Usualmente se presenta como una masa yuxtacortical polilobulada y densamente osificada.
Puede verse unida a la cortical o separada por una fina lÃnea radiolucente,
muy caracterÃstica del tumor.
12.
SARCOMA DE EWING.
Edad: 5-25 aÃąos. H>M.
LesiÃģn parecida al osteosarcoma,
aunque la vemos tÃpicamente en niÃąos.
Su caracterÃstica radiolÃģgica es la apariciÃģn de una masa de partes blandas,
a menudo de gran tamaÃąo,
asociada a destrucciÃģn del hueso en el que se origina.
Vamos a poder ver osteolisis y producciÃģn de hueso endÃģstico dando lugar a una reducciÃģn de la luz medular,
lo cual es muy caracterÃstico de esta lesiÃģn.
TambiÃĐn veremos reacciÃģn periÃģstica,
usualmente espiculada o multilaminar (en capas de cebolla),
que podemos reconocer por los triÃĄngulos de Codman y espÃculas paralelas o divergente.
Y sobre todo el aumento de tejidos blandos.
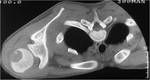
En la FIGURA 24 podemos ver las caracterÃsticas previamente descritas.
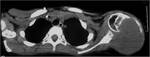
La FIGURA 25 corresponde a un corte axial de TomografÃa Computarizada (TC) en el que vemos una gran masa de partes blandas asociada a destrucciÃģn del extremo proximal del hÚmero.
13.
TUMOR DE CÃLULAS GIGANTES
Edad: 20-40 aÃąos. H:M = 1:2.
Suele ser una lesiÃģn solitaria y benigna.
Sin embargo,
en un 5-10% serÃĄn malignos.
LesiÃģn osteolÃtica excÃĐntrica,
generalmente en la epÃfisis de los huesos largos.
Presenta un patrÃģn geogrÃĄfico con mÃĄrgenes bien delimitados.
Casi siempre provoca expansiÃģn Ãģsea y adelgazamiento de la cortical,
pudiendo observarse en algunos casos interrupciÃģn de la misma con afectaciÃģn de partes blandas.
En las imÃĄgenes de RM podemos ver un realce difuso.
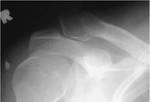
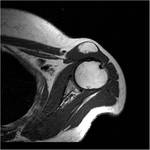
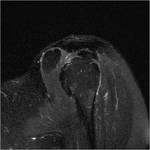
En la FIGURA 26 se presenta una lesiÃģn osteolÃtica de borde esclerÃģtico en el extremo lateral de la clavÃcula,
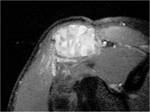
siendo la FIGURA 27 la RM correspondiente a este pacidente.
Son caracterÃsticos los niveles lÃquido-lÃquido,
que podemos ver mejor en la RM.
14.
LINFOMA ÃSEO PRIMARIO.
Edad: 45-75 aÃąos. H:M = 3:2.
Es una lesiÃģn muy rara,
siendo normalmente del tipo No Hodgkin.
La mayorÃa de los linfomas Ãģseos son secundarios.
Suele presentarse como una lesiÃģn lÃtica permeativa con apariencia similar a otros tumores de cÃĐlulas pequeÃąas y redondas,
como por ejemplo el sarcoma de Ewing.
En la FIGURA 28 observamos una lesiÃģn osteolÃtica intramedular con patrÃģn permeativo y reacciÃģn periÃģstica asociada con triÃĄngulo de Codman.
15.
METÃSTASIS.
Edad: >45 aÃąos.
Son el tumor Ãģseo mÃĄs comÚn,
y mucho mÃĄs frecuentes que las lesiones primarias.
El hueso es la tercera localizaciÃģn en frecuencia de las metÃĄstasis.
En niÃąos el origen mÃĄs frecuente es el neuroblastoma seguido del rabdomiosarcoma.
En adultos la mayorÃa son metÃĄstasis de carcinomas de pulmÃģn,
prÃģstata,
mama y riÃąÃģn.
El aspecto radiolÃģgico es variable:
- MetÃĄstasis blÃĄsticas: como las causadas por el carcinoma de prÃģstata.
Se presentan como nÃģdulos esclerÃģticos de mayor densidad que el hueso sano.
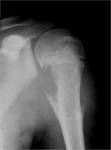
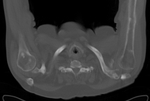
En la radiografÃa de la FIGURA 29 y en el TC de la FIGURA 30 vemos metÃĄstasis blÃĄsticas en la cabeza del hÚmero y escÃĄpula respectivamente,
secundarias a carcinoma de prÃģstata.
- MetÃĄstasis osteolÃticas: vamos a ver ÃĄreas radiolÚcidas con densidad menor a la del hueso adyacente.
Rompen la cortical e invaden las partes blandas con facilidad,
lo cual no se suele observar en las metÃĄstasis osteoblÃĄsticas.
- MetÃĄstasis mixtas: es el patrÃģn radiolÃģgico mÃĄs comÚn.
En la RM,
las metÃĄstasis Ãģseas suelen aparecer como lesiones que sustituyen la seÃąal normal de la mÃĐdula Ãģsea.
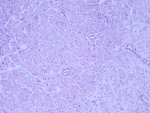
En la FIGURA 31 presentamos una imagen de anatomÃa patolÃģgica correspondiente a una metÃĄstasis.
TUMORES DE PARTES BLANDAS
Desde un punto de visto histolÃģgico los tumores de los tejidos blandos se clasifican segÚn la semejanza que tengan con los tejidos de origen.
Si un tumor estÃĄ pobremente diferenciado puede resultar muy Útil la inmuno-histoquÃmica y los anÃĄlisis genÃĐticos.
SegÚn la OMS,
por tejido blando entendemos el mÚsculoesquelÃĐtico,
la grasa,
el tejido fibroso,
el sistema nervioso perifÃĐrico y las estructuras vasculares que lo riegan.
Los tumores benignos mÃĄs frecuentes son,
por orden decreciente: Lipoma y variantes,
histiocitoma fibroso,
fascitis nodular,
hemangioma,
fibromatosis,
neurofibroma y schwanoma.
Estos representan tres cuartas partes de los tumores benignos.
Entre los malignos los mÃĄs frecuentes son por orden decreciente: histiocitoma fibroso maligno,
dermatofibrosarcoma protuberans,
liposarcoma, leiomiosarcoma y schwanoma maligno.
Ãstos representan el 80% de los tumores de partes blandas.
TUMORES BENIGNOS MÃS FRECUENTES EN EL HOMBRO:
1.
LIPOMA.
Es la tumoraciÃģn mÃĄs frecuente y estÃĄ infradiagnosticado.
- EcografÃa: masa elÃptica,
paralela a la superficie de la piel.
Lo mÃĄs frecuente es que sean hiperecogÃĐnicos,
seguido de hipoecogÃĐnicos.
Lo menos frecuente es que sean isoecogÃĐnicos.
No muestran aumento por la transmisiÃģn y se comprimen con la presiÃģn moderada del transductor.
- TC: muestran una baja atenuaciÃģn de forma difusa (entre -65 y -120 UH),
sin realce tras la administraciÃģn de contraste intravenoso.
Si presentan cÃĄpsula,
ÃĐsta tiene una atenuaciÃģn similar a la del mÚsculo.
- RM: tienen una intensidad de seÃąal idÃĐntica a la grasa en todas las secuencias.
No presentan realce postcontraste.
FIGURAS 32 Y 33.
2.
HISTIOCITOMA FIBROSO.
Edad: 15-60 aÃąos. H=M.
ClÃnicamente se manifiesta como una masa indolora, bien circunscrita.
Su tratamiento es la resecciÃģn quirÚrgica.
Como la mayorÃa son superficiales y se diagnostican clÃnicamente,
hay pocas series descritas.
Son inespecÃficos en TC y RM,
presentando una atenuaciÃģn e intensidad de seÃąal similar al mÚsculo.
3.
FASCITIS NODULAR.
Se da en adultos jÃģvenes.
Presenta un crecimiento rÃĄpido.
Hay tres tipos,
por orden decreciente:
- SubcutÃĄnea.
Es la mÃĄs frecuente y aparece como un nÃģdulo subcutÃĄneo.
- AponeurÃģtica.
- Muscular.
Dado a su mayor tamaÃąo y su localizaciÃģn profunda sugiere malignidad hasta que es diagnosticada correctamente.
Existe una escasa descripciÃģn radiolÃģgica de sus caracterÃsticas:
- TC: masa bien o mal definida.
Puede ser isodensa o hipodensa respecto al mÚsculo.
Casi nunca calcifica.
- RM: en T1 es iso o levemente hiperintenso.
En T2 se ve hiperintensa respecto a la grasa,
aunque a veces es isodensa.
Tras la administraciÃģn de contraste intravenoso la mayorÃa presentan un realce difuso,
sin embargo un 25% de estas lesiones muestra un realce perifÃĐrico.
Expresan el anticuerpo actina mÚsculo liso especÃfico (HHF35).
4.
HEMANGIOMA.
Pueden ser superficiales o profundos.
Afectan mÃĄs a las mujeres que a los hombres.
Pueden clasificarse en capilares,
cavernosos,
arterio-venosos y venosos.
En RM su imagen caracterÃstica son canales y espacios vasculares sinuosos asà como un crecimiento graso excesivo con intensidad de seÃąal alta.
Esto se observa en el 90-95% de los casos.
5.
FIBROMATOSIS.
Masa de tejido blando de lento crecimiento.
Tiene una apariencia muy variable en RM.
Un signo muy tÃpico es la cola aponeurÃģtica,
que es la extensiÃģn del tumor a travÃĐs de la aponeurosis.
Muestra un realce moderado de contraste tanto en TC como en RM.
Generalmente tiene unos bordes bien definidos.
6.
NEUROFIBROMA y SCHWANOMA.
Suponen el 10% de los tumores de partes blandas benignos.
Se engloban dentro del grupo de tumores de la vaina nerviosa.
- Schwanoma o neurilemoma: dado que se localizan en la periferia del nervio,
pueden ser extirpados quirÚrgicamente con preservaciÃģn de la funciÃģn nerviosa.
- Neurofibroma: lo mÃĄs frecuente es que sean lesiones aisladas,
no asociadas a neurofibromatosis tipo I.
Los neurofibromas plexiformes son patognomÃģnicos de la neufofibromatosis tipo I.
Dado que estos tumores infiltran el nervio,
la funciÃģn nerviosa se pierde si se extirpan quirÚrgicamente.
- RM: Sirve para diferenciar el schwanoma del neurofibroma.
- Signo diana: Casi patognomÃģnico del neurofibroma.
Se observa una intensidad de seÃąal baja en la parte central con un reborde perifÃĐrico hiperintenso en imÃĄgenes potenciadas en T2.
- Signo fascicular: estructuras mÚltiples pequeÃąas con forma de anillo en imÃĄgenes potenciadas en T2,
que representan los haces fasciculares.
- Tienen los bordes bien definidos,
y suelen realzar tras la administraciÃģn de contraste.
- Signo de desplazamiento de la grasa vecina.
Debido a que el nervio estÃĄ rodeado de grasa,
la masa al crecer mantiene este borde de grasa.
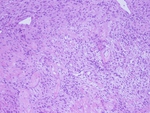
En la FIGURA 34 tenemos una imagen de anatomÃa patolÃģgica de un neurofibroma,
y en la FIGURA 35 de un schwanoma.
TUMORES MALIGNOS MÃS FRECUENTES EN EL HOMBRO:
1.
HISTIOCITOMA FIBROSO MALIGNO.
Edad: 20-60 aÃąos. La frecuencia es similar en mujeres y hombres.
Se trata de un sarcoma pleomÃģrfico.
Es el tumor de partes blandas mÃĄs frecuente de la edad adulta,
suponiendo el 20-30% de todos los sarcomas.
- TC: Masa de partes blandas lobulada y grande,
con atenuaciÃģn similar a la del mÚsculo.
Tiene zonas hipoatenuantes en el interior que corresponden a necrosis.
Realza tras la administraciÃģn de contraste,
fundamentalmente los bordes.
- RM: masa intramuscular con intensidad de seÃąal intermedia en T1 e intermedia-alta en T2.
Presenta un patrÃģn heterogÃĐneo en todas las secuencias.
La RM permite detectar la posible destrucciÃģn del hueso cortical adyacente y la invasiÃģn del canal medular.
Tiene los bordes bien definidos debido a una pseudocÃĄpsula.
Con frecuencia tiene componente hemorrÃĄgico,
pudiendo simular un hematoma.
Son tumores con aspecto y celularidad heterogÃĐnea,
y son un diagnÃģstico de exclusiÃģn.
Tienen en comÚn un marcado pleomorfismo nuclear y citolÃģgico.
2.
LIPOSARCOMA.
Segundo tumor de partes blandas mÃĄs frecuente.
Normalmente se presenta como una masa indolora,
pero a veces puede ser dolorosa per se o con la palpaciÃģn.
Su apariencia en las pruebas de imagen depende del grado de diferenciaciÃģn.
Cuanta mÃĄs grasa haya en ÃĐl,
mÃĄs se parecerÃĄ al lipoma.
A veces es muy difÃcil diferenciarlo.
Se observan tabiques fibrosos de diferente grosor en su interior que realzan tras la administraciÃģn de contraste.
Tabiques gruesos orientan a malignidad.
Pueden tener una apariencia heterogÃĐnea debido a la presencia de nÃģdulos,
hemorragia y/o necrosis.
En ocasiones se presenta como una masa inespecÃfica con atenuaciÃģn similar al mÚsculo.
El liposarcoma se da en personas de mayor edad y suele ser mÃĄs grande que el lipoma.
3.
DERMATOFIBROSARCOMA PROTUBERANS.
Constituye el 6% de todos los sarcomas de partes blandas.
- TC: lesiÃģn nodular o lobular con atenuaciÃģn similar al mÚsculo.
Tiene bordes bien definidos.
- RM: seÃąal inespecÃfica.
En T1 es similar al mÚsculo,
siendo hiperintensa en T2 y STIR.
Suele presentar zonas de hemorragia y necrosis en su interior.
Se pueden encontrar extensiones lineales a lo largo de la superficie cutÃĄnea en secuencias con TR largo.
Podemos observar nÃģdulos satÃĐlites en el tejido subcutÃĄneo adyacente.
4.
LEIOMIOSARCOMA.
Tercer tumor maligno de partes blandas mÃĄs frecuente.
- TC: masa de partes blandas inespecÃfica.
Si son grandes pueden presentar ÃĄreas hipoatenuantes que corresponden a necrosis y/o hemorragia.
Si asociamos este hallazgo con metÃĄstasis hepÃĄticas es altamente sugestivo de leiomiosarcoma.
- RM: inespecÃfica.
Presenta un realce muy marcado al administrar gadolinio.
5.
TUMORES MALIGNOS DE LA VAINA NERVIOSA.
Entre ellos estÃĄ el Schwanoma maligno.
Suponen el 5-10% de todos los tumores de tejidos blandos.
Asociado a la neurofibromatosis tipo I en el 50-60% de los casos.
Tienen un aspecto fusiforme.
- RM: masa de tejidos blandos circunscrita o infiltrante,
frecuentemente hemorrÃĄgica se observa nervio que entra y que sale.
Por lo general tiene un gran tamaÃąo,
midiendo mÃĄs de 5 cm,
con mÃĄrgenes mal definidos.
La lesiÃģn es isointensa al mÚsculo en las imÃĄgenes potenciadas en T1,
heterogÃĐneamente hiperintensa en imÃĄgenes ponderadas en T2 (secundario a ÃĄreas de hemorragia,
degeneraciÃģn quÃstica y calcificaciÃģn) y muestra un marcado realce tras la administraciÃģn de contraste.
Asocia infiltraciÃģn de los tejidos blandos adyacentes.
No es frecuente el signo de la diana,
el signo fascicular ni la homogeneidad observados en las formas benignas.
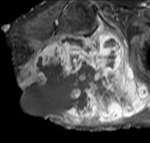
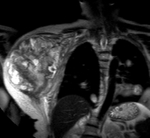
En las FIGURAS 36 y 37 presentamos imÃĄgenes de un neurofibrosarcoma,
y en las FIGURAS 38 y 39 de un PNET (tumor neuroectodÃĐrmico primitivo).