1.
Manejo diagnóstico
El diagnóstico de cáncer de mama durante la gestación resulta más complicado debido a los cambios fisiológicos que ocurren en la mama durante este periodo.
La ecografía es la técnica de imagen de elección para evaluar las alteraciones mamarias durante el embarazo y la lactancia y por tanto,
también en el diagnóstico del cáncer de mama asociado a la gestación,
ya que no emplea radiación ionizante y tiene una alta sensibilidad (100%).
Permite la diferenciación entre masa y tejido normal y la caracterización de la misma en el primer caso (características benignas o malignas).
No obstante,
los cambios fisiológicos también pueden alterar la apariencia del cáncer de mama y han sido descritas en algunos casos características ecográficas que se asocian normalmente a benignidad (orientación paralela,
realce posterior...) Las neoplasias agresivas pueden alterar el aporte vascular conduciendo a necrosis o degeneración quística.
Por ello la biopsia de cualquier lesión que no tenga criterios de quiste simple está recomendada.
La ecografía también es útil en la detección de adenopatías axilares y en la monitorización de la respuesta a quimioterapia neoadyuvante.
En nuestra revisión,
se realizó ecografía como prueba inicial en todos los casos (11).
En 7 pacientes la forma de presentación fué como nódulo-masa de entre 2'5-5cm mal delimitado,
hipoecoico,
de bordes espiculados con orientación perpendicular al plano de la piel y ocasionalmente mala transmisión acústica.
En algunos de estos 7 casos presentó orientación paralela a la piel,
no obstante el resto de características fueron altamente sugestivas de malignidad.
En 1 paciente se halló un nódulo de 2'5cm sólido de ecogenicidad heterogénea,
contorno microlobulado.
En otras 2 pacientes se presentó como masa mixta,
con componente sólido y quístico,
relativamente bien delimitada y con eje paralelo a la piel,
con polo sólido de ecogenicidad heterogénea.
Por último en 1 paciente se observó alteración de la ecogenicidad difusa y mala delimitación por planos,
con múltiples nódulos.

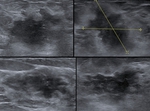
Fig. 1: Nódulos de 4 diferentes pacientes. Presentan contorno mal delimitado, espiculado, alteración de la ecogenicidad del tejido fibroglandular adyacente, alguno de ellos cono orientación perpendicular al plano de la piel y uno de ellos con calcificaciones.

Fig. 2: En 1 paciente nódulo sólido de ecogenicidad heterogénea, paralelo a la piel, contorno microlobulado.

Fig. 3: Nódulos mixtos en 2 pacientes con componente sólido-quístico.

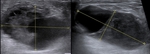
Fig. 4: Alteración difusa de la ecogenicidad con múltiples nódulos. En las imágenes de la derecha se observa imagen nodular (marcada con cruces).
En resumen aunque en algunas ocasiones presentaron alguna característica de benignidad,
en su conjunto el resto de hallazgos fueron sugestivos de malignidad y se clasificaron en las categorías de BI-RADS4b a BI-RADS 5.
Los cambios fisiológicos en la mama se traducen en la mamografía con variaciones en la densidad fibroglandular que adopta un aspecto denso,
confluente,
con disminución del tejido graso,
por lo que la sensibilidad de la técnica se encuentra reducida.
La realización de mamografía está indicada en pacientes con alteración clínica como apoyo a la ecografía ya que permite identificar calcificaciones y podría colaborar en la detección de bilateralidad o multicentricidad.
La realización de mamografía con la técnica habitual en dos proyecciones es posible durante el embarazo,
con pocos riesgos para el feto,
empleando protección abdominal.
La radiación recibida por el feto sería teóricamente de 0'004Gy.
A pesar de ello las recomendaciones generales aconsejan evitar la mamografía durante el primer trimestre,
que abarca el periodo de organogénesis cuando el feto es más susceptible.
Durante la lactancia su realización se aconseja inmediatamente después de vaciar el pecho para disminuir la densidad mamaria,
aún así su utilidad es limitada.
Los hallazgos sospechosos de malignidad son los mismos que en las pacientes no gestantes incluyendo masa/nódulo,
microcalcificaciones,
asimetría en la densidad,
alteración de la estructura y engrosamiento de la piel o retracción del pezón.
La mamografía se realizó en 7 de nuestros 11 casos,
en 2 no consta la realización por ser casos antiguos y en los 2 restantes no se realizó debido a diagnóstico durante el 1º trimestre.
En 4 de ellas únicamente se observó una asimetría de densidad mamaria,
a veces muy sutil,
en otras nodular,
en 1 se observó masa con características sugestivas de benignidad y en 1 aumento de la densidad,
refuerzo trabecular,
masa y engrosamiento de la piel.

Fig. 5: Carcinoma retroareolar mama izquierda. Únicamente se identifica mínima asimetría en la densidad fibroglandular.

Fig. 6: Asimetría nodular en cuadrantes sueriores de mama derecha de contorno mal delimitado. Corresponde a un carcinoma en CSE de mama derecha.

Fig. 7: En CSE de mama izquierda masa con características sugestivas de benignidad, de contorno bien circunscrito, ovalada, con calcificación gorsera en su interior, que correspondió a carcinoma.

Fig. 8: Alteración de la densidad de LIC inferior de mama derecha que se extiende parcialmente a todos los cuadrantes, con masa de contorno circunscrito y engrosamiento cutáneo.
En líneas generales la ecografía resultó más sensible y específica para el diagnóstico y extensión de lesiones ya que los cambios fisiológicos disminuyeron la sensibilidad de la mamografía en algunas pacientes.
El uso de la RM durante la gestación no está aceptado en líneas generales.
No está completamente establecida la seguridad del uso de contraste y ciertos estudios han demostrado su paso a través de la placenta y entrada en la circulación fetal.
En el momento no se dispone de suficientes datos sobre su posible repercusión.
Técnicamente también presenta dificultades ya que la exploración se realiza en decúbito prono.
La ACR únicamente acepta el uso de la RM en gestantes en aquellas situaciones donde el riesgo-beneficio es claro y señala específicamente que los agentes de contraste no se deben emplear en este grupo.
La ESR afirma que el uso de contraste es probablemente seguro ya que la cantidad que se espera que cruce la barrera placentaria es poca y sería rápidamente eliminada por los riñones.
Hasta el momento,
no obstante,
el uso de la ecografía y la mamografía resulta suficiente para el diagnóstico de cáncer de mama durante la gestación.
Su empleo durante la lactancia se puede realizar de forma segura,
inmediatamente tras vaciar el pecho y dejando pasar 24 horas para la siguiente toma ya que una mínima cantidad de contraste se puede excretar por la leche,
por lo que se desecha.
El parénquima fibroglandular durante la lactancia presenta un realce rápido que puede interferir en la detección generando falsos positivos,
aunque generalmente los nódulos malignos presentan mayor y más rápido grado de realce que el tejido adyacente.
La RM tendría más utilidad en la valoración de la extensión y la multicentricidad que en el diagnóstico.
En nuestras pacientes únicamente se empleó RM en 3 casos.
En todas se realizó para evaluar respuesta a quimioterapia neoadyuvante antes y despues de la misma.
En 2 de ellas tras IVE en el 1º trimestre y en 1 tras cesárea en la semana 35 de una neoplasia detectada en la semana 32.

Fig. 9: RM en una paciente tras IVE en la semana 5. Nódulo en mama izquierda de contorno microlobulado, con realce intenso precoz y posterior lavado, de alta sospecha de malignidad.
Para establecer el diagnóstico definitivo se requiere confirmación histológica.
Al igual que en las no gestantes,
la mestra para estudio anatomopatológico se puede obtener de forma segura por biopsia con aguja gruesa guiada por ecografía con anestesia local.
Aunque se ha descrito el riesgo de fístula láctea,
su incidencia es mínima y no ocurrió en ninguno de los casos estudiados.

Fig. 10: BAG guiada con ecografía. Se observa la aguja en el margen izquierdo de la imagen antes y después de efectuar el disparo, comprobando la presencia de la misma en el interior de la lesión en la segunda imagen.
En cuanto a la estadificación,
durante la gestación se deben evitar los métodos que empleen radiación ionizante,
postponiéndolos si son necesarios,
a la terminación de la gestación.
Durante el embarazo se puede emplear de forma segura la Rx Tórax con protección abdominal,
ecografía hepática y RM sin contraste de cuerpo enterpo para evaluar columna,
en el caso de que se sospeche afectación ósea secundaria.
En 3 pacientes se observaron metástasis.
En 2 de ellas hepáticas,
al diagnóstico y en 1 pleurales y óseas durante el curso de la enfermedad.
El diagnóstico de las metástasis hepáticas se identificó mediante ecografía y posteriormente TC.
El diagnóstico de metástasis pleurales y óseas se realizó mediante TC y rastreo óseo ya que se presentaron durante el curso de la enfermedad,
tras finalización de la gestación.

Fig. 11: Metástasis hepáticas en una de las pacientes. La TC se realizó tras la finalización de la gestación.
2.
Análisis descriptivo de la clínica,
estadificación,
características anatomopatológicas,
receptores y antecedentes de riesgo.
La presentación habitual es como mása o nódulo palpable no doloroso.
Los cambios fisiológicos implican un aumento de la densidad mamaria,
por lo que la palpación y por tanto la detección se ven dificultadas.
Otras presentaciones como secreción a través del pezón,
son más infrecuentes.
En cuanto a la histología,
la más frecuente es el tipo infiltrante de ningún tipo especial de alto grado (ductal NOS,
anteriormente llamado carcinoma ductal infiltrante), siendo los otros tipos menos frecuentes.
Algunos de los estudios revisados sugieren una menor proporción de receptores hormonales positivos y/o mayor proporción de Her2neu positivo,
mientras que otros no.
En general, no parece que se hayan encontrado diferencias inmunohistoquímicas ni inmunopatológicas con respecto a mujeres no gestantes para el mismo grupo de edad y parece ser que las características biológicas del tumor podrían estar más asociadas con la edad al diagnóstico que con la asociación a gestación.
Tampoco se han descrito en la literatura factores de riesgo específicos asociados al cáncer de mama gestacional,
ni genéticos ni ambientales,
ni se ha observado mayor incidencia de mutaciones tipo BRCA1 o BRCA 2 con respecto a la población no gestante de la misma edad.

Fig. 12: Resumen de la clínica, estadiaje, características anatomopatológicas, receptores y antecedentes personales de riesgo.
Nuestros datos concuerdan con los descritos.
Todas las pacientes se presentaron con clínica de masa palpable (3 y 6cm),
su histología fué de carcinoma infiltrante grado 3,
con receptores hormonales positivos en 6 pacientes (54,5%),
negativos en 5 pacientes (45.5%) y Her2-neu positivo en 2 pacientes (18%). Únicamente se hallaron factores de riesgo relevantes en 2 pacientes (18%),
una de ellas presentó BRCA1 positivo y la otra tenía antecedentes de carcinoma medular previo en ambas mamas.
En 3 pacientes se observaron metástasis al diagnóstico (en 2 de ellas hepáticas y en 1 pleurales y óseas).
La edad al diagnóstico fue de 29 a 38 años,
siendo la mayoría (70%) de edad igual o mayor a 34.
3.
Manejo terapéutico pre y postparto,
manejo de la gestación y evolución.
El manejo terapeutico en líneas generales debe ser lo más similar posible al de la población general no gestante,
adaptándose según las diferentes particularidades de cada caso (edad gestacional al diagnóstico,
estadio,
receptores,
deseos de descendencia,
etc.) y teniendo en cuenta la salud fetal.
Se debe evitar la demora en el diagnóstico y tratamiento a después del parto asi como la prematuridad.
También hay que tener en cuenta que la terminación de la gestación no parece mejorar el pronóstico materno.
Son muchas las decisiones a tener en cuenta en el tratamiento de la paciente gestante con neoplasia de mama y afectan a especialidades diferentes que deben coordinarse entre sí.
El abordaje terapéutico y el manejo de la gestación,
por tanto,
exige la colaboración interdisciplinar,
y las decisiones deben consensuarse y tomarse desde un comité multidisciplinar que comprenda diferentes especialidades (oncología médica y radioterápica,
anatomopatología,
radiología,
ginecología,
cirugía...)
En líneas generales la cirugía mamaria puede realizarse durante cualquier trimestre,
siguiendo la elección de la cirugía las mismas directrices que para no gestantes.
Tamién se puede emplear de forma segura la biopsia selectiva de ganglio centinela ya que las dosis absorbidas en abdomen en pacientes no gestantes es menor del umbral de dosis fetal (0'1Gy).
No está aprobado el uso de RT durante la gestación,
no obstante en caso de cirugía conservadora se puede administrar quimioterapia y demorar la radioterapia a después del parto.
La decisión de administrar quimioterapia también debe seguir las mismas directrices que en no gestantes y debe ser administrada después del primer trimestre,
ya que éste comprende el periodo de organogénesis.
Determinados régimenes de quimioterapia han sido aceptados con seguridad para el feto durante el segundo y tercer trimestre de gestación.
Otros tratamientos como anticuerpos monoclonales,
hormonoterapia o bifosfonatos no se pueden emplear durante la gestación ya que son nocivos para el feto,
aunque se puede demorar su administración a después del parto.
Determinados fármacos de soporte durante la quimioterapia (estimuladores de colonias de granulocitos,
determinados tipos de corticoesteroides) no son perjudiciales y se pueden emplear si son necesarios.
Convencionalmente se ha afirmado que el pronóstico es peor con respecto a la población general,
no obstante los estudios más recientes afirman que no parece existir peor pronóstico con respecto a las pacientes no gestantes para el mismo grupo de edad y estadio,
por lo que el peor pronóstico es probablemente debido a que usualmente se diagnostica en estadios más avanzados a causa de los cambios fisiológicos mamarios y/o a la no estandarización del tratamiento.
Las pacientes en nuestro estudio fueron seguidas en la unidad multidisciplinar de patología de mama de nuestro hospital.
Se trató de aplicar el tratamiento estándar ajustándose individualmente en cada caso como se detalla en la tabla a continuación (Fig. 13),
destacando que se empleó quimioterapia sin repercusión fetal durante el 3º trimestre en algunas pacientes.
Los régimenes de quimioterapia empleados durante la gestación fueron todos de adyuvancia,
en dos pacientes con esquema Antraciclinas + Ciclofosfamida,
reservando los Taxanos a después del parto por disponer de menos información acerca de su seguridad.
Otra paciente recibió quimioterapia en otro centro y según los datos que disponemos se administraron Antraciclinas + Ciclofosfamida + 5-Fluoracilo.

Fig. 13: Manejo terapéutico pre y postparto, manejo de la gestación y evolución
La evolución hasta el momento ha sido similar al de la misma edad y estadio para la población no gestante.
De las pacientes que presentaron metástasis,
dos evolucionaron con progresión a pesar del tratamiento y éxitus durante los 3 primeros años y una con respuesta completa y libre de enfermedad desde hace 10 años (metástasis hepáticas).
En cuanto a la gestación,
1 paciente se encontraba dando lactancia y 3 pacientes decidieron IVE,
de las 7 restantes únicamente en una tuvo lugar un parto pretérmino no programado en la semana 25 y en las otras 6 se programó el parto sin incidencias entre la semana 34-38. Todos los fetos fueron normales,
sin anomalías,
con peso normal para la edad gestacional.
4.
Presentación de casos
CASO 1

Fig. 14

Fig. 15

Fig. 16

Fig. 17
CASO 2

Fig. 18
CASOS 3 y 4

Fig. 19
CASO 5

Fig. 20

Fig. 21

Fig. 22