Existe una gran variedad de neoplasias intraventriculares.
Estas lesiones pueden descubrirse como un hallazgo incidental o por síntomas como dolores de cabeza secundarios al aumento de la presión intracraneal e hidrocefalia.
También pueden debutar con convulsiones o con un déficit neurológico,
como los tumores situados en el IV ventrículo que pueden producir ataxia o paresia.
Es importante entender la embriología,
la anatomía y el desarrollo histológico del sistema ventrícular (1).
Los ventrículos cerebrales comienzan como unas herniaciones saculares en extremo craneal del tubo neural,
que se llaman vesículas telencefalicas.
Los plexos coroideos se desarrollan a partir de una invaginación de la pía-aracnoides primitiva y de los vasos en estas vesículas.
El revestimiento epitelial de los ventrículos está compuesto de células ependimales,
que son el origen de los ependimomas.
Subyacente al revestimiento ependimal existe una placa subependimaria compuesta de células gliales de la surgen los subependimomas.
El septum pelúcido también está recubierto por células gliales y células precursoras neuronales residuales,
de las que se origina el neurocitoma central.
El plexo coroideo que es muy vascular y produce el líquido cefalorraquídeo (LCR) da lugar a neoplasias primarias o en ellos se pueden implantar las metástasis.
Las células aracnoideas pueden quedar atrapadas dentro de los plexos coroideos durante desarrollo embriológico y originar meningiomas intraventriculares.
El diagnóstico diferencial es complicado ya que varios tumores intraventriculares tienen una morfología similar aunque con la RM avanzada tienen unos patrones de señal bastante característicos.
Sin embargo,
pueden no ser suficientes para el diagnóstico,
y características como la localización de la lesión junto con la edad y el sexo,
pueden ayudar a reducir las posibilidades diagnósticas.
EPENDIMOMA
Representan el 3-5 % de neoplasias intracraneales (2).
Son tumores gliales que surgen de las células ependimarias de la pared ventricular y del epéndimo medular.
Pueden aparecer a cualquier edad,
pero son más comunes en jóvenes.
Los de fosa posterior son más frecuentes en niños (6 años de media),
mientras que la edad media para los supratentoriales es de 18-24 años (2).
Es el tercer tumor del SNC más común en niños,
por detrás del meduloblastoma y los astrocítomas.
En los niños la supervivencia a los 5 años es de 50-75% (3).
La cirugía es el tratamiento de elección,
pero la resección quirúrgica es a menudo difícil,
por lo que se suele dar radioterapia postoperatoria.
Si la resección es subtotal,
tiende a ser recurrente y su pronóstico es muy malo.
Son neoplasias de grado II (de bajo grado,
bien diferenciado) o grado III (anaplásico) de la clasificación de la Organización Mundial de la Salud (OMS) (4).
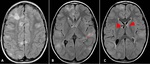
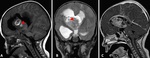
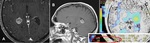
Hallazgos de imagen:
El 40% tienen una localización supratentorial y el resto surgen en la fosa posterior (5).
Los supratentoriales pueden tener una localización intraparenquimatosa no intraventricular y se cree que sea debidos a restos de tejido ependimal atrapado en el desarrollo embriológico (4).
Con frecuencia muestran un componente quístico (sobre todo los intraparenquimatosos supraventriculares y el diagnóstico diferencial incluye astrocitoma pilocítico,
pleomórfico xantoastrocitoma y ganglioglioma) y áreas de calcificación groseras.
A veces pueden tener zonas de hemorragia intratumoral.
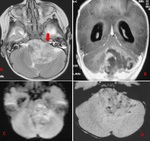
Los que implican el IV ventrículo tienden a llenar el ventrículo como un molde de yeso y pueden extenderse a través del foramen de Luschka o de Magendie o el foramen magnum.
Pueden difundir por el LCR.
TC
- hipo/isodenso.
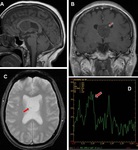
RM
- iso/hipointensa en secuencias T1.
- iso/hiperintensa en secuencias T2.
Puede haber edema vasogénico en la sustancia blanca periventricular.
- realce heterogéneo en secuencias T1 con contraste.
- focos de ausencia de señal por calcificación o hemorragia en secuencias de susceptibilidad (T2*).
- el componente quístico tiende a tener una intensidad de señal similar en T1 y en T2,
pero no puede ser completamente suprimida en FLAIR debido al alto contenido proteico.
- en difusión (dRM) la señal es variable,
dependiendo de la celularidad del tumor,
con valores del coeficiente de difusión (ADC) generalmente intermedio entre la de los astrocitomas pilocíticos y tumores neuroectodérmicos primitivos.
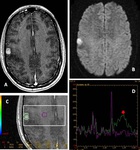
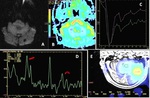
- su espectroscopia (eRM) tiene un patrón neoplásico con la reducción del pico de N-acetilaspartato (NAA) y elevado del lactato y de la colina (Cho).
En algunos casos presentan alto el pico de mioinositol (mI) y el de glicina (Gly) y un pico preservado del NAA.
Sin embargo,
la espectroscopia por si sola no los diferencia de otros tumores (6).
- la perfusión (pRM),
en general,
demuestra el volumen sanguíneo cerebral marcadamente elevado y,
a diferencia de muchos otros tumores gliales,
tienen un pobre retorno a la línea de base por la alteración de la barrera hemato-encefálica (7).
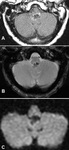
SUBEPENDIMOMA
Representan el 0,2-0,7 % de las neoplasias intracraneales ,
sin embargo,
esta cifra puede subestimada,
ya que a menudo son asintomáticos y se encuentran incidentalmente (8).
Surgen de la capa glial subependimaria que rodea los ventrículos cerebrales.
Tienen un predominio masculino (razón hombre-mujer 2,3:1),
y el 82% se producen en pacientes mayores de 15 años.
El pronóstico es bueno y la recurrencia después de la resección quirúrgica es poco frecuente (2).
Son neoplasias grado I de la OMS muy diferenciados (mezcla de tipos de células ependimarias y astrocitos que se consideran variantes del ependimoma) (4).
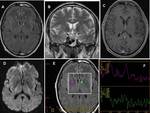
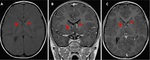
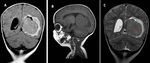
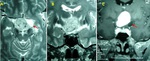
Hallazgos de imagen:
El 50-60% aparecen en el cuarto ventrículo y el resto en los ventrículos laterales y tercero.
La mayoría son de menos de 2 cm de tamaño,
pero las lesiones sintomáticas tienden a ser ≥ 4 cm.
Son lesiones bien circunscritas.
Pueden ocurrir,
como en el ependimoma,
que exista degeneración quística,
calcificación o la hemorragia intratumoral.
A diferencia de los ependimomas no suelen existir invasión extraventricular (8,9).
TC
- hipo/isodensas.
RM
- hipo/isointensas en secuencias T1.
- hiperintensa en T2 sin edema del parénquima adyacente.
- focos de ausencia de señal por calcificación o hemorragia en secuencias de susceptibilidad (T2*).
- la captación de contraste es variable,
ya que son tumores avasculares y por tanto,
la mayoría de las lesiones tienen escaso o nulo realce,
y los distingue de los tumores subependimarios de células gigantes,
que tienen una ubicación similar.
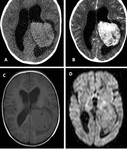
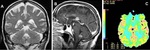
NEUROCITOMA CENTRAL
Son el 0,25-0,5 % de los tumores intracraneales y se describieron en los años 80 (10).
El origen de estos tumores no está claro,
parece que provienen de células progenitoras bipotenciales neuronales y gliales (11).
La edad media de los pacientes es de 29 años,
pero es amplia; no hay predilección de sexo.
Generalmente, se presentan con síntomas de aumento de la presión intracraneal.
La resección total es curativa,
pero pueden recurrir.
Son neoplasias grado II de la OMS,
de aspecto histológico benigno con una delicada red vascular y áreas parcheadas de neuroepitelio fibrilar (4).
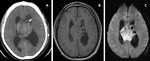
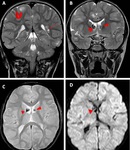
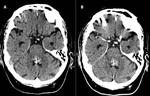
Hallazgos de imagen:
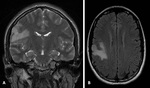
Se desarrollan en la pared del cuerpo o asta frontal del ventrículo lateral (adjunto al septum pellucidum) con o sin extensión al tercero (8,10).
Son lesiones bien definidas,
lobuladas y con frecuencia tienen áreas que parecen quistes que le dan un aspecto "burbujeante". Hasta 50% puede contener calcificación y la hemorragia es rara.
TC
- isodensa o ligeramente hiperdensa.
RM
- isointensa en secuencias T1.
- iso/hiperintensa en T2.
En la sustancia blanca periventricular adyacente puede existir edema.
- con contraste,
el patrón de realce es variable,
de moderado a intenso,
y heterogéneo.
Pueden apreciarse vacíos de flujo prominentes.
- en difusión muestran una apariencia heterogénea hiperintensa.
- la espectroscopía muestra un gran pico de Cho (↑ Cho/creatina y ↓
NAA /Cho) y un pico a 3,55 ppm que probablemente mI o Gly (6,
12).
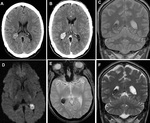
TUMOR SUBEPENDIMARIO DE CELULAS GIGANTES (TSCG)
Es el tumor cerebral más frecuente en los pacientes con esclerosis tuberosa (ET),
hasta el 16% de los casos,
y se considera patognomónico (13).
Previamente se denominaba astrocitoma subependimario de células gigantes,
pero los estudios patológicos recientes han revelado que es un tumor glioneuronal (14).
La ET es un trastorno neurocutáneo que resulta de la inactivación de mutaciones en uno de los dos genes supresores de tumores: TSC1 (cromosoma 9) o TSC2 (cromosoma 16) (15).
Hay un amplio rango de edad para la presentación,
desde el nacimiento hasta la quinta década (11 años de media) (2,13).
Se ha propuesto que surgen de un nódulo subependimario (16).
Tienen un crecimiento lento casi siempre,
un comportamiento benigno y las indicaciones para la resección son el aumento el tamaño del tumor,
la hidrocefalia o un déficit neurológico focal.
La cirugía suele ser curativa.
Se recomienda vigilancia cada 2 y 3 años para los pacientes con la mutación TSC2 y TSC1,
respectivamente; una vez se identifica un TSCG,
el seguimiento es anual (17).
Es una lesión grado I de la OMS con una histogénesis confusa con una tinción inmunohistoquímica que revela marcadores tanto para proteínas gliales y neuronales (14).
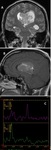
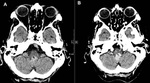
Hallazgos radiológicos:
Es una lesión bien circunscrita típicamente >1 cm y comunmente situada cerca del foramen de Monro.
Pueden coexistir otros nódulos subependimarios.
A veces presentan focos de calcificación.
Es raro que sangren.
TC
- hipo/isodensas.
RM
- hipo/isointensa en secuencia T1.
- iso/hiperintensa en secuencia T2.
- captan avidamente contraste.
- en difusión muestran valores de ADC menores que los hamartomas de los nódulos subependimarios de la ET.
- la espectroscopía puede mostrar ↑ Cho/creatina y ↓ NAA/Cr,
similares a otras neoplasias.
- la dRM y eRM pueden ser herramientas para detectar la transformación neoplásica de los nódulos subependimarios (6).
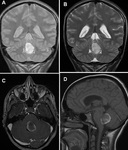
NEOPLASIAS DE LOS PLEXOS COROIDEOS
Representan entre 2-4 % de los tumores cerebrales pediátricos (20% en el primer año de vida) y el 0,5% del adulto (8).
Surgen desde el epitelio en cualquier parte del plexo coroideo.
Las lesiones del IV ventrículo son más comunes en varones (razón hombre-mujer,
3:0,2 ) y están distribuidos de manera uniforme entre todas las edades; las lesiones del ventrículo lateral no tienen predilección de género y son más comunes en los niños (80% de los casos) (4).
Tienen asociación con varios síndromes como el de Aicardi y Li - Fraumeni.
Se subdividen sobre la base de los hallazgos histológicos: papiloma del plexo coroideo (PPC) (grado I de la OMS); CPP atípico (grado II) y carcinoma del plexo coroideo (CPC) (grado III).
La proporción de PPC supera a CPC en 5:01.
La transformación es poco frecuente de un papiloma a carcinoma.
El PPC y el CPP atípico tienen una distribución de edad amplia,
por el contrario,
el CPC se encuentra casi en su totalidad en la población pediátrica, y en adultos al ser my raro es muy difícil de diferenciar histologicamente de carcinomas metastásicos.
La hidrocefalia se cree que sea por: 1) superproducción de LCR por la neoplasia; 2) disminución de la absorción del LCR por el exudado proteínico que generan y/o la hemorragia intraventraventricular a veces se produce; 3) directamente por la obstrucción del tumor.
Los carcinomas tiene un alto potencial de diseminación a lo largo del neuro-eje y hay que estudiarlo antes de la cirugía.
El pronóstico para los pacientes con PPC es bueno,
con una tasa de supervivencia a 5 años del 97 %,
pero para el CPC esta tasa se reduce al 26-43 % (18).
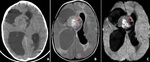
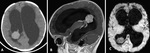
Hallazgos radiológicos:
La mitad aparecen en el ventrículo lateral (sobre todo en el atrio),
el 40% en el IV ventrículo y aproximadamente el 5 % en más de un lugar (4).
Están bien definidos,
con forma de coliflor,
pueden estar pediculados,
muy vasculares y son comunes las hemorragias y quistes.
No tienen características específicas pero el PPC y PPC atípico con frecuencia tienen aspecto lobulado; los CPC tienden a tener un más contorno irregular,
son heterogéneos por la presencia de necrosis y tienden a invadir más el parénquima cerebral adyacente que PPC.
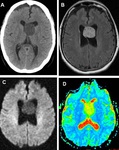
TC
- iso/hiperdensas.
- captan contraste y en Angio-TC o arteriografía puede detectarse un agrandamiento de la arteria coroidea seguido de un pedículo vascular.
RM
- iso/hipointensa en T1.
- iso/hiperintensa en T2; son comunes vacíos de flujo.
Puede aparecer edema vasógenico periventricular.
- realce intenso homogéneo debido a la alta vascularización .
- no tienen ninguna restricción de difusividad del agua en dRM.
- en pRM refleja un flujo arterial alto y una pérdida de la barrera hemato-encefálica con una persistencia de contraste.
- la eRM en los PPC muestra un pico Cho y un pico ausente de NAA.
Los CPC además muestran elevado el lactato debido al aumento de la proliferación celular y la glucólisis anaeróbica (6).
MENINGIOMAS INTRAVENTRICULARES
Representan el 0,5-3,7 % de los meningiomas intracraneales.
Se cree que surgen de las células aracnoideas atrapadas en el plexo coroideo o de la tela coroidea durante la formación embriológica de la fisura coroidea y el plexo (1,2).
La relación de mujer-varón es de 0,2:0,1 con un rango de edad entre 30-60 años.
Rara vez aparecen en los niños (menos del 3 % de las neoplasias intracraneales) pero tienen mayor riesgo a transformación sarcomatosa (19).
Están asociados a la neurofibromatosis tipo II.
La mayoría demuestran comportamiento indolente,
pero se han descrito lesiones con atípicidad o anaplásicos.
Hallazgos radiológicos:
El lugar más frecuente de aparición es en el atrio de los ventrículos laterales (8).
Es una lesión bien definida de aspecto globular.
Pueden calcificarse (50%) y tener áreas quísticas.
Existen casos de hemorragia intraventricular.
TC
- iso/hiperdensa.
RM
- iso/hipointensa en las imágenes potenciadas T1.
- iso/hiperintensa en T2.
El edema periventricular puede ser secundario a la reversión del flujo del LCR transependimal o a la secreción del factor de crecimiento endotelial vascular por el meningioma (8).
- realce intenso con contraste (muy vascularizados).
- en algunos meningiomas existe una reducción de la difusión por la alta densidad celular.
- en pRM muestran un alto el volumen de sangre y la persistencia de material de contraste en el intersticio del tumor debido a la falta de un barrera hemato-encefálica.
- en la eRM el nivel de colina es elevado con cantidades variables de lactato,
lípidos y la alanina (doblete centrado a 1,47 ppm) sin pico NAA (6,20).
GLIOMA CORDOIDE
Es una neoplasia glial descrita en 1998 por Brat y colaboradores (8,21).
Son lesiones raras y por lo tanto la información demográfica es limitada con un predominio del sexo femenino (02:01-03:01) y una edad media de 46 años.
Es un grado II de la OMS de crecimiento lento que parece provenir de una célula ependimal de origen desconocido que se encuentra en la región anterior del tercer ventrículo y el hipotálamo (11).
Debido a su localización,
los pacientes presentan una disfunción hipotalámica,
hemianopsia homónima o aumento de la presión intracraneal.
La resección total logra un aumento de la supervivencia,
pero esto con frecuencia no se puede lograr debido a la ubicación y muy frecuentemente recurren.
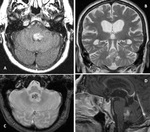
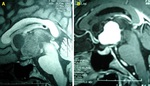
Hallazgos radiológicos:
Es una tumoración ovoide bien circunscrita en la región anterior del tercer ventrículo y el hipotálamo (22).
Pueden tener componente quístico.
Son raras las calcificaciones.
TC
-hiperdensas.
RM
- isointensa en las imágenes potenciadas en T1
- hiperintensa en T2.
Edema perilesional
- realzan con avidez después de la administración de contraste.
TUMOR GLIONEURONAL EN FORMACIÓN DE ROSETA (TGNR)
Es muy raro (por lo que no se han podido aportar imágenes originales).
Se incluye como neoplasia glioneuronal grado I en la clasificación de la OMS (11) y se ha sugerido que surgen de las células progenitoras pluripotenciales de la placa subependimaria (8).
Típicamente ocurren en los adultos jóvenes (media edad de 31,5 años) con una proporción de mujer-hombre de 1,75:1.
Tienen un comportamiento indolente y curan tras resección quirúrgica (8,
23).
Hallazgos radiológicos:
Originalmente descritos como típicos del cuarto ventrículo,
pero también se han encontrado en otras localizaciones.
Masa mixta, sólida y quística,bastante bien delimitada,
heterogénea y con realce heterogéneo con contraste.
Pueden tener hemorragia intratumoral y calcificaciones.
METASTASIS Y OTRAS NEOPLASIAS INTRAVENTRICULARES
Las metástasis intraventriculares representan el 0,9-4,6 % de las metástasis cerebrales.
En los adultos las más comunes son de el carcinoma renal,
de colon y el de pulmón son los más comunes; en niños las de el neuroblastoma,
tumor de Wilms y el retinoblastoma son los más frecuentes (2,
8).
Hallazgos radiológicos:
Son más comunes en los ventrículos laterales,
pero también puede aparecen en el III y IV ventrículo.
Una metástasis solitaria puede ser indistinguible de un meningioma o una neoplasia del plexo coroideo, pero si existe un antecedente de tumor primario,
debe plantearse la sospecha de metástasis como primera opción.
Captan intensamente contraste y el edema vasogénico se puede ver en el parénquima cerebral adyacente.
La detección de lípidos mediante espectroscopia en las metástasis es un marcador de necrosis,
característica de estos tipos de tumores (6).
Existen otras neoplasias que implican el sistema ventrícular como el linfoma,
gliomas bajo y de alto grado,
lesiones vasculares,
craneofaringioma intraventricular y tumor neuroectodérmico primitivo (7).