El adenocarcinoma (ADC) es el subtipo histológico más frecuente de carcinoma de pulmón en muchos países del mundo.
Histológicamente,
es también la forma más variable y heterogénea de cáncer de pulmón.
De acuerdo a la nueva clasificación de la IASLC/ATS/ERS Fig. 1,
el adenocarcinoma puede clasificarse en:
LESIONES PREINVASIVAS
Hiperplasia adenomatosa atípica (AAH): proliferación localizada y de pequeño tamaño (<5mm).
Adenocarcinoma in situ: Adenocarcinoma localizado,
de pequeño tamaño (≤3 cm) con crecimiento lepídico y ausencia de invasión estromal,
vascular o pleural.
El AIS se subdivide en variantes no mucinosas,
mucinosas y mixtas,
aunque virtualmente todos los casos de adenocarcinoma in situ son del tipo no mucinoso.
Adenocarcinoma mínimamente invasivo (MIA): adenocarcinoma solitario,
de pequeño tamaño (≤3 cm),
con patrón de crecimiento predominantemente lepídico y componente invasivo ≤5 mm de diámetro máximo.
LESIONES INVASIVAS
Supone más del 70-90% de todos los tumores pulmonares resecados.
Se clasifican según el subtipo histológico predominante (lepídico,
acinar,
papilar,
micropapilar y solido).
- Adenocarcinoma predominantemente lepídico (invasión≥5mm).
Contiene > 5 mm de otro subtipo histológico distinto al lepídico (acinar,
papilar,
micropapilar o sólido),
ó + de 5 mm de estroma miofibroblástico con células tumorales invasivas o bien invasión de linfáticos,
vasos sanguíneos o pleura o presenta necrosis tumoral.
- Adenocarcinoma predominantemente acinar
- Adenocarcinoma predominantemente papilar
- Adenocarcinoma predominantemente micropapilar
- Adenocarcinoma predominantemente sólido con producción de mucina.
- Y las variantes: mucinosa invasiva,
coloide,
fetal y entérica.
El 70% de los cánceres de pulmón son detectados en estadíos avanzados y son irresecables.
En estos pacientes se recomienda realizar la determinación de mutaciones en el gen que determina el receptor del EGG (EGFR),
teniendo en cuenta que los pacientes que presentan este tipo de mutación presentan una mejor respuesta al tratamiento con inhibidores de la tirosin kinasa (ITK).
Los adenocarcinomas invasivos no mucinosos son los que en mayor proporción presentan mutación en el receptor del factor de crecimiento epidérmico (EGFR).
Numerosos casos clínicos publicados han intentado correlacionar las diversas características del tumor con la presencia de mutaciones en el EGFR, sin embargo este aspecto no ha sido conseguido todavía a través de suficientes estudios clínicos.
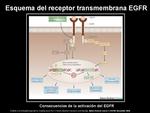
El EGFR es una proteína transmembrana que aumenta la actividad quinasa citoplasmática necesaria para el crecimiento celular Fig. 2.
En el cáncer de pulmón no microcítico (CPNM),
el EGFR se expresa en cantidades mucho mayores que en el tejido pulmonar normal.
Las mutaciones en el gen que sintetiza el EGFR ,
tal y como anteriormente hemos indicado,
identifican una subpoblación de pacientes con una mejor respuesta al tratamiento con los inhibidores de la tirosin-kinasa.
Gefitinib (Iressa®) y erlotinib (Tarceva®) son 2 inhibidores tirosin-kinasa (ITK) utilizados en el tratamiento del cáncer de pulmón de célula no pequeña (CPCNP) que inhiben de forma reversible al EGFR,
interrumpiendo la transmisión de la señal de crecimiento celular tumoral. El descubrimiento de las mutaciones activadoras del dominio tirosina-quinasa del gen EGFR como la delección del exón 18,
la del exón 19,
la mutación L858R del exón 21 se asociaron específicamente a la respuesta al tratamiento con TKIs.
De forma global,
la frecuencia de la mutación en los CPCNP es del 5–20% dependiendo de la población estudiada,
siendo más frecuentes en mujeres,
no fumadoras,
histología de adenocarcinoma,
de raza asiática y en los casos bien o moderadamente bien diferenciados.
En nuestro medio,
la mutación del gen del EGFR se observa en aproximadamente el 15% de los CPCNP.
Alrededor de un 75% de los pacientes con mutación en el gen del EGFR responde al tratamiento con erlotinib/gefitinib,
mientras que entre los no mutados solo responde un 10%.
A pesar de la buena respuesta inicial,
en prácticamente todos los casos se observa una adquisición de resistencia a los inhibidores tirosin-kinasa de EGFR (EGFR-TKI) a medio plazo.
Desde el año 2010,
en nuestro hospital se realiza la determinación de mutaciones genéticas en aquellos pacientes que tienen un diagnóstico anatomopatológico de adenocarcinoma pulmonar,
con el objetivo de facilitarles el acceso a un tratamiento selectivo con inhibidores de la tirosin kinasa.
En el momento de realizar esta revisión (diciembre 2013),
en el Hospital Universitario Mútua de Terrassa, se habían realizado un total de 144 determinaciones de mutaciones,
de las cuales 21 resultaron positivas para la mutación EGFR.
A día de hoy,
abril del 2014,
el total de determinaciones asciende a 169,
de las cuales 24 han sido positivas (un 14,7%).
Del total de mutaciones positivas un 64,12% corresponden a adenocarcinomas y un 15,29 a carcinomas de células grandes.
De estos 21 pacientes,
13 fueron mujeres y 8 hombres. El promedio de edad fue de 68 años. De ellos 15 eran no fumadores y 6 fumadores o exfumadores.
(el 100% de las mujeres fueron no fumadoras)
En el 100 % de ellos se detectó la mutación del receptor del EGF a través de muestra procedente de biopsia o citologia (17 biopsias y 4 citologías).
En 6 casos se detectó una mutación a nivel del exón 21 (L858R) y en 12 casos la mutación detectada fue una delección a nivel del exón 19.
En 3 pacientes no se indicó el tipo de mutación.
De los 21 pacientes,
15 fueron tratados con inhibidores de la tirosinkinasa (gefitinib y erlotinib),
siendo la media de tiempo de tratamiento 9 meses con un rango comprendido entre 2 y 26 meses y la moda fue de 2 meses.
La causa de la interrupción del tratamiento fue en 12 casos por progresión de la enfermedad,
en 2 casos por toxicidad hepática.
Únicamente,
1 paciente continua en tratamiento.
La Rx de tórax fue la prueba inidical diagnóstica en 16 de los 21 pacientes,
en los 5 pacientes restantes la prueba que permitió el diagnóstico fue el TC de tórax.
En relación al estadiaje inicial de la patología en 12 de los 21 casos fueron clasificados como Estadío IV (cualquier T,
cualquier N,
M1 a,
b).Fig. 3
A continuación se expondrán diversos ejemplos de casos con mutaciones positivas del gen del EGFR incluidos en la revisión:
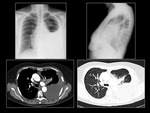
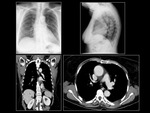
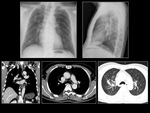
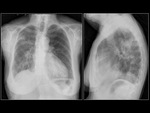
Paciente 1
Mujer de 71 años,
no fumadora,
con el diagnóstico de adenocarcinoma de pulmón con mutación en el gen EGFR.
El estadio al diagnóstico fue T4 M1.
La paciente fue tratada con inhibidores de la tirosin-kinasa durante 9 meses El tratamiento se suspendió por progresión de la enfermedad.
Fig. 4 Fig. 5
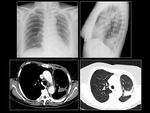
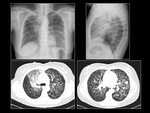
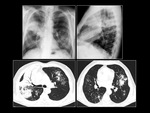
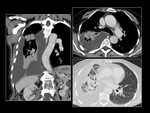
Paciente 2
Mujer de 63 años,
no fumadora, con el diagnóstico de adenocarcinoma de pulmón con mutación en el gen EGFR con delección del exón 19.
Al diagnóstico la patología presentó un estadio IV.
La paciente fue tratada durante 9 meses con inhibidores de la tirosin-kinasa.
El tratamiento se suspendió por progresión de la enfermedad.
Fig. 6 Fig. 7
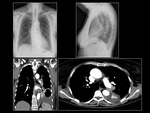
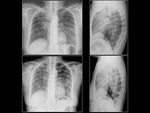
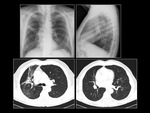
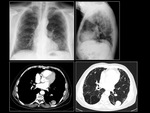
Paciente 3
Mujer de 56 años,
no fumadora,
con el diagnóstico de adenocarcinoma de pulmón con mutación en el gen EGFR en el exón 21 del tipo L858R.
Al diagnóstico la patología presentó un estadio IV.
La paciente fue tratada durante 2 meses con inhibidores de la tirosin-kinasa.
El tratamiento se suspendió por ausencia de respuesta al tratamiento. Fig. 8 Fig. 9
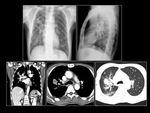
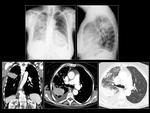
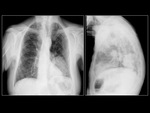
Paciente 4
Hombre de 51 años,
fumador,
diagnosticado de adenocarcinoma de pulmón con mutación en el gen EGFR con delección del exon 19.
Al diagnóstico la patología presentaba un estadío IV. El paciente tras 21 meses,
continua en tratamiento con inhibidores de la tirosin-kinasa.
Presenta mejoría de su patología.
Fig. 10 Fig. 11
Paciente 5
Hombre de 73 años,
fumador,
con diagnóstico de adenocarcinoma que presenta la mutación EGFR positivo en exon 19 tipo 748-751.
Al diagnóstico la patología presentaba un estadío IV.
El paciente fue tratado con inhibidores de la tirosin-kinasa durante un periodo de 10 meses.
El tratamiento se suspendió por progresión de la enfermedad.
Fig. 12 Fig. 13
Paciente 6
Hombre de 73 años,
no fumador,
con diagnóstico de adenocarcinoma que presenta la mutación EGFR positivo en exon 19 tipo 748-751.
Al diagnóstico la patología presentaba un estadío IV.
El paciente fue tratado con inhibidores de la tirosin-kinasa durante un periodo de 10 meses.
El tratamiento se suspendió por progresión de la enfermedad.
Fig. 14 Fig. 15 Fig. 16
Paciente 7
Paciente varón de 83 años, fumador,
con diagnóstico de el diagnóstico de adenocarcinoma de pulmón con mutación del gen del EGFR.
Al diagnóstico la patología presentaba un estadío IV.
La paciente fue tratada con inhibidores de la tirosin-kinasa durante un período de 2 meses.
El tratamiento se suspendió por progresión de la enfermedad.
Fig. 17 Fig. 18