La edad media de los pacientes incluÃdos es de 51 aÃąos,
un 44% de hombres y un 56% mujeres.
La neoplasia primaria mÃĄs frecuente es la de pulmÃģn seguida del tumor primario cerebral.
En nuestro centro existe un gran volumen de tumores cerebrales debido a que es centro de referencia,
pudiendo sobreestimar la prevalencia.
En dos pacientes no habÃa clÃnica neurolÃģgica en el momento del diagnÃģstico,
predominando en el resto de casos cefalea,
nauseas,
crisis y diversos dÃĐficits neurolÃģgicos multifocales.
Ãnicamente se realizÃģ punciÃģn lumbar en 3/9 casos sin repeticiones posteriores.
SÃģlo en un caso se obtuvo resultado positivo y las otras dos punciones no fueron valorables.
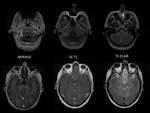
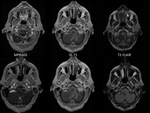
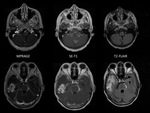
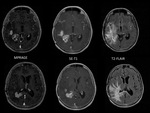
En 6/9 pacientes se considerÃģ que la clÃnica y la RM eran suficientes para establecer el diagnÃģstico. Fig. 2
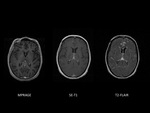
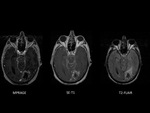
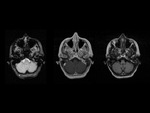
En el paciente nÚmero 8 no se identificÃģ realce leptomenÃngeo en ninguna secuencia con contraste.
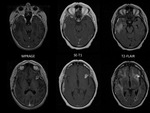
En la secuencia gradiente se objetivÃģ meningosiderosis y posteriormente en la punciÃģn lumbar se visualizaron cÃĐlulas malignas. Fig. 2 y Fig. 3
En los demÃĄs casos,
todas las secuencias identificaron el realce leptomenÃngeo.
Al analizar los resultados,
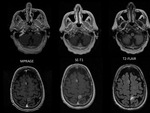
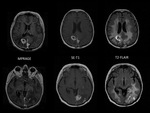
la secuencia SE-T1 sigue siendo la que en conjunto mejor visualiza el realce leptomenÃngeo y parenquimatoso (captaciÃģn constante de la meninge y de los implantes sÃģlidos si existen) seguida por la secuencia T2-FLAIR que si potencia la meninge lo hace de forma mÃĄs intensa que la secuencia SE-T1 aunque de forma mÃĄs variable,
puede no visualizar implantes.
La intensidad de captaciÃģn leptomenÃngea fue de 21/27 en SE-T1,
21/27 en T2-FLAIR y 13/24 en MPRAGE (en un paciente no se hizo esta secuencia) y parenquimatosa de 19/24 en SE-T1,
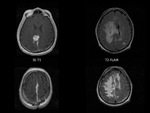
18/24 en T2-FLAIR y 17/24 en MPRAGE (un caso no tenÃa afectaciÃģn parenquimatosa). Fig. 3 Fig. 4 Fig. 5 Fig. 6 Fig. 7 Fig. 8 Fig. 9 Fig. 10 Fig. 11 Fig. 12 Fig. 13 Fig. 14 Fig. 15
En algunos de los estudios,
la SE-T1 y la T2-FLAIR no sÃģlo ven el realce menÃngeo sino que identifican un aumento de la seÃąal del LCR,
en la mayorÃa de los casos con mayor intensidad en la secuencia T2-FLAIR. La MPRAGE no muestra el aumento de seÃąal del LCR.
Se desconoce cual es el mecanismo exacto por el que se produce el realce menÃngeo.
Creemos que puede ser debido a aumento de seÃąal de la pia-aracnoides o por relleno del espacio subaracnoideo del contraste extravasado,
llegando a ver a veces de forma muy evidente un aumento de la seÃąal del LCR. Fig. 4 ,, Fig. 9 , Fig. 12
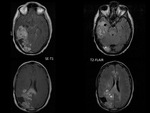
En las lesiones parenquimatosas cavitadas,
la secuencia SE-T1 muestra realce de la pared mientras que la T2-FLAIR,
en la mayorÃa de los casos,
es en la cavidad central.
Fig. 6 , Fig. 10 En ocasiones la T2-FLAIR tambiÃĐn identifica realce de la porciÃģn sÃģlida parenquimatosa. Fig. 7 ,
Fig. 9 ,
Fig. 12 , Fig. 13 , Fig. 15 Al revisar el orden de realizaciÃģn de cada secuencia,
en los casos en los que se potencia el componente sÃģlido parenquimatoso,
la secuencia T2-FLAIR se hizo en primer lugar (habitualmente en los primarios cerebrales donde se sospechaba afectaciÃģn menÃngea).
Esto puede hacernos sospechar que el tiempo que se espera al realizar la secuencia sea importante,
pudiendo objetivar un realce u otro en funciÃģn del mismo.
La MPRAGE muestra en todos los casos realce del componente sÃģlido,
siendo mucho mÃĄs constante.
DiscusiÃģn
La diseminaciÃģn leptomenÃngea tumoral o carcinomatosis meningea (CM) es una complicaciÃģn muy grave que ocurre en hasta el 15% de los pacientes neoplÃĄsicos.
Se define como la diseminaciÃģn de un cÃĄncer sistÃĐmico sÃģlido o hematolÃģgico o un tumor primario del SNC por la piamadre,
espacio subaracnoideo,
lÃquido cefalorraquÃdeo (LCR) y aracnoides.
El pronÃģstico de la CM no tratada es muy pobre,
con una mediana de supervivencia en el rango de unos pocos meses despuÃĐs del diagnÃģstico.
El tratamiento con quimioterapia intratecal o radiaciÃģn tiene el potencial de extender la supervivencia media de 6 a 10 meses.
Las neoplasias que con mÃĄs frecuencia presentan DLT son el cÃĄncer de mama,
pulmÃģn,
melanoma y procesos linfoproliferativos como LNH de alto grado y leucemias agudas linfoblÃĄsticas (linfomatosis menÃngea o meningitis leucemica).
Neoplasias del SNC primarias asociados con la metÃĄstasis leptomenÃngeas incluyen el glioblastoma multiforme,
el meduloblastoma ,
los tumores de la glÃĄndula pineal y tumores del plexo coroideo.
La diseminaciÃģn leptomenÃngea puede producirse por distintas vÃas: contigÞidad,
hematÃģgena y perineural.
En un alto porcentaje de casos coexiste con metÃĄstasis cerebrales intraparenquimatosas al momento del diagnÃģstico.
El diagnÃģstico de la CM se basa habitualmente en la combinaciÃģn de los hallazgos clÃnicos,
el examen del LCR y en la RM con gadolinio.
Los sÃntomas clÃnicos son muy inespecÃficos dependiendo del momento evolutivo y la localizaciÃģn de las lesiones.
Generalmente los pacientes presentan cefalea,
nauseas o dÃĐficits neurolÃģgicos focales,
pudiendo ocasionar sÃntomas encefalopÃĄticos por afectaciÃģn difusa del encÃĐfalo,
multineurÃticos o espinales,
siendo frecuente la afectaciÃģn multifocal.
En cuanto al anÃĄlisis del lÃquido cefalorraquideo sÃģlo el 3% de los pacientes con carcinomatosis leptomenÃngea tienen un LCR normal.
La presencia de aumento de presiÃģn del LCR (50% de los casos),
pleocitosis,
hipoglucorraquia moderada o intensa (75%) y aumento de proteÃnas (75%) es inespecÃfica.
La demostraciÃģn definitiva de carcinomatosis leptomenÃngea se basa en la verificaciÃģn de cÃĄlulas neoplÃĄsicas en el LCR.
AsÃ,
la citologÃa positiva para malignidad obtenida mediante punciÃģn lumbar PL establece el diagnÃģstico de certeza (> 95% de especificidad) y es condiciÃģn suficiente aunque no necesaria.
Su rentabilidad diagnÃģstica varÃa en funciÃģn del nÚmero de punciones lumbares realizadas (50% en la primera,
90% en la segunda con escasa mejorÃa en punciones ulteriores).
La citometrÃa de flujo puede facilitar el diagnÃģstico de cÃĐlulas neoplÃĄsicas en el LCR; su sensibilidad es del 70%,
pero su especificidad es del 95%.
En los casos en los que no es posible realizar PL o esta es negativa,
las tÃĐcnicas de imagen junto con la sospecha clÃnica son suficientes para establecer el diagnÃģstico.
AdemÃĄs la PL es una tÃĐcnica semi-invasiva no exenta de complicaciones.
Para el radiÃģlogo el diagnÃģstico precoz de meningitis carcinomatosa sigue siendo todo un reto.
Un hallazgo clave es la demostraciÃģn de realce leptomenÃngeo (pia y aracnoides) en las secuencias SE-T1 o FLAIR postgadolinio.
Este realce puede ser lineal difuso o nodular con o sin relace de los surcos o cisternas.
La hiperintensidad de la seÃąal en el espacio subaracnoideo se ha descrito en las imÃĄgenes FLAIR en todas las meningitis (infecciosa,
inflamatoria o neoplÃĄsica).
Sin embargo,
hiperintensidad FLAIR tambiÃĐn puede verse en la hemorragia subaracnoidea,
la melanosis leptomenÃngea,
ACV y en la enfermedad de Moyamoya.
Para complicar aÚn mÃĄs las cosas,
la hiperintensidad de los surcos en FLAIR tambiÃĐn se observa despuÃĐs de la administraciÃģn de propofol y en pacientes ventilados mecÃĄnicamente con de alta tensiÃģn parcial de oxÃgeno.
El diagnÃģstico diferencial del realce leptomeningeo es muy amplio e incluye la meningitis carcinomatosa,
la meningitis infecciosa (piÃģgena,
tuberculosis o micÃģtica),
la meningitis linfomatosa,
la neurosarcoidosis y la neurosÃfilis entre otras.
El sÃndrome SMART tambien debe de ser incluido en pacientes con tumores cerebrales que han recibido radioterapia previa.
En pacientes con un tumor con tendencia a metÃĄstasis leptomenÃngea,
con enfermedad sistÃĐmica avanzada,
manifestaciones clÃnicas tÃpicas de carcinomatosis leptomenÃngea,
LCR anormal (pero con citologÃa negativa) y RM indicativa de carcinomatosis leptomenÃngea,
debe considerarse este diagnÃģstico y tratarse como tal.
En otras situaciones,
como cuando las manifestaciones clÃnicas y la RM sugieren meningitis crÃģnica,
pero se desconoce la presencia de un tumor y el estudio del LCR no es diagnÃģstico,
se recomienda una biopsia menÃngea.
AsÃ,
la tendencia actual es hacia un incremento del peso de la RM en el manejo clÃnico de estos pacientes.
Las secuencias que se deben utilizar para la valoraciÃģn de afectaciÃģn menÃngea es tema de discusiÃģn.
ClÃĄsicamente se utilizan las secuencias potenciadas en T1 debido a que el gadolinio acorta en T1 y se ve hiperintenso.
En la secuencia potenciada en T2 el gadolinio acorta tambiÃĐn el T2,
siendo esperable hipointensidad.
En la secuencia T2-FLAIR el realce se debe a que el FLAIR es en inicio una secuencia potenciada en T1 en la que se utilizan tÃĐcnicas FAST-FLAIR o EPI-FLAIR para rellenar el espacio K,
pudiendo tener un TE efectivo que potencie la imagen en T2.
Hemos revisado la literatura y hemos encontrado escasas publicaciones que comparen las secuencias clÃĄsicas SE-T1 o 3D SPGR con la T2-FLAIR.
P.
Mathews et Al aseguran que las lesiones hiperintensas en la secuencia T2-FLAIR precontraste,
como los tumores parenquimatosos,
se verÃĄn mejor en SE-T1 con contraste que en T2-FLAIR y que esta Última es mejor que las secuencias clÃĄsicas potenciadas en T1 para la valoraciÃģn de patologÃa menÃngea y de la superficie cortical porque no muestra el realce de los vasos con flujo lento.
TambiÃĐn observaron que el realce era mÃĄs intenso en la secuencia realizada en Último lugar por lo que consideraron que uno de los factores mÃĄs determinantes en la valoraciÃģn del grado de captaciÃģn era el tiempo de espera.
T.
Hirota et Al refieren que la secuencia FLAIR parece mÃĄs sensible al demostrar realce leptomenÃngeo menores concentraciones de contraste.
S.
Kramer et Al,
consideraron que la adquisiciÃģn retardada postcontraste (indistintamente de que sea la T1 o FLAIR) es mÃĄs sensible que la adquisiciÃģn precoz para la valoraciÃģn de las lesiones menÃngeas.
TambiÃĐn aseguran que el FLAIR retardado postcontraste parece mejorar el diagnÃģstico de afectaciÃģn menÃngea infecciosa o tumoral si se compara con el retardado en T1.
Creen que pueden existir tres factores que influyan en estos resultados.
Por un lado la supresiÃģn del LCR conlleva a una mejor definiciÃģn de las lesiones menÃngeas.
AdemÃĄs estÃĄn de acuerdo con Hirota el Al y P.
Mathews en relaciÃģn a que es capaz de identificar menores concentraciones de contraste y que no muestra el flujo lento de los vasos.
Para explicar el realce menÃngeo creen que los vasos piales daÃąados permiten la extravasaciÃģn local al LCR adyacente a la superfÃcie cortical.
Waneerat et AL,
compararon la secuencia potenciada en T1 con saturaciÃģn grasa con la T2-FLAIR ambas postcontraste.
Estos autores consideran que las secuencias potenciadas en T1 son mejores que las imÃĄgenes potenciadas en T2 debido a que al suprimir la seÃąal de la grasa se delinea con mucha mÃĄs precisiÃģn la afectaciÃģn menÃngea,
mejorando la escala de grises mientras que la T2 no es tan precisa.
AdemÃĄs tienen dificultades para distinguir el efecto T2 de la captaciÃģn postcontraste debido a que en su protocolo no incluyen una secuencia T2-FLAIR precontraste.
Zhou Zheng-Rong et Al,
compararon la SE-T1 y la T2-FLAIR postcontraste para valorar el realce en tumores intracraneales.
En 7 casos el realce fue visualizado sÃģlo en SE-T1 mientras que en 4 sÃģlo en T2-FLAIR.
No encontraron diferencias estadÃsticamente significativas entre ambas secuencias para la detecciÃģn de tumores parenquimatosos,
considerando mejor la secuencia T2 para identificar lesiones superficiales,
en el sulcus o en regiÃģn periventricular.
AdemÃĄs,
esta secuencia fue capaz de objetivar,
en algunos casos mejor que la secuencia T1,
invasiÃģn de estructuras adyacentes.
Estos autores consideran que ambas secuencias son complementarias y que deberÃan incluirse en el estudio sistemÃĄtico de tumores intracraneales debido a que puede aportar informaciÃģn con relevancia clÃnica.
En nuestra serie de casos,
realizamos la secuencia T2-FLAIR pre y postcontraste,
eliminando la limitaciÃģn del estudio de Waneerat et AL que al carecer de la secuencia precontraste no distinguÃan con claridad el efecto T2 de la captaciÃģn. En todos los casos que la secuencia SE-T1 identificÃģ realce menÃngeo tambiÃĐn se visualizÃģ en la secuencia T2-FLAIR,
siendo habitualmente mucho mÃĄs evidente en esta Última por lo que puede ser una herramienta que nos ayude a confirmar una sospecha diagnÃģstica o a resolver una captaciÃģn dudosa.
Creemos,
en definitiva,
que la secuencia FLAIR aporta mayor definiciÃģn en estructuras superficiales y periventriculares debido a que anula la seÃąal del LCR.
AdemÃĄs no muestra el realce de los vasos con flujo lento eliminando por tanto esa posible fuente de error.
TambiÃĐn coincidimos con diversos autores en que el realce visualizado es probablemente debido tanto al realce leptomenÃngeo-pial como al del propio del espacio subaracnoideo por extravasaciÃģn vascular.
En nuestra serie la secuencia FLAIR tuvo grandes limitaciones en la identificaciÃģn de implantes sÃģlidos durales y tambiÃĐn de las lesiones parenquimatosas.
Por Último,
el realce de las lesiones parenquimatosas fue muy variable,
identificando realce en casi todos los pacientes pero en unas ocasiones mayoritariamente del componente sÃģlido y en otras del componente necrÃģtico central,
aunque a este respecto el momento en que se adquiere la secuencia parece ser muy importante.
Hay que seÃąalar que sÃģlo en un paciente se identificÃģ realce de una lesiÃģn no visualizada en la SE-T1,
tal y como se explica en el estudio de Zhou Zheng-Rong et Al. Asà pues,
pensamos que la secuencia FLAIR postgadolinio debe seguir siendo estudiada para conocer mejor sus utilidades diagnÃģsticas.
Las limitaciones mÃĄs importantes de este trabajo son el escaso tamaÃąo de la muestra y la ausencia de lectura sistemÃĄtica doble ciego de los hallazgos en imagen.