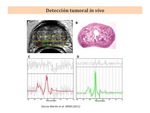
La espectroscopía in vivo que se realiza habitualmente en clínica es una técnica no invasiva que puede aportar importante información para el diagnóstico y seguimiento de distintas lesiones.
Las aplicaciones más conocidas actualmente de la espectroscopía in vivo son las que se llevan a cabo mediante espectroscopía localizada de 1H, monovoxel o multivoxel (imagen espectroscópica),
en cerebro,
próstata o mama.
Existen otras modalidades,
como la espectroscoía de 31P ó 13C,
pero son mucho menos frecuentes y sólo se llevan a cabo en unos pocos centros especializados.
Sin ninguna duda,
el uso clínico más extendido se circunscribe al sistema nervioso central.
Los principales metabolitos empleados en diagnóstico en el SNC son (Fig.
3):
NAA (N-acetil aspártico) - Marcador Neuronal.
Su disminución refleja un empobrecimiento neuroaxonal (típico en los tumores gliales)
mI(mioinositol) - Marcador Glial Su aumento refleja un aumento de la contribución glial (en tumores gliales es indicativo de tumor bajo grado). Su disminución indica desdiferenciación glial (tumores de alto grado)
Cho (Colina) - Metabolismo de Membrana. En Tumores es Indicador de Actividad Proliferativa. Aumenta en procesos de desmielinización e inflamatorios
Cr (Creatina) - Marcador del Metabolismo Energético. Se encuentra típicamente disminuida en tumores malignos (alto grado)
Lípidos móviles - Marcador de Malignidad (necrosis). No se suele hablar de malignidad a menos que estén presentes.
También aparecen con tratamiento radioterápico (radionecrosis).
Lac (Lactato) - Marcador del Metabolismo Anaeróbico.
Típico de tumores activos frente a tumores quiescentes.
También aparece en procesos hipóxicos/isquémicos e infecciosos/inflamatorios.
En cuanto a la próstata,
el número de metabolitos observados es menor:
Citrato - Marcador de tejido glandular prostático sin alteraciones.
Disminuye drásticamente en los adenocarcinomas.
Cho (Colina) - Marcador de actividad proliferativa. Aumenta en los adenocarcinomas.
Poliaminas. Al igual que el citrato,
su presencia es indicador de metabolismo glandular normal y se encuentran disminuidas en los adenocarcionomas.
Por último,
en la mama,
dada la gran contribución de las señales de lípidos,
que dificultan la observación de la mayoría de los metabolitos in vivo,
el único metabolito que se utiliza para el diagnóstico tumoral es la colina,
que se eleva de forma significativa en los tumores.
La espectroscopía por HR-MAS ex vivo por su lado tiene la ventaja de tener una gran sensibilidad y resolución espectral lo que permite la detección de múltiples metabolitos no visibles por espectroscopía in vivo, por tanto,
la especificidad diagnóstica es mucho más alta.
Así por ejemplo,
la espectroscopía in vivo sólo permite resolver un pico en la zona de los metabolitos derivados de colina,
mientras que el HR-MAS permite separar sus diferentes componentes: fosfocolina(PC) glicerofosfocolina(GPC) y colina (Cho).
Fig.
4 y Fig.
5.
Se realiza revisión bibliográfica de los resultados de la espectroscopía in vivo en comparación con la espectroscopía de alta resolución ex vivo y de la aportación en el diagnóstico de distintas patologías de ambas técnicas,
en concreto en tres tipos tumorales: cerebral,
próstata y mama.
CEREBRAL
Espectroscopía invivo: La espectroscopía in vivo a nivel cerebral ha demostrado su utilidad en la evaluación tumoral,
para ello se han medido principalmente varios metabolitos: NAA,
Cho,
lactato,
Creatina y Mioinositol. Fig.
3
Los niveles de Cho aumetan en multitud de tumores,
pero a nivel cerebral además sus niveles son significativamente mas altos cuanto mayor grado presente el tumor,
por tanto son útiles para diferenciar gliomas de bajo,
alto grado y patología benigna cerebral.
El NAA (ácido N-Acetil Aspártico) disminuye en aquellas patologías en la que existe empobrecimiento neuroaxonal,
como ocurre en los tumores gliales.
(19)
Estos metabolitos se han utilizado para diferenciar gliomas de bajo grado con lesiones isquémicas en personas jóvenes sin factores de riesgo para infarto cerebral donde el diagnóstico por imagen de RMN resulta cuanto menos complicado,
así,
los gliomas de bajo grado presentan picos altos de Cho (colina),
ausencia de NAA (Nacetil aspartato) y Lactato indetectable,
mientras que los infartos presentan picos bajos de Cho,
de NAA y un aumento significativo del Lactato.
EL Lactato se ha visto aumentado en gliomas de alto grado,
pero estos no suelen presentar dificultad para su diagnóstico en la imagen.
(19)
Espectroscopía ex vivo:
El HR-MAS a nivel cerebral es capaz de cuantificar multitud de metabolitos que no son visibles por espectroscopía convencional in vivo.
Martinez Bisbal y otros realizaron espectro HR-MAS de biopsias de gliomas de alto grado,
determinando 37 metabolitos.
(12)
Por otro lado se ha demostrado que existe una buena correlación del diagnóstico in vivo y ex vivo con la única salvedad de que en ex vivo aumentan metabolitos relacionados con el metabolismo anaeróbico,
lactato y alanina,
debido al periodo de hipoxia que experimentan las piezas de tejido hasta que son congeladas.
(12)
En estudio publicado en 2009 se determinó que los distintos niveles de los componentes del pico de colina total (tCho),
GPC (glicerofosfocolina),
PC (fosofocolina) y Cho (Colina libre),
y la relación entre estos,
es diferente según se trate de gliomas de bajo o alto grado.
Así,
en gliomas de bajo grado el componente que predomina es la GPC mientras que en Gliomas de alto grado predomina la PC.
(8) Fig.
5
Por otro lado parece existir correlación entre determinados metabolitos detectados por HR-MAS y la gradación del tumor.
Así el aumento del ratio PC/GPC se caracteriza con formas severas de glioblastoma multiforme.
Y un aumento del ratio de mioinositol/Cho permite diferenciar la evolución clínica de distintos gliomas de bajo grado.
(9)
También ha sido demostrada la utilidad de HR-MAS para el diagnóstico diferencial entre agresividad de meningiomas,
se determinó que los metabolitos glutamina y glutamato que están relacionados con el metabolismo del glutatión están significativamente más aumentados en meningiomas más agresivos y con mayor posibilidad por tanto de recurrencia.
(16)
PRÓSTATA
Espectroscopía in vivo
En la próstata la espectroscopía in vivo mediante RMN endorectal con técnica multivoxel ha demostrado gran utilidad para el diagnóstico del cáncer de próstata.
Las células epiteliales prostáticas tienen la peculiaridad de producir gran cantidad de citrato en condiciones normales,
como consecuencia de una inhibición de la enzima aconitasa mediada por zinc.
Sin embargo,
cuando se produce tranformación tumoral,
esta inhibición se pierde y los niveles de citrato caen drásticamente (Fig.
6).
Por otro lado,
como en otros procesos tumorales,
la colina aumenta significativamente.
Esta técnica ha demostrado ser de gran utilidad en casos de PSA elevado para localizar zonas de sospecha tumoral y así dirigir la dirigir la biopsia hacia una zona concreta (Fig.
7).
Por otro lado,
en casos de tratamiento radioterápico,
la espectroscopía prostática es de gran utilidad para el diagnóstico de recidiva local,
ya que tras el tratamiento el tejido prostático presenta una apariencia anodina y las técnicas de imagen resultan poco informativas.
Sin embargo,
la espectroscopía permite observar el pico de colina en aquellas zonas en las que hay recidiva.
(5)
Espectroscopía ex vivo
La determinación de metabolitos ex vivo que no son resueltos mediante espectroscopía in vivo han aportado información relevante en el cáncer de próstata.
Así se ha determinado que se puede diferenciar entre tejido maligno y no maligno utilizando los ratios de los espectros de GPC (Glicerofosfocolina) + PC (fosfocolina) y Creatina.
Además se ha determinado que los derivados de colinas son mejores biomarcadores de tumor que el propio citrato,
especialmente en la próstata central,
ya que el citrato aparece alto en células epiteliales prostáticas y bajo en tumor,
pero también aparece bajo en estroma.
Sin embargo las colinas aparecen altas sólo en tejido tumoral.
(20)
Por otro lado se ha visto que la relación Citrato/Creatina se relaciona significativamente con la agresividad tumoral.
(20)
Por último,
resulta interesante mencionar el trabajo de Asten et al. en el que se demuestra que el tejido de biopsia prostático no se altera después de realizarse el análisis por HR-MAS,
por lo que puede ser utilizado para diagnóstico histológico.(1)
MAMA
Espectroscopía in vivo:
La elevación del pico de colina,
al igual que en otros tipos de cáncer,
se utiliza como biomarcador de actividad tumoral,
sin embargo hay que ser cauto con esta afirmación ya que,
según se ha mostrado en varias publicaciones,
la elevación de colina puede deberse también a otras patologías de carácter benigno,
en concreto fibroadenomas,
adenomas tubulares y durante la lactancia (4,7,14).
Por otro lado,
la cuantificación de este metabolito mediante espectroscopía in vivo ha demostrado su utilidad para determinar la respuesta a tratamiento antes de que aparezca datos de respuesta clínica.
Así,
hay estudios que indican que a las 24 horas del tratamiento con doburrobuxina,
existen cambios significativos del pico de colina en la lesión tumoral y que la disminución del pico a las 24 horas se asocia a una mejor respuesta al tratamiento.
(4,13)
Espectrocopía ex vivo:
Al igual que en otros tejidos la espectroscopía ex vivo permite el análisis de muchos metabolitos no visibles mediante espectroscopía in vivo.
Lo que plantea la posibilidad de establecer un diagnóstico de agresividad tumoral basado en el perfil metabolico o metaboloma.
Esto resulta especialmente atractivo en el caso de la mama porque la espectroscopía in vivo plantea grandes dificulatades por la gran abundancia de lípidos en el tejido mamario,
que dificultan enormemente su realización de forma rutinaria.
Fig.
8
Se ha demostrado que existe un patrón metabolómico de cáncer de mama,
caracterizado fundamentalmente por aumento de Lactato y Glicina,
y de PC con respecto a GPC.
Comparando el perfil metabolómico con parámetros clínicos,
se ha demostrado que la Glicina,
Taurina y PC están más elevadas en tumores de mayor grado,
y que la relación PC/GPC está muy aumentada en tejido tumoral con respecto a sano.
(18)
En otro estudio se detectó que niveles altos de glicina y lactato predecían significativamente menor supervivencia a los 5 años en cánceres con RE (receptores estrogénicos positivos),
mientras que esta relación no se daba en pacientes con RE negativos.
Los resultados de predicción de supervivencia a los 5 años en mujeres con cánceres RE positivos resultaron más robustos que la predicción realizada clínicamente.
(10)
En los modelos de mejor pronóstico (basal-like) la concentración de GPC es más alta que la concentración de PC,
y lo contrario ocurre en los luminal-like.
(15,
11) La repercusión de un posible paralelismo entre perfil metabólico y tipo genético supone un importante campo para la metabolómica,
ya que los estudios genotípicos de cáncer de mama tienen un alto coste,
su realización requiere de mucho tiempo y además la realización de estos supone la destrucción de las muestras.