La tomografía computarizada (TC) torácica es parte de las exploraciones incluidas en el estudio de los pacientes candidatos a transplante de pulmón.
La utilidad de la TC en este contexto es principalmente detectar procesos malignos desconocidos,
como nódulos pulmonares o adenopatías; patología pleural o parenquimatosa,
dado que la afectación asimétrica puede condicionar la elección de un pulmón u otro en el transplante unipulmonar y por el riesgo de sangrado aumentado en el caso de la patología pleural; alteraciones anatómicas del árbol traqueobronquial que puedan condicionar la técnica quirúrgica o incluso contraindicar el procedimiento; hallazgos que sugieran infección (micetoma),
etc.
Realizamos una revisión de los pacientes trasplantados de pulmón hasta agosto de 2013 en nuestro centro (77 pacientes) así como de la literatura existente al respecto con el objetivo de aclarar los aspectos más relevantes a incluir en el informe de la TC previa a la cirugía y mostrar ejemplos ilustrativos.
1.
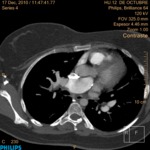
Existencia de afectación pleural.
En los inicios del trasplante pulmonar era considerada una contraindicación para la realización del mismo.
Actualmente no condiciona la morbimortalidad a corto ni a largo plazo,
aunque sí se ha demostrado que existe un aumento de las necesidades transfusionales operatorias en pacientes con antecedentes de biopsia pulmonar abierta,
drenaje crónico de empiema,
pleurodesis quirúrgica o con talco,
decorticación,
toracoplastia y bullectomía,
lobectomía,
neumonectomía y trasplante bipulmonar.
(Detterbeck et al). El volumen del hemitórax afecto es también considerado en la selección del donante en cuanto al tamaño pulmonar (se aceptan variaciones de volumen entre el 75 y el 125%).
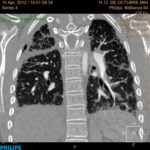
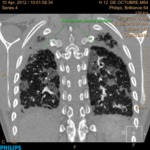
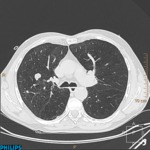
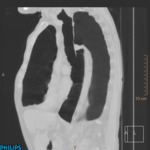
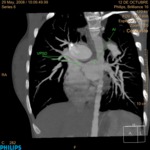
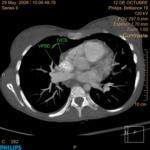
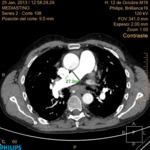
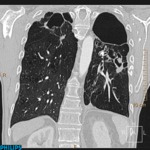
En muchos de nuestros pacientes existió patología pleural sin que se reportaran incidencias operatorias en relación con la misma.
(Fig. 1 y Fig. 2).
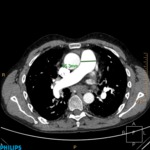
2 Asimetría en la patología pleural y parenquimatosa.
La afectación pleural asimétrica es un factor a tener en cuenta a la hora de decidir qué pulmón explantar primero,
aunque este criterio está más sujeto a la decisión del cirujano.
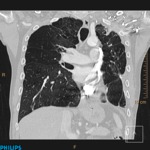
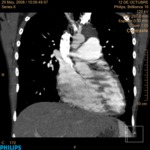
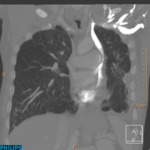
En pacientes con destrucción asimétrica del parénquima pulmonar el pulmón más afectado ha de ser quitado primero para disminuir la inestabilidad hemodinámica y la necesidad de circulación extracorpórea durante la cirugía.
Este parámetro también se puede valorar con radiografía de tórax y gammagrafía.
Además determina el pulmón a explantar en el caso de que el trasplante sea unipulmonar.
(Fig. 3).
La utilidad del análisis de los factores mencionados anteriormente ha sido puesta en entredicho en los pacientes afectos de fibrosis quística (FQ),
en los que hay autores (Marom et al.) que sugieren que la realización de la TC se puede reemplazar por los hallazgos de la radiografía de tórax,
los parámetros clínicos y las pruebas funcionales.
Esto es así porque la mayoría de los pacientes tienen afectación pleural,
muchas veces bilateral,
y en su estudio los hallazgos de radiología simple predijeron mejor la presencia o ausencia de patología pleural (81%) que la TC (69%),
con una sensibilidad y especifidad del 67% y 96% para la radiografía tórax y del 38% y 100% para la TC respectivamente.
Por otro lado,
dado que al ser una enfermedad supurativa siempre se realiza transplante bipulmonar,
la asimetría de la afectación parenquimatosa no juega un papel significativo en esta entidad (no así en pacientes candidatos a transplante unipulmonar).
Además en las TC realizadas a pacientes con FQ que finalmente se transplantan en la mayoría de los casos existe una afectación (bronquiectasias) simétrica.
Como comentaremos más adelante,
los pacientes afectos de FQ son jóvenes y de bajo riesgo para el desarrollo de neoplasias pulmonares; por estos motivos estos autores concluyen que la TC de rutina pretransplante en FQ sería prescindible.
3.
Detección preoperatoria de neoplasias ocultas.
Es imperativa por la mayor mortalidad que conlleva y la posibilidad de recurrencia del tumor en el injerto.
El diagnóstico de cáncer,
exceptuando los tumores cutáneos de bajo grado,
en los dos años previos es una contraindicación absoluta para ser incluido como candidato.
La presencia de neoplasia en el momento del transplante puede ser de hasta al menos el 5% (dependiendo del tipo de estudio y del país; en un estudio autópsico japonés de 1995,
Matsushita et al. analizaban la frecuencia de tumores malignos en el seno de FPI llegando a alcanzar el 48%),
fundamentalmente en pacientes con enfisema y fibrosis pulmonar idiopática (Ma et al.; Daniels et al.,
Bouros et al.).
Esta cifra ha aumentado por la mejora en la detección histológica (optimización del muestreo y de las técnicas de diagnóstico anatomopatológico),
la mayor edad de los pacientes transplantados que además son grandes fumadores,
más tejido disponible (un mayor número de transplantes bipulmonares implica mayor cantidad de tejido pulmonar analizable), así como aumento de transplantes en pacientes con fibrosis pulmonar idiopática/neumonía intersticial usual (FPI/NIU),
ya que la NIU es un factor predisponente para el desarrollo de neoplasias independiente del tabaquismo.
En un estudio (Strollo et al.) se objetivaron como factores de mayor riesgo de neoplasia oculta en el pulmón explantado la existencia de NIU y de NIU y EPOC de forma concomitante en las zonas de fibrosis; éste también era el caso en las áreas afectadas por radiación y en los grandes fumadores (más de 30 paquetes-año).
En este análisis se encontró en el estudio anatomopatológico de los pulmones explantados que había neoplasia incidental en casi el 3% de los pacientes estudiados y tras correlacionarlo con las imágenes previas al transplante que el 54% de ellas estaban ocultas en la TC . Todos los pacientes que tenían neoplasia eran grandes fumadores y la mayoría con NIU.
Además el 45% de las TC tenían una o más anormalidades benignas que podían simular neoplasia (nódulos estables o en resolución,
consolidaciones,
ganglios aumentados de tamaño,
etc.),
lo cual se comprobó a lo largo del seguimiento con TC.
Basándose en lo anterior,
estos autores proponen una TC de reevaluación a los tres meses para comprobar su resolución o cambio y que la última TC previa al transplante esté realizada en los tres meses anteriores al mismo y examinada por radiólogos especializados en radiología torácica para mejorar la detección de procesos malignos.
Además recomiendan la realización de PET-TC y/o biopsia endobronquial guiada por ultrasonido en el caso de pacientes con NIU y adenopatías >2 cm o si se ha observado aumento en el tamaño de las mismas.
Por su parte,
Kazerooni et al. no identificaron casos de neoplasias ocultas en los pacientes con Síndrome de Eisenmenger,
fibrosis quística o hipertensión pulmonar primaria (HTP) estudiados con TC,
si bien cabe señalar que la población del estudio englobada en estas patologías estaba constituida por una bajo número de individuos. Aunque los pacientes con FQ tienen un riesgo incrementado de desarrollar procesos malignos gastrointestinales éste no está aumentado para neoplasias intratorácicas (cáncer de pulmón,
linfoma o tumor de células germinales).
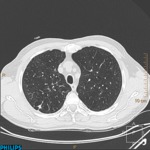
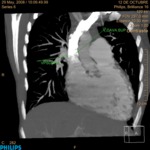
La detección de nódulos pulmonares (Fig. 4 y Fig. 5) aumenta el tiempo de espera para la inclusión en la lista de transplante.
Cuando exista un nódulo indeterminado en pacientes que por el estadio de su enfermedad no puedan realizar un seguimiento habitual (dos años con estabilidad o disminución del nódulo),
Strollo et al. proponen valorar la cirugía en pacientes seleccionados a pesar del hallazgo indeterminado debido al escaso margen de tiempo en esta situación.
4.
Anomalías o variantes anatómicas vasculares o bronquiales.
El tamaño bronquial,
la existencia de bronquios accesorios,
las alteraciones congénitas del árbol vascular,
las discrepancias en el tamaño de los vasos o los bronquios a anastomosar,
la presencia de trombosis arteriales o venosas,
etc.
son circunstancias que pueden condicionar la cirugía.
Así por ejemplo,
aunque en los útimos años se prefiere la anastomosis termino-terminal bronquial a la telescopada por presentar ésta mayor número de complicaciones (Garfein et al.),
hay grupos que realizan la anastomosis telescopada cuando existen discrepancias en el tamaño bronquial (Ng et al.).
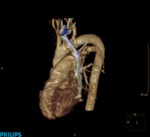
En nuestros pacientes encontramos casos de traqueobroncomegalia (Fig. 6),
drenaje venoso pulmonar anómalo (Fig. 7,
Fig. 8,
Fig. 9 y Fig. 10),
existencia de una vena cava superior izquierda (que aunque no condicionaba en este caso las anastomosis quirúrgicas,
hubiera podido hacerlo en el caso de un transplante cardiopulmonar) (Fig. 11 y Fig. 12),
trombosis crónica de la arteria pulmonar derecha (Fig. 13) y aumento del calibre de las arterias pulmonares (Fig. 14 y Fig. 15).
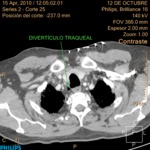
Se encontró también un pequeño divertículo traqueal (Fig. 16) que no condicionó la técnica por su localización.
5.) Procesos infecciosos.
La presencia de micetoma es considerada una contraindicación en algunos centros.
El engrosamiento pleural asociado a micetoma complica la disección anatómica y la extracción del pulmón nativo y conlleva el riesgo adicional de provocar una infección fúngica del espacio pleural.
En una serie de casos (Hadjiliadis D.
et al.),
la presencia de un micetoma en el pulmón nativo se asoció con una mortalidad perioperatoria del 45%.
Por tanto debe valorarse minuciosamente la selección de estos pacientes; aquellos con reacción pleural extensa y cavidades que impronten la superficie pleural serán generalmente excluidos.
En nuestra serie se sospechó micetoma en un paciente por los hallazgos de la TC que finalmente no fue confirmado microbiológicamente (Fig. 17 ).
Para la realización del transplante se deben excluir signos de infección activa,
siendo contraindicación absoluta para el mismo la infección crónica extrapulmonar no curable (incluyendo VHB,VHC y VIH).
La colonización con bacterias,
hongos o virus altamente resistentes o virulentos se considera una contraindicación relativa,
si bien es algo presente en la mayoría de los pacientes transplantados con FQ.
6.) Otros procesos:
Valorando las contraindicaciones absolutas,
relativas y las complicaciones postquirúrgicas que pueden surgir encontramos que también podría ser importante aportar información acerca de:
- Osteoporosis severa (contraindicación relativa).
- Deformidades de la pared torácica o de la columna vertebral (contraindicación absoluta).
- Signos morfológicos de posible disfunción cardiaca y afectación del árbol coronario.
- Alteraciones en otros órganos (si es que la TC los incluye por algún motivo) como hígado,
riñón y corazón.
La disfunción avanzada intratable de alguno de estos órganos es contraindicación absoluta de transplante (salvo que,
en el caso del corazón,
se plantee injerto cardiopulmonar).
Como reflejamos anteriormente también la existencia de neoplasia maligna descarta la selección del candidato.
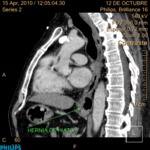
- Patología que condicione reflujo gastroesofágico (RGE) como la hernia de hiato (Fig. 18).
El RGE debe ser tratado de forma óptima antes y después del transplante,
ya que puede incrementar el riesgo de rechazo crónico del injerto.
- Hallazgos sugestivos de HTP que deben correlacionarse con los parámetros hemodinámicos con el fin de evaluar su severidad.
- Aunque no se utiliza en nuestro centro,
en algunos se realizan técnicas de preservación de la circulación bronquial con idea de disminuir el riesgo de isquemia en la anastomosis bronquial manteniendo el doble aporte (Petterson et al.). Éstas técnicas consisten en la extracción de las arterias bronquiales realizando luego una anastomosis con la arteria mamaria interna (arteria torácica interna),
por lo que podría ser de utilidad identificar la presencia de alteraciones a este nivel.