1.
SINDROME DE ENCEFALOPATIA POSTERIOR REVERSIBLE.
(PRES)
Descrito por primera vez en 1996 por Hinchey et al.
constituye una entidad caracterizada clÃnicamente por cefalea,
crisis,
encefalopatÃa y alteraciones visuales.
Aunque inicialmente se asociÃģ a hipertensiÃģn arterial severa,
eclampsia,
alteraciones renales e inmunosupresiÃģn,
el listado de causas se ha ampliado en los Últimos aÃąos,
encontrÃĄndose tambiÃĐn en asociaciÃģn con fÃĄrmacos inmunosupresores y quimioterÃĄpicos entre otras.
(tabla 1).

Table 1
Su patogÃĐnesis es todavÃa controvertida y existen dos teorÃas que intentan explicarla:
- Fallo de la autorregulaciÃģn cerebral.
La HTA severa excede los mecanismos de autorregulaciÃģn cerebral dando lugar a hiperperfusiÃģn con extravasaciÃģn capilar y edema vasogÃĐnico.
La mayor inervaciÃģn simpÃĄtica del territorio anterior actuarÃa como mecanismo protector.
- DisfunciÃģn endotelial acompaÃąada de vasoconstricciÃģn cerebral,
edema citotÃģxico e isquemia.
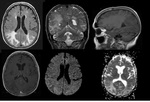
Los hallazgos radiolÃģgicos (Fig 1) muestran ÃĄreas de edema,
bilaterales y simÃĐtricas,
caracterizadas por mostrar hiperseÃąal en secuencias T2 y FLAIR,
con afectaciÃģn predominante de los lÃģbulos occipital y parietal.
Las regiones infratentorial y anterior tambiÃĐn pueden afectarse.
En la secuencia de difusiÃģn (DWI) las zonas afectadas son hiperintensas,
con valores altos en los mapas de ADC,
lo que traduce edema vasogÃĐnico.
En casos severos el ADC puede verse reducido localmente (edema citotÃģxico).
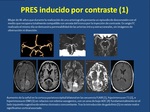
- Las lesiones caracterÃsticamente son reversibles en un periodo de corto (semanas) desde la instauraciÃģn de un tratamiento anti-hipertensivo y la retirada del agente causal, aunque en aquellas ÃĄreas con edema citotÃģxico es posible el desarrollo de isquemia y daÃąo residual (Figuras 2 y 3).
Nosotros presentamos el caso de un sÃndrome de PRES por el uso de Genciclavina (Figura 1) y otro caso de PRES tras la administraciÃģn de contraste yodado intravenoso (Figuras 2 y 3).
2. ACCIDENTES CEREBROVASCULARES (ACV) DE ORIGEN ARTERIAL O VENOSO
Son complicaciones raras de la quimioterapia.
Pueden causar daÃąo isquÃĐmico,
hemorrÃĄgico o tromboembolico por varios mecanismos,
como toxicidad directa en el endotelio vascular,
problemas de coagulaciÃģn,
lesiones vasculiticas,
estimulaciÃģn de fibroblastosâĶ
- A. TROMBOSIS.
Existen varios fÃĄrmacos que pueden causar tromboflebitis cerebral,
como el Cisplatino,
Bleomicina y Etoposido.
Presentamos el caso de una trombosis de una vena cortical por L-asparraginasa,
usada en el tratamiento de la leucemia.
(Figura 4).
El Bevacizumab por su parte,
se asocia con trombosis venosa cerebral.
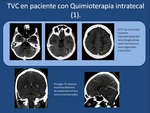
La Figura 5 muestra el caso de una trombosis masiva de senos durales en un paciente con tratamiento quimioterapico intratecal con Metotrexate,
Ara-C e hidrocortisona.
- B. CUADROS ICTALES Y PSEUDO/ICTALES
El uso combinado de quimioterapicos como asparraginasa,
5-fluoracil,
metotrexate y cisplatino ha sido relacionado con la apariciÃģn de ACV. El bevacizumab incrementa el riesgo de sufrir un evento tromboembolico.
El uso de Metotrexate intratecal tambien se asocia con la apariciÃģn de clÃnica neurolÃģgica que simula un ictus,
y con lesiones en RM hiperintensas en secuencias de difusiÃģn,
con valores bajos de ADC.
El estudio angiografico no revela anomalÃas y la clÃnica y las lesiones son reversibles.
(Figura 6)
- C.
SÃNDROME DE VASOCONSTRICCIÃN CEREBRAL REVERSIBLE (SVCR).
El SVCR engloba un conjunto de entidades (tabla 2) caracterizadas clÃnicamente por:
- Cefalea aguda de inicio sÚbito ("en trueno"),
con o sin otros sÃntomas neurolÃģgicos asociados.
- VasoconstricciÃģn arterial cerebral segmentaria y multifocal.
- LCR normal
- Reversibilidad de la clÃnica y las alteraciones angiogrÃĄficas en 12 semanas.

Table 2
Su fisiopatologÃa es desconocida.
Se cree que es causado por una alteraciÃģn transitoria en la regulaciÃģn del tono de la vasculatura cerebral.
Puede ocurrir espontÃĄneamente o provocado por factores desencadenantes,
los mÃĄs comunes son el postparto y la exposiciÃģn a sustancias vasoactivas (tabla 3).
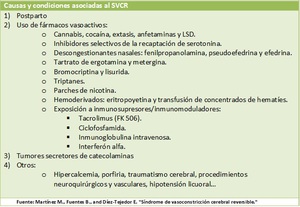
Table 3
Su principal diagnÃģstico diferencial es la arteritis primaria aislada del SNC.
Presentamos un caso,
sin fÃĄrmaco desencadenante confirmado.
(Figuras 7 y 8)
3. LESIÃN REVERSIBLE EN EL ESPLENIO DEL CUERPO CALLOSO.
La presencia de una lesiÃģn transitoria en el esplenio del cuerpo calloso se ha descrito en pacientes con encefalitis/encefalopatÃas de diferentes etiologÃas.
Puede estar causada por fÃĄrmacos antiepilÃĐpticos como la carbamacepina,
infecciones como la gastroenteritis por rotavirus,
el edema cerebral secundario a la altitud,
o desÃģrdenes metabÃģlicos como la hipoglicemia y la hipernatremia.
En imagen se muestra como una lesiÃģn redondeada u ovalada,
en el esplenio del cuerpo calloso,
que restringe la difusiÃģn,
lo que sugiere edema citotÃģxico,
aunque tambiÃĐn hay casos descritos con valores altos de ADC en relaciÃģn con edema vasogÃĐnico.
Suele resolver por completo despuÃĐs de un periodo variable de tiempo.
(Figura 9)
4.
TOXICIDAD CEREBELOSA INDUCIDA POR METRONIDAZOL:
El metronidazol es un antibiÃģtico y antiparasitario de la familia de los nitroimidazoles que inhibe la sÃntesis del ÃĄcido nucleico y que es utilizado para el tratamiento de infecciones provocadas por bacterias anaerÃģbicas y protozoos.
Sus efectos adversos neurolÃģgicos incluyen neuropatÃa perifÃĐrica,
marcha atÃĄxica,
disartria,
crisis convulsivas y encefalopatÃa.
En los estudios de RM se observan ÃĄreas de aumento de seÃąal en secuencias potenciadas en T2 en los nÚcleos dentados cerebelosos,
con valores altos en los mapas de ADC (edema vasogÃĐnico),
sin efecto de masa y sin realce tras la administraciÃģn de contraste.
Estas alteraciones revierten tras la retirada del fÃĄrmaco.
(Figura 10)
5.
LMP-IRIS
La Leucoencefalopatia Multifocal Progresiva (LMP) es una infecciÃģn desmielinizante destructiva causada por el poliomavirus JC que infecta a los oligodendrocitos en pacientes inmunodeficientes.
Asociada frecuentemente a SIDA,
trasplante de Ãģrgano,
cÃĄncer,
quimioterapia o cualquier inmunodepresiÃģn.
En un paciente con VIH y anomalÃas en la sustancia blanca subcortical hay que pensar en la LMP.
TambiÃĐn ha sido descrita tras el uso de Natalizumab,
un anticuerpo monoclonal usado como segunda lÃnea en el tratamiento de la esclerosis mÚltiple.
(Figura 11).
Se caracteriza por la presencia de placas desmielinizantes,
multifocales,
que afectan a la sustancia blanca subcortical extendiÃĐndose a la profunda y con respeto inicial de la sustancia gris.
Suele ser tÃpicamente bilateral y asimÃĐtrica,
sin efecto de masa ni realce tras la administraciÃģn de contraste.
En una fase mÃĄs tardÃa las lesiones son confluentes y con cavitaciones.
Aunque originalmente se hablaba de predilecciÃģn por la regiÃģn parieto-occipital,
la LMP puede afectar a todo el encÃĐfalo (incluyendo la fosa posterior),
y puede ser solitaria o multifocal,
con tamaÃąo variable desde pequeÃąas lesiones subcorticales hasta lesiones hemisfÃĐricas confluentes.
Los hallazgos radiolÃģgicos son:
- Lesiones hipointensas en T1 (lesiones "quemadas" y formas agresivas)
- Hiperintensidades subcorticales y periventriculares en secuencias potenciadas en T2 y FLAIR,
con afectaciÃģn de las fibras en "U" subcorticales,
dando una apariencia "festoneada".
- En difusiÃģn puede observarse restricciÃģn en las lesiones mÃĄs recientes.
- No hay realce tras la administraciÃģn de contraste,
aunque a veces puede verse un refuerzo perifÃĐrico dÃĐbil en pacientes con supervivencia prolongada.
- En la espectroscopia se observa una disminuciÃģn del pico de NAA con aumento de colina y lÃpido-lactatos.
El tratamiento consiste en la retirada del fÃĄrmaco y el uso de tÃĐcnicas para eliminarlo del plasma,
como el intercambio plasmÃĄtico o la inmunoadsorciÃģn.
Durante el tratamiento con estas tÃĐcnicas puede aparecer un empeoramiento de la clÃnica y los hallazgos radiolÃģgicos,
debido a la rÃĄpida restauraciÃģn del sistema inmune conocido como IRIS (sÃndrome inflamatorio de reconstituciÃģn inmune).
6.
TRASTORNOS NEUROLÃGICOS SECUNDARIOS AL USO DE ANTI-TNF.
Los fÃĄrmacos anti-TNF son usados en el tratamiento de trastornos autoinmunes como la Artritis Reumatoide,
Artritis PsoriÃĄsica,
Espondilitis Anquilosante,
Artritis crÃģnica juvenil y Enfermedad de Crohn.
Se han asociado con mÚltiples trastornos neurolÃģgicos como la neuropatÃa perifÃĐrica (Guillain-BarrÃĐ...),
el desarrollo de Esclerosis MÚltiple,
Neuritis Ãģptica y mielitis transversa aguda.
Presentamos el caso de una paciente a tratamiento con Adalimumab para una artritis psoriÃĄsica,
que desarrollÃģ una mielitis secundaria al uso de anti-TNF (Figura 12).
El uso de anti-TNF tambiÃĐn se ha asociado a un mayor riesgo de infecciones oportunistas en el sistema nervioso central,
tales como tuberculosis cerebral,
meningitis por criptococos,
toxoplasmosis,
asà como infecciÃģn por Lysteria,
Nocardia...
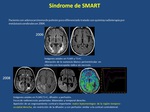
7. SÃNDROME DE SMART (stroke-like migraine attacks after radiotherapy).
A pesar de que no es una complicaciÃģn secundaria a un fÃĄrmaco,
incluÃmos aquà este sÃndrome debido a que tiene unos hallazgos radiolÃģgicos caracterÃsticos.
Se trata de una complicaciÃģn tardÃa de la radioterapia craneal que se manifiesta con clÃnica de disfunciÃģn neurolÃģgica reversible que puede incluir cefalea (con o sin aura),
dÃĐficit neurolÃģgico y/o crisis.
La fisiopatologÃa de este sÃndrome no estÃĄ del todo esclarecida,
aunque tiene similitudes con el sÃndrome de PRES.
Se piensa que puede ser debido al daÃąo endotelial causado por la radioterapia (vasculopatÃa reversible) o bien por disfunciÃģn neuronal por radiaciÃģn.
Deben descartarse otras causas de afectaciÃģn neurolÃģgica como recidiva tumoral,
diseminaciÃģn leptomenÃngea o enfermedad isquÃĐmica.
Las imÃĄgenes de RM muestran tÃpicamente engrosamiento y edema cortical,
con afectaciÃģn predominante de la corteza parieto-occipital.
Tras la administraciÃģn de contraste se observa un realce giriforme.
(Figura 13).