INTRODUCCIÓN:
Se considera infertilidad cuando tras un año de relaciones sin protección no se consigue un embarazo3.
En España se estima que un 15% de las parejas tienen problemas de fertilidad.
El estudio comienza habitualmente con la historia clínica y la realización de ecografía transvaginal,
ya que tiene una alta disponibilidad y permite valorar la morfología uterina y ovárica.
A continuación y dado que la causa más frecuente de infertilidad es la obstrucción de las trompas,
se realiza una hiterosalpingografía (HSG).
La HSG permite valorar la permeabilidad tubárica y la morfología de la cavidad endometrial,
si bien no se puede diferenciar entre patologías como pólipos,
sinequias,
miomas submucosos,
adenomiosis,
etc.
En los últimos tiempos se ha extendido el uso de la resonancia magnética ya que presenta una mayor resolución espacial y permite diferenciar entre determinadas patologías donde la ecografía y la HSG no llegan.
Otras ventajas de la RM es que es poco invasiva,
no utiliza radiaciones ionizantes,
permite obtener imágenes multiplanares y es menos observador dependiente.
Por otra parte presenta una serie de desventajas como largos tiempos de exploración,
alto coste y está contraindicada en pacientes con marcapasos,
implantes cocleares,
etc 3,5.
Adquisición de imágenes de RM:
La prueba se realiza habitualmente con la paciente en supino con la vejiga vacía y en ayunas de 6 horas y se administra un agente para inhibir la motilidad intestinal (generalmente glucagón).
Se realizan secuencias potenciadas en T2 (FSE) en plano sagital,
axial y coronal y una secuencia coronal de alta resolución en el eje largo del útero para valorar la cavidad endometrial y distinguir con exactitud la zona de unión.
El estudio incluye secuencia T1 y T1 con supresión grasa para disntinguir entre presencia de grasa o sangre.
Las secuencias postcontraste,
difusión y secuencia coronal T2 de abdomen de adquisición rápida no se realizan de rutina,
solo en casos seleccionados2,3,4.
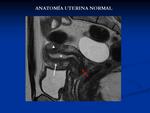
Anatomía normal:
En secuencias T2 es donde mejor se valora la anatomía.
El endometrio es hiperintenso,
después está la zona de unión marcadamente hipointensa (transición entre miometrio y endometrio) y finalmente el miometrio de señal intermedia.
El espesor endometrial varía entre 1,5 cm en chicas jóvenes (según la fase del ciclo) hasta 5 mm en mujeres posmenopáusicas.
El cérvix uterino presenta una capa interna hiperintensa (mucosa),
capa media hipointensa (estroma) y el exterior de señal media.
Las paredes de la vagina son hipointensas.
El estroma ovárico es hipointenso con pequeños quiste hiperintensos que son los foliculos. En mujeres posmenopáusicas el cuerpo uterino es de pequeño tamaño con mala definición de la zona de unión y los ovarios son difíciles de delimitar dada la ausencia de folículos 2,3,5.
Fig. 1
PATOLOGÍA ASOCIADA A LA INFERTILIDAD:
Las patologías más frecuentes asociadas a infertilidad las clasificamos en:
- Anomalías uterinas congénitas: malformaciones uterovaginales.
- Anomalías uterinas adquiridas: Adenomiosis y leiomiomas.
- Anomalías extrauterinas:
- Anomalías tubáricas: Hidrosalpinx y EPI.
- Endometriosis.
- Trastornos ovulatorios: tumores hipofisarios y Sd.
ovario poliquístico.
1.- Anomalías uterinas congénitas:
MALFORMACIONES UTEROVAGINALES:
Están presentes en el 25-30% de las mujeres con infertilidad3,6.
Los conductos mullerianos son estructuras pares que se fusionan entre la 6 y 11 semanas de gestación para formar el útero,
trompas y dos tercios superiores de la vagina4.
En un 30% de los casos se asocian con anomalías renales.
La HSG y la ecografía sirven para detectarlas aunque para caracterizarlos adecuadamente,
sobre todo para planificar el tratamiento la resonancia es la técnica de elección 7,8.
La Sociedad Americana de Medicina Reproductiva establece la clasificación más aceptada,
a pesar de que no incluye determinadas anomalías vaginales 1,3,7,8.
*Clase I: Hipoplasia o Agenesia: Fallo en el desarrollo de los conductos mullerianos (MDA) con resultado de hipoplasia o agenesia del útero,
cérvix y de los dos tercios superiores de la vagina.
Se manifiesta en la adolescencia con amenorrea.
En los casos de hipoplasia puede haber un útero rudimentario funcionante que causa dolor abdominal mensual.
Se subclasifican en:
- IA: Hipoplasia o agenesia de la parte superior de la vagina.
- IB: Hipoplasia o agenesia del cérvix.
- IC: Hipoplasia o agenesia del fundus uterino.
- ID: Hipoplasia o agenesia de la trompa.
- IE: Hipoplasia o agenesia combinada (dos o mas de las clases IA a la ID)
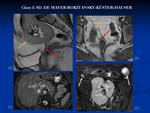
El caso más severo es el Síndrome de Mayer-Rokitansky-Küster-Hauser Fig. 2 .
Se caracteriza por ausencia completa de la vagina y en el 90% del cérvix y cuerpo uterino,
un 10% presentan conducto rudimentario con un remanente uterino que puede ser funcionante o no.
*Clase II: Útero unicorne: Es una anomalía asimétrica con un único cuerno que se abre a la vagina.
Se subdivide en:
- IIA: Cuerno rudimentario con una cavidad endometrial que comunica con un útero unicorne.
- IIB: Cuerno rudimentario con una cavidad endometrial que no comunica con un útero unicorne.
- IIC: Cuerno rudimentario sin cavidad endometrial.
- IID: Ausencia de cuerno rudimentario.
En la RM se visualiza un útero pequeño y asimétrico con forma de “banana”.
El cuerno rudimentario se valora mejor con RM que con la ecografía.
En caso de cuerno rudimentario no comunicante y no funcionante aparece hipointenso sin distinguir zona de unión.
En caso de cuerno funcionante no comunicante se manifiesta en la menarquia con dismenorrea y hematometra (lo que aumenta la probabilidad de endometriosis) y aparece la cavidad endometrial deformada con hiperseñal en T1 y T2.
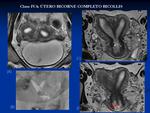
*Clase III.
Útero didelfo: Fallo completo en la fusión de los conductos mullerianos,
dando como resultado dos cavidades uterinas completamente separadas con dos cérvix y en la mayoría un septo longitudinal en la vagina.
Puede haber un septo parcial horizontal en una hemivagina dando como resultado un hematometrocolpos,
en estos casos casi siempre asocia agenesia renal en el mismo lado del septo.
Suele ser asintomático salvo en casos de obstrucción que se manifiesta con dismenorrea.
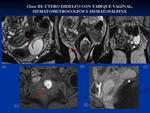
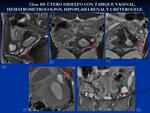
En la RM se ven dos cuernos uterinos bien desarrollados y completamente separados,
el contorno externo del útero presenta una hendidura profunda en todos los casos.
El hematometrocolpos se visualiza con hiperintensidad de señal en T1 y T2 y en casos severos hematosálpinx (siendo en estos casos necesaria la cirugía).
Fig. 3 Fig. 4
*Clase IV: Útero bicorne: Resultado de la fusión incompleta de los conductos de Müller.
Presenta dos cuernos simétricos que se fusionan caudalmente.
Se clasifica en:
- IVA: Útero bicorne completo: El septo llega hasta el orificio cervical interno (útero bicorne unicollis) o al orificio cervical externo (bicollis).
Fig. 5
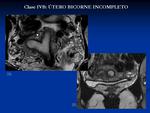
- IVB: Útero bicorne incompleto: El septo se limita al fundus uterino.
Fig. 6
Son asintomáticos con escasos problemas de fertilidad pero alta tasa de aborto diferido,
sobre todo en función de la longitud del septo.
En la imagen el útero tiene forma de corazón con dos cuernos muy divergentes.
Los criterios de RM para el diagnóstico son:
- Distancia intercornual superior a 4 cm.
- Hendidura del fundus superior a1 cm.
- La parte inferior del septo puede ser fibrosa y se ve hipointensa en T1.
- Siempre hay comunicación entre las cavidades incluso en el bicollis.
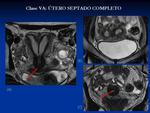
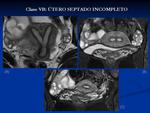
*Clase V: Útero septado: Es la más frecuente y se produce por fallo en la reabsorción del septo una vez que los conductos se han fusionado.
El septo suele tener componente muscular y fibroso.
Puede ser:
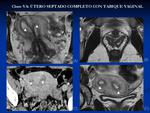
- VA: Útero septado completo: El septo se extiende más allá del orificio cervical interno.
Fig. 7 Fig. 8
- VB: Útero septado incompleto: El septo no sobrepasa el orificio cervical interno.
Fig. 9
El útero presenta un contorno exterior normal.
Se manifiesta generalmente con alto índice de abortos tardío.
La diferencia fundamental con el útero bicorne es la forma exterior que es de corazón en el bicorne con una hendidura superior a 1 cm.
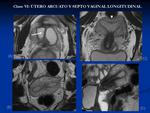
*Clase VI: Útero arcuato: Se considera una variante anatómica ya que no supone problemas de fertilidad.
La cavidad endometrial presenta una pequeña hendidura en el fundus con un contorno exterior normal.
Fig. 10
*Clase VII: Anomalías relacionadas con la ingesta de dietilbetilestrol: Es un estrógeno sintético usado en los años 40 a los 70 para prevenir abortos.
La exposición intraútero a éste estrógeno da como resultado aumento del carcinoma de células claras de la vagina y una serie de anomalías uterinas en las que se incluyen:
- VIIA: Útero con forma de “T”
- VIIB: Útero con forma de “T” y cuernos dilatados
- VIIC: Hipolasia uterina.
Aumenta el riesgo de aborto,
de parto pretermino y de embarazo ectópico si bien dado que no se usan desde hace más de 30 años esta patología se visualiza raramente en la actualidad.
2.- Anomalías uterinas adquiridas: ADENOMIOSIS Y LEIOMIOMAS:
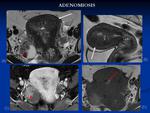
2.1 ADENOMIOSIS:
Es una enfermedad benigna que se caracteriza por la presencia de glándulas endometriales ectópicas en el miometrio (siempre sobrepasando de 2 a 3 mm la zona de unión) rodeadas de músculo liso hiperplásico.
Aunque es una enfermedad frecuente es una causa rara de infertilidad ya que suele afectar a mujeres de 35 a 50 años y con embarazos previos3,9.
Puede cursar con dolor,
dismenorrea y metrorragia10.
El estudio comienza con la ecografía pero se completa con RM dado que tiene una sensibilidad entorno al 65-85% y especificidad del 96%.
Hay dos formas 10,11:
- Difusa,
afecta a la totalidad del útero: Se visualiza aumento de tamaño del útero con engrosamiento difuso de la línea de unión que es superior a12 mm (el espesor normal es hasta 8 mm).
Aparece hipointensa en T2 con focos milimétricos hiperintensos en su interior que corresponden con glándulas endometriales dilatadas; Pueden verse focos milimétricos hiperintensos en T1 que indican hemorragia (sobre todo durante la menstruación).
Fig. 11
- Focal,
también llamada adenomioma: En RM se visualiza una masa hipoitensa en T2 mal definida con focos hiperintensos en T1 y T2 en su interior al igual que la forma difusa.
Se diferencia del mioma por que los bordes son peor definidos y en que el mioma tiene menor señal que el miometrio tanto en T1 como en T2 sin focos hiperintensos milimétricos en su interior.
En lo que refiere a la captación de gadolinio son indistinguibles.
El único tratamiento definitivo es la cirugía sin embargo en los últimos tiempos se están utilizando análogos de GnRH; Con la RM se puede monitorizar la efectividad de este tratamiento ya que muestra una mejoría en el engrosamiento en la zona de unión y disminución del número de focos hiperintensos.
2.2 LEIOMIOMAS:
Es la neoplasia ginecológica más frecuente (entre el 20-30% de las mujeres).
La RM es la técnica más exacta para establecer el número,
localización y tamaño de los miomas y ayudan a planificar y predecir la eficacia del tratamiento y seguimiento post-tratamiento1,
3,
12.
Se clasifican en:
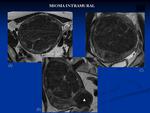
- Intramurales: Dentro del espesor miometrial.
Los más frecuentes y suelen ser asintomáticos.
Fig. 13
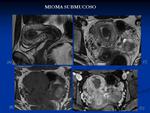
- Submucosos: Se introducen hacia la luz endometrial.
Los menos frecuentes (5%) pero los más frecuentemente sintomáticos.
Raramente son pedunculados y protruyen en el canal cervical o vagina.
Fig. 14
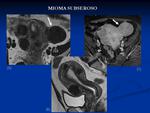
- Subserosos: Se extienden más allá de la serosa.
Suelen ser asintomáticos salvo que sean pedunculados y se torsionen.
Fig. 15
Aunque son una causa infrecuente de infertilidad,
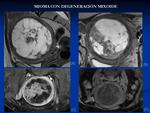
en este caso suele ser por compresión de las trompas o distorsión de la cavidad endometrial. En RM se visualizan como masas bien circunscritas,
homogéneas,
con menor señal que el miometrio en T2 Fig. 12 .
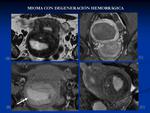
Algunos miomas tienen un anillo hiperintenso en T2 que corresponde a vasos linfaticos o venas dilatadas y que produce un realce en anillo con gadolinio.
Fig. 16 Fig. 17 En el diagnóstico diferencial hay que incluir: Adenomiosis,
masas anexiales,
contracciones uterinas y sarcoma uterino.
El tratamiento tradicional ha sido la cirugía (histerectomía o miomectomía).
En los últimos años se han desarrollado nuevas técnicas quirúrgicas: Miomectomía histeroscópica (para miomas subserosos),
miomectomía laparoscópica (en miomas subserosos),
coagulación laparoscópica del tumor,
éstas últimas para pacientes que tienen deseos de concepción.
Entre los tratamientos médicos se incluyen: análogos de GnRH y la embolización de la arteria uterina,
ambos producen un tratamiento sintomático y pueden usarse antes de tratamiento quirúrgico para disminuir el tamaño del tumor o los síntomas.
En estos casos la RM ayuda a predecir el resultado y seguir la efectividad del tratamiento en función de la señal y realce del tumor con gadolinio 3,12.
3.- Anomalías extrauterinas:
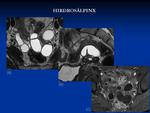
3.1 Alteraciones tubáricas: HIDROSÁLPINX Y EPI
Son la causa más frecuente de infertilidad (30-40%).
La histerosalpingofrafía permite evaluar adecuadamente la permeabilidad e irregularidad tubárica y presencia de adherencias peritubáricas,
sin embargo la RM permite una mejor caracterización de la patología causante de la obstrucción.
Se considera hidrosálpinx a la dilatación de la trompa con forma de “C” o “S” y ocupada por contenido líquido con finos septos incompletos en su interior que corresponden a los pliegues mucosos.
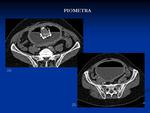
Fig. 18 La causa más frecuente de hidrosálpinx es la EPI,
que es una infección de transmisión sexual ascendente cervical o de vías bajas.
Junto con la historia clínica la ecografía suele ser suficiente para el diagnóstico,
si bien para la valoración de masas anexiales complejas y debido a la mayor disponibilidad en los servicios de urgencias se suele realizar una TC Fig. 19 ,
sin embargo la RM es más eficaz ya que no utiliza radiaciones ionizantes,
permite diferenciar con más exactitud entre diferentes tejidos blandos adyacentes y caracterizar masas anexiales14.
La EPI produce importantes secuelas que van desde el dolor pélvico crónico,
infertilidad hasta altas tasas de embarazo ectópico.
Los criterios para el diagnóstico de EPI son14:
- Piosálpinx: La trompa aparece dilatada con contenido heterogéneo pudiendo ver niveles líquido-detritus o líquido-líquido con la pared engrosada e irregular y realce con gadolinio.
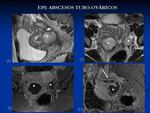
- Absceso tubo-ovárico: Masa mal definida con paredes gruesas e irregulares,
líquido y ocasionalmente niveles en su interior.
Puede verse un anillo interior hiperintenso en T1 con marcado realce que corresponde con tejido de granulación y hemorragia y un anillo periférico de alta señal en T2 que corresponde con edema3.
Fig. 20
- Hidrosálpinx
- Ovarios multiquísticos y presencia de líquido libre intraabdominal (criterios menores).
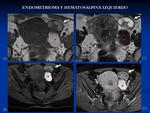
Otras causas de oclusión tubárica son: la torsión de la trompa (trompa dilatada con contenido líquido y que adquiere forma de “coma” con zonas de ausencia de realce); La endometriosis (trompa dilatada pero el contenido tiene señal alta tanto en T1 como en T2→hematosálpinx y suele asociar implantes endometriósicos ováricos y/o pélvicos) Fig. 21 ; Cáncer de trompa (hidro y/o hematosálpinx asociado a una masa que realza); Los embarazos ectópicos (se aprecia hematosálpinx con engrosamiento de la trompa y puede verse un saco gestacional)15.
Las trompas también se pueden afectar por patología extraginecológica como en casos de diverticulitis,
apendicitis o patología tumoral 2.
3.2 ENDOMETRIOSIS:
Se define como la presencia de tejido endometrial funcional fuera del útero,
la forma localizada es el endometrioma.
Afecta entre el 7-10% de las mujeres y llega hasta el 20-50% en mujeres con problemas de fertilidad10.
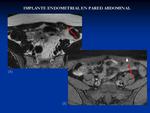
Las localizaciones más frecuentes son: ovario,
ligamento ancho,
trompa,
intestino,
vejiga,
parte posterior del fondo de saco de Douglas y cicatrices quirúrgicas (sobre todo en la cicatriz de cesárea)16,
17.
Fig. 22 Fig. 23 Es una causa muy frecuente de dolor pélvico e infertilidad en mujeres premenopáusicas.
Debido a los sangrados de repetición inducen una respuesta inflamatoria y con ello fibrosis y formación de adherencias.
El estudio comienza siempre con la ecografía tranvaginal que es muy útil para delimitar quistes endometriosicos pero que tiene poca fiabilidad para la visualización de implantes peritoneales de pequeño tamaño y adherencias,
para lo cual la RM es muy útil10,18.
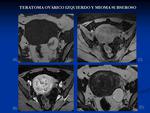
Los endometriomas se caracterizan por presentar una menor señal en T2 que el líquido normal (la señal varía en T2 en función de las hemorragias previas y el grado de fibrosis,
“efecto shading”) siendo marcadamente hiperintensas en T1,
por ello es fundamental incluir siempre en todo estudio de pelvis femenina una secuencia T1 con saturación de la grasa,
ya que permite diferenciarlo de la grasa de los teratomas maduros Fig. 24 y ayuda a la detección de lesiones muy pequeñas que pueden quedar camufladas entre la grasa pélvica17.
La presencia de hematosálpinx es altamente sugestivo de endometriosis y a veces puede ser la única manifestación de la enfermedad.
Fig. 21
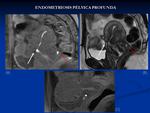
Los implantes endometriósicos pélvicos profundos aparecen como nódulos mal definidos (con pérdida de los márgenes de los órganos adyacentes),
hipointensos en T2 y pueden tener pequeños focos hiperintensos en T1 y realce con gadolinio debido a la presencia de fibrosis18.
El desplazamiento posterior del útero y ovarios,
angulación de asas intestinales,
elevación del fórnix vaginal posterior y presencia de colecciones líquidas deben hacer pensar en la presencia de adherencias 3,19.
La endometriosis lleva asociado un mayor riesgo de neoplasias ováricas,
fundamentalmente carcinoma de células claras o carcinoma ovárico endometrioide epitelial.
Se sospecha en caso de aumento de tamaño y de la señal en T2 de un endometrioma y principalmente por la aparición de nódulos sólidos con realce en su interior.
El tratamiento puede ser: médico,
con AINEs o anticonceptivos orales para mejorar los síntomas y análogos de GnRH.
La RM permite hacer un seguimiento de la evolución de las lesiones con el tratamiento médico,
sin embargo el tratamiento definitivo de elección es quirúrgico,
mediante laparoscopia ya que se eliminan implantes,
liberan adherencias y es la forma más sensible para diagnosticar la enfermedad10,18.
3.3 Trastornos ovulatorios: TUMORES HIPOFISARIOS Y SD.
OVARIO POLIQUÍSTICO (SOP)
SOP: El síndrome de ovario poliquístico es la alteración endocrina más frecuente en mujeres en edad reproductiva con importantes consecuencias para la salud como son infertilidad,
anovulación,
hiperplasia endometrial,
hiperandrogenismo,
diabetes y enfermedades cardiovasculares.
Hay controversia en cuanto a los criterios diagnósticos pero lo que todos tienen en común es la presencia de hiperandrogenismo.
Hay desequilibrio entre niveles de LH y FSH con incremento de la primera sobre la segunda lo que favorece la síntesis de andrógenos y estos probablemente son los causantes de la disfunción ovárica.
Se trata de un diagnóstico de exclusión.
En los últimos años se ha incluido la imagen ovárica como criterio diagnóstico (aunque no es suficiente ya que se pueden detectar ovarios poliquísticos de forma incidental).
La ecografía transvaginal es la técnica de elección.
Se consideran ovarios poliquísticos cuando: uno o ambos ovarios presentan 12 o más folículos de 2-9 mm en la superficie o el volumen ovárico excede los 10 cm3.
La RM no está indicada para el estudio del SOP dado su elevado coste y la adecuada caracterización con ecografía,
sin embargo puede ser útil en casos que no se puede realizar ecografía transvaginal y por vía abdominal no se consiguen visualizar los ovarios.
En la secuencia T2 aparece el ovario con abundante estroma central hipointenso y anillo periférico de quistes hiperintensos (siempre hay que tener en cuenta el volumen y el número de folículos)3,20.
Fig. 25
ADENOMA HIPOFISARIO: Constituyen el 10% de los tumores intracraneales y se clasifican en micro o macroadenomas en función de su tamaño (< o > de 10 mm respectivamente).
Los macroadenomas pueden dar síntomas compresivos sobre el quiasma óptico,
tallo hipofisario,
hipotálamo,
invasión de los senos cavernosos y pueden erosionar la silla turca.
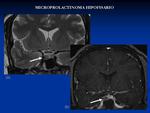
Los microadenomas no suele producir compromiso de espacio sin embargo es más frecuente que sean funcionales.
El prolactinoma es el tumor funcionante más frecuente y cursa con amenorrea y galactorrea en mujeres lo que puede llevar a infertilidad.
Un vez que se ha descartado que la hiperprolactinemia es por causas exógenas,
la RM es la técnica de elección para su diagnóstico.
Presentan una señal variable en T2 y en T1,
siendo generalmente discretamente hipointensos; Tras la administración de contraste presentan retraso y menor captación de contraste que la glándula normal.
Los macroadenomas suelen captar contraste de forma homogénea21.
Fig. 26