Animales
El estudio experimental se realizó en 18 ratas macho WAG/RijCrl de 2,5 meses de edad y 211-263g de peso.
Todos los procedimientos se practicaron de acuerdo con la legislación estatal vigente referente a la protección de los animales utilizados para experimentación y otros fines científicos.
Fluido Magnético
El magnetofluido se elaboró a partir de nanopartículas magnéticas de Fe3O4,
de 25nm.
En el proceso de síntesis las nanopartículas eran rodeadas de ligandos orgánicos lipídicos,
que mediante ultrasonificación,
permitían su suspensión en el Clinoleic® 20%,
una combinación de aceites de oliva (80%) y soja (20%) purificados cuyo uso está indicado en la nutrición parenteral.
De este modo,
se prepararon suspensiones de entre 3,5 y 5,5mg de nanopartículas de óxido de hierro en 0,4ml de Clinoleic® 20%,
que posteriormente serían infundidas individualmente a cada animal,
por vía percutánea intratumoral.
Anestesia
En el proceso de inoculación tumoral,
los animales se mantuvieron bajo anestesia inhalada inducida por Halotano.
Para la práctica de las exploraciones ecográficas,
la infusión intratumoral de los fluidos magnéticos,
y los estudios de RM,
se utilizó anestesia intraperitoneal a base de una inyección de Diazepam (25mg/kg) combinada posteriormente a los diez minutos con Ketamina (100mg/kg).
Inducción tumoral
En el día 0 del experimento a los animales se les practicó una laparotomía media subxifoidea para exponer el hígado.
Posteriormente se realizó punción subcapsular directa en el lóbulo hepático izquierdo,
para inyectar 25.000 células singénicas de adenocarcinoma de colon (línea celular: CC-531) suspendidas en 0,05ml de solución de Hank.
Control del desarrollo tumoral
Para monitorizar el desarrollo y progresión de las lesiones neoplásicas hepáticas,
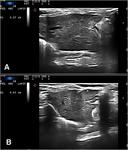
a los animales se les realizaron ecografías abdominales seriadas a los 21 y 28 días de la inyección tumoral.
Las ecografías se practicaron en un ecógrafo “MyLab60 XVision” de Esaote,
dotado con una sonda lineal multi-frecuencia de 6-18 Mhz (Fig.1).
Las ratas que no demostraron desarrollo tumoral fueron sacrificadas.
En los animales que se apreciaron masas neoplásicas se calculó el volumen tumoral mediante la fórmula: diámetro mayor x (diámetro menor)2 / 2
Procedimiento de infusión eco-guiada del magnetofluido
En el día 28 se procedió a la infusión intratumoral de los magnetofluidos,
en diez animales que habían desarrollado lesiones neoformativas.
Los diámetros máximos de los tumores fueron: mediana 8mm (rango: 10-4mm).
El procedimiento de infusión se practicó mediante punción directa transparietal de las lesiones neoplásicas,
guiada por ecografía y con técnica de manos libres (Ver Presentación Electrónica Científica: “ Experimento preliminar “ex vivo” de termoablación tumoral mediada por nanopartículas magnéticas.
Proceso I: monitorización por imagen de la infusión intratumoral”).
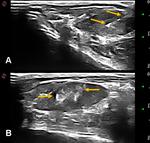
Tras verificarse la correcta ubicación intratumoral de la aguja se instilaban lentamente los magnetofluidos en el interior de los tumores (Fig.2).
En el caso de tumores grandes se requirieron de dos o tres punciones,
en lugares diferentes,
para alcanzar la mayor parte del tejido neoplásico.
Una vez administrado todo el fluido se retiraba la aguja y se realizaba presión sobre la superficie hepática con la propia sonda ecográfica para favorecer la hemostasia.
Estudios de RM
A las seis horas de la infusión de los magnetofluidos se realizaron los estudios de RM para valorar la idoneidad de la infusión (Ver Presentación Electrónica Científica: “Experimento preliminar “ex vivo” de termoablación tumoral mediada por nanopartículas magnéticas.
Proceso I: monitorización por imagen de la infusión intratumoral”).
Procedimiento de inducción y control térmico
El día 29,
tras 18 horas de la infusión de los magnetofluidos,
los animales fueron sacrificados mediante anestesia profunda y luxación cervical.
Posteriormente,
se extrajeron los hígados de los seis animales infundidos que habían desarrollado las lesiones tumorales de mayor tamaño,
y de otra rata no infundida que emplearíamos para control.
Una vez extirpados los hígados,
estos se sumergieron en suero fisiológico (n=5) o en agua destilada (n=2).
Previamente,
en el interior de las lesiones tumorales se habían implantado sondas para el registro de la temperatura.
En el medio en el que iban inmersos los hígados,
también se situó una sonda para monitorización térmica.
Posteriormente,
los hígados se dispusieron en el interior de la bobina inductora de RF (Fig.3).
Tras alcanzar el equilibrio térmico entre las sondas ubicadas en el interior del tejido hepático y el medio perihepático de inmersión,
20ºC,
los especímenes se sometieron,
durante un periodo máximo de 30 minutos,
a potencias de campo magnético de entre 12,5 y 16KA/m,
y frecuencias de hasta 699KHz.
Análisis histológico
Tras la finalización del procedimiento de inducción térmica,
los hígados se fijaron en formol para la realización de análisis histopatológico.
Se obtuvieron secciones representativas de tejido hepático y tejido tumoral; las muestras fueron teñidas con hematoxilina-eosina y azul de Perls para posterior estudio con microscopia óptica.
Mediante la primera tinción se evaluarían potenciales lesiones tisulares térmicas,
y con la segunda se identificarían los depósitos tisulares del hierro inyectado.