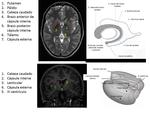
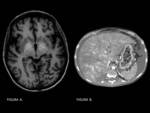
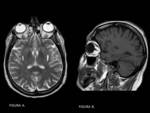
ANATOMÍA DE LOS GANGLIOS BASALES Y TÁLAMOS:
Los ganglios basales son núcleos pares de sustancia gris localizados en el interior de los hemisferios cerebrales que pertenecen al prosencéfalo.
Algunos autores consideran como parte de los ganglios basales el núcleo subtalámico y la sustancia negra,
sin embargo en este poster vamos a revisar exclusivamente la patología que afecta al nucleo caudado,
al putamen y al globo pálido.
El núcleo caudado está anatómicamente asociado con los ventrículos laterales,
sigue su curvatura y en él distinguimos tres porciones,
la cabeza,
localizada en el lóbulo frontal,
el cuerpo,
en el lóbulo parietal,
y la cola,
en el lóbulo temporal.
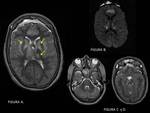
FIGURA 1.
El núcleo lenticular está compuesto por dos partes funcionalmente distintas, putamen (lateral) y globo pálido (medial),
y en cortes axiales se observa separado de la cabeza del caudado por el brazo anterior de la cápsula interna y del tálamo por el brazo posterior.
FIGURA 1.
Histológicamente el núcleo caudado y el putamen están compuestos por el mismo tipo de neuronas,
y se ha denominado conjuntamente núcleo neoestriado,
mientras que el globo pálido,
más rico en fibras,
se subdivide en segmento externo e interno,
con diferentes conexiones cerebrales en cada una de ellas.
Tanto el putamen como el pálido contienen abundantes mitocondrias,
aporte vascular y neurotransmisores,
y su elevada actividad metabólica así como utilización incrementada de glucosa y oxígeno los hacen vulnerables a anomalías metabólicas o enfermedades sistémicas.
La función de los ganglios basales es compleja.
Están principalmente implicados en la producción de movimientos y son parte del sistema extrapiramidal,
pero también participan en los circuitos emocionales,
de memoria y otras funciones cognitivas.
Cuando se encuentran afectados la sintomatología puede variar ampliamente,
desde trastornos del movimiento (corea,
tremor,
bradicinesia,
distonia) hasta coma,
dependiendo de si la afectación es aislada o existe un trastorno metabólico generalizado con necrosis cerebral extensa.
En RM,
el núcleo caudado y el putamen son isointensos respecto a la sustancia gris cortical en todas las secuencias,
y no realzan tras la administración de contraste.
El globo pálido puede aparecer discretamente hipointenso en secuencias T2 respecto al putamen,
un hallazgo normal por el depósito de hierro con la edad.
Los tálamos son estructuras localizadas en la línea media entre los hemisferios cerebrales y el mesencéfalo,
con dos porciones simétricas localizadas a ambos lados del III ventrículo que se comunican a través de la masa intermedia.
Estas estructuras quedan divididas en varios núcleos por estrías de sustancia blanca,
y están implicados en la transmisión de estímulos motores y sensitivos hacia y desde el córtex cerebral,
así como en la regulación de la consciencia,
el sueño y el estado de alerta.
FIGURA 1.
Es importante también conocer en profundidad los aportes vasculares de los ganglios basales por sus implicaciones clínicas.
La arteria cerebral anterior vasculariza la cabeza del caudado mediante las ramas perforantes anteromediales.
La arteria cerebral media,
mediante las ramas perforantes anterolaterales vasculariza el núcleo lenticular,
el núcleo caudado,
la cápsula interna y el tálamo.
La arteria comunicante posterior vasculariza la porción interna del tálamo.
La arteria cerebral posterior en su segmento P1 da ramas perforantes para el mesencéfalo y el tálamo (ramas talamoperforantes).
El drenaje venoso de los ganglios basales se hace a través del sistema venoso profundo. Las venas talamoestriadas superior e inferior drenan en las venas cerebrales internas,
que a su vez se unen a la vena de Rosenthal para formar la vena de Galeno.
Ésta confluye con el seno sagital inferior para formar el seno recto,
que drena en la tórcula.
- 1.
VARIANTES NORMALES:
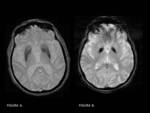
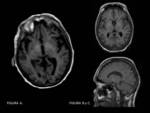
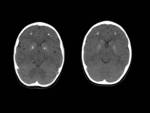
1.1. Dilataciones de los espacios perivasculares de Virchow-Robin:
Los espacios de Virchow-Robin (EVR) son los espacios perivasculares que rodean la pared de los vasos en su trayecto desde el espacio subaracnoideo a través del parénquima cerebral.
El aumento de tamaño de los EVR así como su frecuencia de aparición se relaciona con la edad.
En TC se observan como imágenes hipodensas de pequeño tamaño (menor de 1 cm),
únicas o múltiples,
de morfología redondeada-ovalada y bordes bien definidos que no producen efecto de masa ni tienen edema asociado.
En RM suelen tener la misma intensidad de señal que el LCR en todos los pulsos de secuencia.
En función de su localización,
los EVR dilatados se clasifican en tres tipos: tipo I,
II y III.
Los Tipo I se localizan en los ganglios basales y representan el espacio alrededor de las arterias lentículo-estriadas cuando entran en los ganglios de la base desde el espacio perforado anterior.
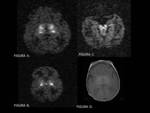
FIGURA 2.
Los tipo II se localizan en la sustancia blanca subcortical y los tipo III en la línea media tanto infra como supratentoriales.
1.2.
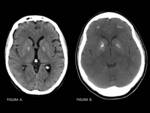
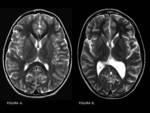
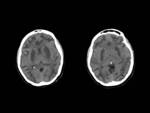
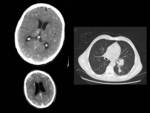
Calcificaciones bilaterales y simétricas:
Las calcificaciones bilaterales y simétricas en ganglios basales,
en concreto en los núcleos pálidos,
corresponden a depósito de material coloide en el interior y alrededor de los vasos cerebrales de menor calibre,
con la posterior calcificación de dicho material,
y cuando se encuentran en sujetos mayores de 40 años se pueden considerar fisiológicas.
Sin embargo,
las calcificaciones en los ganglios basales están relacionadas con múltiples patologías (hipoparatiroidismo,
pseudohipoparatiroidismo,
enfermedad de Fahr,
toxoplasmosis..etc.) y por ello cuando se observan calcificaciones en los pálidos en sujetos menores de 40 años o bien en otra parte de los ganglios basales,
núcleo dentado u otra parte del córtex en sujetos de cualquier edad debemos buscar indicios de patología.
FIGURA 3.
1.3.
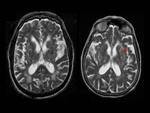
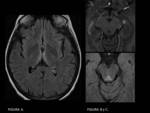
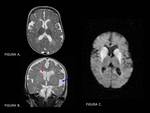
Hipointensidad asociada a la edad por depósito de hierro:
El acúmulo patológico de hierro en los tejidos cerebrales produce importante daño tisular y además se relaciona con el pronóstico de algunas patologías,
por lo que es fundamental distinguir los patrones normales de distribución de esta sustancia en el tejido encefálico.
Las secuencias con TR y TE largo muestran áreas hipointensas en relación con el acúmulo de hierro en su forma férrica.
Se pueden considerar fisiológicas las hipointensidades en secuencias T2 en pálidos en adultos sanos de edad media y ancianos.
El putamen presenta hipointensidades en T2 solamente en sujetos mayores de 60 años y el tálamo y el caudado no deben mostrar estas hipointensidades a ninguna edad.
FIGURA 4.
-2.
ENFERMEDADES METABÓLICAS:
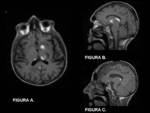
2.1 Patología hepática:
Los pacientes con cirrosis crónica,
hipertensión portal y shunts porto-sistémicos sufren daño cerebral a largo plazo porque los productos nitrogenados atraviesan la barrera hemato-encefálica.
En RM con secuencias potenciadas en T1 estos pacientes presentan con frecuencia áreas hiperintensas en globos pálidos y sustancia negra.
Estos hallazgos son atribuibles al depósito de manganeso,
que puede ser reversible tras el trasplante hepático.
Se han observado también en pacientes con atresia biliar,
sometidos a nutrición parenteral y en personas con exposición ambiental a manganeso.
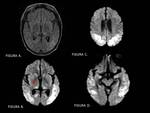
FIGURA 5 y 6.
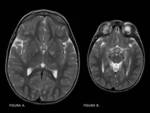
2.2 Enfermedad de Wilson:
La enfermedad de Wilson se produce por un acúmulo de cobre debido al déficit de ceruloplasmina,
su proteína transportadora en suero.
Los órganos afectados en esta patología incluyen el hígado y el cerebro,
y se asocia a síntomas neurológicos como disartria,
distonía,
tremor,
ataxia,
parkinsonismos y problemas psiquiátricos.
En RM los hallazgos característicos incluyen prolongación de señal T2 en putámenes (muy frecuente),
pálidos,
núcleos caudados y tálamos.
La afectación talámica está típicamente confinada en la porción ventrolateral.
Sin embargo,
se pueden afectar otras áreas del encéfalo y tronco cerebral,
y en estadios iniciales de la enfermedad con frecuencia se observa restricción de la difusión.
FIGURA 7.
2.3 Encefalopatía de Wernicke:
La encefalopatía de Wernicke se produce por un déficit de vitamina B1 como consecuencia de un estado de malnutrición en relación con alcoholismo crónico,
neoplasias gastrointestinales o hematológicas,
diálisis crónica,
obstrucción intestinal,
hiperémesis gravídica o nutrición parenteral prolongada sin suplementos vitamínicos.
Es una emergencia médica,
cuya terapia consiste en la administración intravenosa de tiamina,
y la triada clínica clásica de alteración de la conciencia,
disfunción ocular y ataxia no siempre se encuentra presente al inicio del cuadro.
Los hallazgos típicos en imagen incluyen hiperintensidad de señal T2 en el tálamo medial,
área periacueductal,
cuerpos mamilares y placa tectal.
Se puede observar también hemorragia petequial,
restricción de la difusión y realce con contraste de las áreas afectadas.
FIGURA 8.
2.4 Mielinolisis osmótica.
La desmielinización osmótica está relacionada con alteraciones electrolíticas,
especialmente con la rápida corrección de la hiponatremia,
y afecta a pacientes con malnutrición,
alcoholismo o debilitados tras un trasplante.
Esta patología se divide en mielinolisis pontina central o mielinolisis extrapontina,
y las manifestaciones clínicas son muy variables,
desde hemiparesia espástica,
parálisis pseudobulbar,
niveles disminuidos de conciencia y coma.
Las células oligondendrogliales son muy susceptibles al estrés osmótico,
y las alteraciones en RM derivadas de esta patología siguen la distribución de estas células en la protuberancia central,
tálamo,
putamen,
cuerpos geniculados laterales y otras localizaciones extrapontinas.
Se observa prolongación de la señal T1 y T2 en las zonas afectadas.
En la forma extrapontina de mielinolisis se observan áreas de hiperintensidad T2 en los núcleos pálidos,
putamen,
tálamo y cerebelo.
Estas lesiones pueden mostrar restricción de la difusión en los estadios iniciales aunque no es un hallazgo típico.
FIGURA 9.
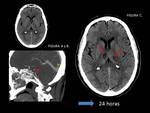
2.5 Encefalopatía hipóxico-isquémica.
Los hallazgos en imagen de la encefalopatía hipóxico-isquémica dependen de varios factores como la madurez cerebral,
la duración y la severidad del daño.
En los neonatos a término que sufren cuadros de asfixia severa se ve afectada la sustancia gris profunda (putamenes,
tálamos ventrolaterales,
hipocampo,
parte dorsal del troncoencéfalo y cuerpos geniculados laterales) y en ocasiones la corteza perirrolándica.
En RM,
se pueden detectar alteraciones en secuencias de difusión en las primeras 24 horas,
momento en el cual las secuencias T1 y T2 pueden ser normales,
con incremento de la restricción en ganglios basales (particularmente en la porción posterior de los putámenes),
región perirrolándica y a lo largo de los tractos cortico-espinales.
Las anomalías en difusión se hacen más prominentes en torno al 3º-5º día.
A partir del segundo día las áreas dañadas muestran hiperintensidad en T1 y T2.
La hiperintensidad en T1 en tálamos,
ganglios basales y córtex perirrolándico puede persistir varios meses.
La causa exacta de los cambios en la intensidad de señal en RM durante la primera semana aún no está del todo clara.
Se ha propuesto que el acortamiento de T1 se produzca por hemorragia,
calcificación,
liberación de lípidos por ruptura de la mielina o incluso los efectos paramagnéticos de los radicales libres.
FIGURA 10.
En los neonatos pretérmino los episodios de hipoxia-isquemia severos afectan a la sustancia blanca profunda y el troncoencéfalo.
Aunque se pueden ver lesiones en los ganglios basales,
lo más común es que se afecten los tálamos,
especialmente en neonatos con menos de 32 semanas de vida.
La mielinización de tálamos y pálidos se realiza en torno a la semana 24-25 de vida,
mientras que el núcleo estriado lo hace en la 35-36 semana,
por lo que la áreas mielinizadas con mayor actividad metabólica serán las que sufran un daño mayor en situaciones de hipoxia-isquemia.
En RM se observan alteraciones de los mapas de difusión en las primeras 24 horas,
que se harán más evidentes en torno al 3-5 días y posteriormente se pseudonormalizan.
Después de dos días se puede ver hiperintensidad de señal en secuencias T2 en tálamos y ganglios basales y el acortamiento de señal T1 comienza en el tercer día y persiste hasta la fase crónica.
En los adultos la encefalopatía hipoxico-isquémica es debida sobre todo a parada cardiaca y patología cerebrovascular.
Cuando la isquemia es leve o moderada se ven afectados los territorios frontera vasculares.
Si es severa,
se afecta la sustancia gris: ganglios basales,
tálamos,
córtex cerebral – especialmente sensitivo-motor y visual-,
cerebelo e hipocampo.
En TC se puede ver edema difuso del parénquima cerebral,
con colapso de las cisternas basales,
pérdida de la diferenciación córtico-subcortical y disminución de la atenuación de los ganglios basales.
En RM las secuencias de difusión detectan de forma más precoz el daño,
observándose restricción en los hemisferios cerebelosos,
ganglios basales y cortex cerebral,
pudiendo observarse también afectación de los tálamos,
troncoencéfalo o hipocampo.
FIGURA 11 y 12.
2.6 Alteraciones del metabolismo del calcio.
Cuando se encuentran calcificaciones densas en ganglios basales,
núcleo dentado,
tálamos o sustancia blanca subcortical hay que incluir como posibles diagnósticos el hipoparatiroidismo o pseudohipoparatiroidismo,
que pueden confirmarse midiendo los valores séricos de calcio,
fósforo y hormona paratiroidea,
e incluso enfermedades poco frecuentes como la enfermedad de Fahr,
una entidad rara que se caracteriza por el depósito de calcio y otros minerales en los ganglios basales,
tálamos,
núcleos dentados y centros semiovales en ausencia de hipoparatiroidismo.
FIGURA 13.
2.7.Aciduria glutárica TIPO I.
La aciduria glutárica tipo I es una aciduria orgánica rara.
Los pacientes no tratados desarrollan característicamente distonía durante la infancia que resulta en una alta morbilidad y mortalidad.
Está causada por la deficiencia hereditaria de glutaril-CoA deshidrogenasa,
que participa en las rutas catabólicas dela L-lisina,
L-hidroxilisina y L-triptófano.
Este defecto da lugar a niveles elevados de ácido glutárico,
ácido 3-hidroxiglutárico,
ácido glutacónico,
y glutarilcarnitina que pueden ser detectados por diferentes pruebas analítica.
El TC puede mostrar atrofia frontotemporal precoz con espacios subaracnoideos pretemporales aumentados de tamaño y cisuras de Silvio con morfología en “alas de murciélago”.
También puede verse hipodensidad en núcleo lenticular y en la sustancia blanca,
dilatación ventricular,
atrofia cerebral generalizada e hidrocefalia comunicante.La RM es la técnica de elección para valorar a los niños con esta patología.
Se observa atrofia o hipoplasia de las regiones frontotemporales de los hemisferios cerebrales,
aumento de los espacios subaracnoideos pretemporales de la fosa craneal media y dilataciones quísticas de la cisura de Silvio como hallazgos precoces.
Tras una descompensación aguda o una larga evolución la neurotoxicidad sobre los ganglios basales se vuelve evidente.
En el episodio agudo se puede observar edema en putamen y caudado que se manifiesta como hiperintensidad de señal en secuencias T2.
La restricción de la difusión refleja edema citotóxico y la alteración del metabolismo oxidativo.
Con el tiempo,
se produce pérdida neuronal y astrogliosis que dan lugar a la atrofia del caudado y el putamen ,
por lo que persiste la hiperintensidad en secuencias T2.
Otros hallazgos adicionales incluyen hiperintensidad T2 en núcleo dentado y sustancia blanca por neurotoxicidad metabólica y alteración de la mielinización.
Cuando la enfermedad progresa la atrofia cerebral,
la dilatación ventricular y la atrofia de los ganglios basales se hace más evidente.
Se ha demostrado que en la mayoría de los pacientes diagnosticados neonatalmente la lesión estriatal puede prevenirse mediante el tratamiento combinado metabólico.
FIGURA 14
-3.ENVENENAMIENTO POR TÓXICOS:
Este tipo de sustancias afectan a los ganglios basales por su elevada actividad metabólica,
pero pueden asociar alteración de otras estructuras cerebrales. El diagnóstico precisa analítica y detección de tóxicos y la evaluación radiológica se utiliza para determinar el daño cerebral.
3.1 Metanol:
La intoxicación por metanol sucede en intentos de suicidio o tras una injesta accidental,
y la clínica se caracteriza por asociar neuritis óptica,
somnolencia,
convulsiones y coma.
En casos raros,
se ha conseguido una recuperación completa si se instaura tratamiento rápido,
pero normalmente quedan secuelas en función de la cantidad de alcohol ingerida (más frecuentemente ceguera).
Los hallazgos característicos de este tipo de intoxicación incluyen neuropatía óptica y necrosis hemorrágica y no hemorrágica de putámenes.
Además pueden aparecer lesiones sustancia blanca profunda y periférica,
necrosis simétrica y bilateral del tegmento pontino y de los nervios ópticos.
En RM se observan lesiones hiperintensas en T2 e hipointensas en T1 en ambos putámenes asociadas o no a edema de sustancia blanca.
FIGURA 15 y 16.
3.2.Monóxido de carbono:
Es la causa más frecuente de intoxicación accidental en Europa y EEUU.
La clínica es muy variable pero con frecuencia los pacientes acuden a los servicios de urgencias con disminución del nivel de conciencia o en coma.
La intoxicación por monóxido de carbono suele afectar al núcleo pálido,
aunque puede también implicar a otros ganglios basales,
sustancia blanca,
córtex,
troncoencéfalo y cerebelo.
En RM se observa prolongación de la señal T2 en ganglios basales con restricción en la difusión en fase aguda.
Además,
posteriormente puede aparecer leucoencefalopatía retardada e hiperintensidad de señal en globos pálidos en T1.
- 4.
ENFERMEDADES NEURODEGENERATIVAS:
4.1 Neurodegeneración con acúmulo de hierro cerebral.
Patología caracterizada por la degeneración cerebral con acúmulo excesivo de hierro en los ganglios basales. La clínica incluye síntomas piramidales y extrapiramidales,
disartria y distonia.
Existen dos categorías clínicas dentro de este grupo: la clásica,
de comienzo precoz y con un curso rápidamente progresivo y la forma atípica,
de comienzo tardío y de lenta progresión.
En la forma clásica y en un tercio de la atípica se observa mutación del gen PANK 2.
En estos pacientes se observa hipointensidad en núcleos pálidos por acúmulo de hierro.
Además,
en aquellos con alteración del gen PANK2 es característico el signo del “ojo de tigre”,
con hiperintensidad de señal central rodeado de una zona hipointensa en los núcleos pálidos.
FIGURA 12.
- 5.
ALTERACIONES VASCULARES:
5.1 Oclusión arterial:
La oclusión de la porción rostral de la arteria basilar puede dar lugar a infartos bilaterales de los tálamos.
La clínica típica consiste en agitación,
obnubulación o coma,
disfunciones de memoria,
alteraciones oculares y de comportamiento.
En RM aparecen como lesiones hiperintensas en T2 y con restricción de la difusión.
Suele acompañarse de afectación del mesencéfalo y porciones de los lóbulos occipital y temporal (ACP) o del cerebelo (ramas del sistema vertebrobasilar).
FIGURA 17.
Una causa rara de infartos talámicos bilaterales es la oclusión de la arteria de Percheron,
un tronco común que se origina de la primera porción de la ACP.
5.2 Trombosis cerebral venosa profunda:
Entidad asociada a estados de hipercoagulabilidad (embarazo o puerperio,
ACOS,
vasculitis,
infecciones sistémicas o intracraneales).
Clinicamente cursa con dolor de cabeza,
náuseas,
vómitos,
convulsiones y alteración del estado mental.
Suelen asociarse a trombosis de senos venosos durales superficiales,
aunque existen casos en los que pueden aparecer aisladamente.
En RM se observan hiperintensidades en T2 debido a la hipertensión venosa y el edema cerebral,
que afecta al tálamo,
y con frecuencia la cápsula interna,
ganglios basales y sustancia blanca profunda.
La conversión hemorrágica hace que disminuya la señal en todas las secuencias,
especialmente EG.
- 6.
PATOLOGÍA INFECCIOSA:
6.1 Creutzfeldt-Jakob:
Se trata de una alteración neurodegenerativa causada por priones.
Existen varias formas: esporádica (la más frecuente),
familiar,
yatrogénica y una variante (la relacionada con la encefalopatía bovina espongiforme).
Clínicamente cursan con demencia rápidamente progresiva,
myoclonus y disfunción neurológica multifocal.
La degeneración neuronal espongiforme condiciona restricción en secuencias de difusión,
por lo que esta técnica es más sensible que los hallazgos en secuencias T2,
especialmente en las lesiones corticales.
Sin embargo,
a pesar de su creciente importancia en el diagnóstico de la patología,
la difusión aún no forma parte de los criterios diagnósticos de la forma esporádica.
Se observa afectación del cortex cerebral y de los ganglios basales.
La forma variante,
asociada con la encefalopatía espongiforme,
muestra lesiones bilaterales en el núcleo pulvinar del tálamo (signo del pulvinar o “hockey stick sign”).
6.2.Toxoplasmosis:
Infección oportunista por Toxoplasma gondii.
Cuando afecta al SNC cursa con fiebre,
dolor de cabeza,
confusión,
defectos neurológicos focales,
convulsiones y progresión a coma.
En imagen la toxoplasmosis se manifiesta como lesiones focales múltiples en los ganglios basales y en la unión sustancia gris-sustancia blanca de los lóbulos cerebrales.
En secuencias T2 las lesiones son típicamente hipo-isointensas,
normalmente con efecto de masa y edema vasogénico.
Las lesiones hemorrágicas pueden aparecer como hiperintensas en T1 e hipointensas en EG.
Tras la administración de contraste,
se observa realce nodular o en anillo.
La apariencia de la toxoplasmosis en RM en individuos con VIH/SIDA puede ser similar a la del linfoma del SNC.
En ocasiones se observa una toxoplasmosis hemorrágica,
un hallazgo que puede ayudarnos a diferenciarla del linfoma,
que no sangra antes del tratamiento.
La utilización de espectroscopia (que muestra picos de colina en casos de linfoma frente a la de la toxoplasmosis que muestra picos de lípidos y lactatos) puede ser útil para el diagnóstico diferencial.
FIGURA 18.
6.3.
Linfoma cerebral primario SNC:
El linfoma cerebral primario con frecuencia afecta a la sustancia blanca periventricular,
cuerpo calloso y ganglios basales. La presencia de múltiples lesiones y la afectación de los ganglios basales en más común en pacientes con VIH-SIDA,
y pueden simular una toxoplasmosis.
Se pueden distinguir por la localización periventricular,
la diseminación subependimaria y los picos de colina en la espectroscopia,
propios del linfoma.
Aparecen como lesiones hiperdensas en TC y son iso-hipointensas respecto a la sustancia gris en T2.
Las lesiones sólidas con un realce homogéneo son típicas en pacientes inmunocompetentes,
mientras que las lesiones con captación periférica y necrosis central se dan en sujetos con SIDA.
6.4.
Metástasis:
Aparecen como lesiones intraparenquimatosas múltiples que afectan con mayor frecuencia a la unión cortico-subcortical y los ganglios de la base.
Realzan con contraste, presentan grados variables de necrosis central en función del tamaño y edema perilesional en mayor o menor medida.
El diagnóstico diferencial debe hacerse con el glioblastoma multiforme cuando se trata de una lesión única.
Sin embargo,
este diagnóstico diferencial es relativamente sencillo cuando se identifican lesiones múltiples en pacientes con tumor extracraneal primario conocido.
FIGURA 19.
- 7.OTRAS:
7.1.Neurofibromatosis tipo I:
La neurofibromatosis tipo I (NF-I) es la facomatosis pediátrica más común.
La NF-Ise considera en un individuo con dos de los siguientes criterios diagnósticos: historia familiar de NF-I,
6 o más manchas “café con leche” cutáneas,
presencia de neurofibromas cutáneos,
presencia de un neurofibroma plexiforme,
pecas en la región axilar o inguinal (signo de Crowe),
nódulos pigmentados en el iris (nódulos de Lisch),
anomalías esqueléticas (curvatura de las piernas,
escoliosis,
adelgazamiento de la tíbia) o glioma del nervio óptico.
En el SNC de estos pacientes aparecen anomalías típicas en la intensidad de señal denominadas “objetos brillantes no identificados”.
Son lesiones asintomáticas que se han relacionado con hamartomas o cambios espongióticos.
En RM aparecen como áreas focales de aumento de señal en T2 a menudo con acortamiento de T1.
Se ha publicado que el globo pálido es uno de los lugares más frecuentemente afectados,
aunque también se puede afectar troncoencéfalo y cerebelo.
No tienen efecto de masa,
no se asocian con edema perilesional y no realzan tras la administración de contraste.
Se deben distinguir de los gliomas con por sus altos índices de: N-acetilaspartato/colina,
N-acetilaspartato/creatina y Creatina/colina.
En lesiones dudosas es recomendable realizar seguimiento con RM con contraste y espectroscopia.
FIGURA 20.