RECURRENCIA LOCAL
La recaida bioquímica a los 5 años ocurre en el 30-50% de los pacientes tratados con radioterapia.
El manejo de estos pacientes es complicado ya que una nueva dosis de radiación es arriesgada y se puden ocasionar daños importantes a la uretra,
vejiga o recto.
La terapia hormonal controla el tumor pero durante un tiempo limitado y la cirugía de rescate puede aumentar la supervivencia libre de enfermedad pero no se realiza de forma rutinaria.
El mejor indicador del estado de la enfermedad es el PSA,
pero no distingue entre recidiva local o a distancia.
Un diagnóstico temprano de la recidiva del cáncer de próstata y un correcto estadiaje del mismo son factores importantes a la hora de decidir una segunda línea de tratamiento tras la radioterapia.
Diagnóstico de recurrencia local
El diagnóstico de recurrencia local depende del tipo de tratamiento primario recibido.
Los 2 tipos de tratamiento posible son el quirúrgico y el no quirúrgico,
ambos con resultados similares.
El tratamiento quirúrgico consiste en la prostatectomia radical.
La referencia del tratamiento no quirúrgico es la radiación externa de alta dosis y la braquiterapia,
prefiriendo esta última para tumores menos agresivos o con una categoria T menor.
El diagnóstico de recurrencia local se basa en el comportamiento del PSA.
Tras la prostatectomía radical el nivel de PSA deberia ser indetectable.
Al existir producción de PSA extraprostática como en las células epiteliales de la traquea,
tiroides,
glándula mamarias y salivares,
yeyuno,
ileon,
epidídimo,
epidermis y páncreas,
se considera un valor normal de PSA tras la prostatectomía aquel entre 0,2 y 0,3 ng/ml.
Valores superiores indican recaida bioquímica.
Si la recaida se debe a recurrencia local en el lecho prostático o a metástasis se correlaciona con la cinética del PSA como el tiempo de doblaje de PSA.
Es infrecuente que la recaida bioquímica se acompañe de recidiva clinicamente evidente.
Por ello no se recomienda la biopsia sistemática del lecho de prostatectomía.
La recaida bioquímica tras el tratamiento no quirúrgico (radioterapia,
HIFU,
crioterapia y terapia fotodinámica) se define según los criterios del Houston que es un nivel de PSA nadir + 2 ng/ml. Hay que tener en cuenta la existencia de los llamados rebotes de PSA que no se relacionan con verdaderas racaidas bioquímicas y que pueden ocurrir especialmente tras braquiterapia y radiación externa de alta dosis.
Para hablar de recaida se debe confirmar la elevación del PSA en exámenes seriados.
También aquí es importante el tiempo de doblaje del PSA como marcador de recidiva ya que estos procedimientos producen fibrosis de la zona tratada y dificulta la interpretación del tacto rectal.
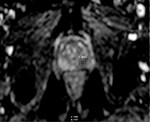
UTILIDAD DE LA RM
SECUENCIAS POTENCIADAS EN T2
Los cambios morfológicos en la próstata tras el tratamiento con radioterapia (externa y braquiterapia) incluyen inflamación,
atrofia glandular,
fibrosis y disminución de tamaño.
Estos cambios se traducen en una reducción de señal difusa en el parénquima y pérdida de la anatomía zonal normal,
lo que dificulta la distinción entre recidiva y el tejido irradiado normal.
Se sospecha recidiva en T2 ante una hipointensisdad focal o nódulo hipointenso en la zona periférica.
La sensibilidad y la especificidad de las secuencias potenciadas en T2 para la detección de recidiva en la próstata radiada son bajas,
S (26-44%) y E (64-86%) por lo que deben acompañarse de técnicas adicionales,
especialmente la espectroscopia por RM y los estudios dinámicos con contraste.
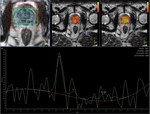
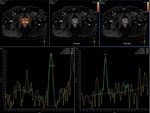
ESPECTROSCOPIA
En la próstata sin tratar la detección del cáncer de próstata se basa en el aumento de la ratio colina mas creatina respecto a citrato ([cho + cr]/cit) en uno o en múltiples voxels del parémquima prostático.
La colina y el citrato son los 2 metabolitos fundamentales en este estudio.
La colina participa en la síntesis y degradación de membranas y se acumula en las áreas malignas.
El citrato se secreta activamente al lumen de los ductos de la glándula normal pero no asi en el tejido neoplásico que pierde esta propiedad.
Tras la radioterapia la reparación proliferativa del parénquima prostático tiende a la conversión del metabolismo desde uno productor de citrato a uno citrato oxidativo.
Se produce además un incremento de la demanda de colina necesaria para síntesis y degradación de menbranas.
Como resultado los niveles de citrato se reducen tanto en las biopsias de tejido maligno como benigno y los niveles de colina aumentan.
Por consiguiente el fondo metabólico normal desaparece y esto conlleva que los criterios metabólicos para diferenciar entre áreas benignas y malignas no esten del todo establecidos.
Pucar et al usaron una ratio (cho+cr)/cit > 0,5 y encontraron un área bajo la curva de 0,88 para la discriminación entre benigno y maligno tras la radioterapia externa.
También era positivo si se detectaba colina y el citrato estaba ausente.
El método usado por Westphalen et al para el diagnóstico de recidiva local por espectrosopia combinado con las secuencias anatómicas en T2 consigue un área bajo la curva de 0.79.
El estudio se consideraba positivo si en 3 o mas vóxels contiguos se detectan niveles elevados de colina y no se detecta citrato.
Si los niveles de creatina son detectables se considera una ratio colina/creatina elevada si es mayor de 1,5 a 1.
Si la creatina no es detectable se utiliza el ruido de fondo con una valor positivo si la ratio colina/ruido de fondo es superior a 5 a 1.
Coakley et al usaron la elevacíón de la colina respecto al citrato (si era detectable) o respecto al ruido de fondo ( si la creatina era indetectable) y consiguieron un area bajo la curva de 0,81 para la detección de cáncer.
La atrofia metabólica,
definida como la ausencia de picos metabólicos de colina y citrato (ratio de metabolito/ruido < 5 a 1.) se relaciona con ausencia de recurrencia local.
Esto puede ser de particular valor en los casos de rebote de PSA para tranquilizar al paciente y puede ser un criterio temprano de control tras la braquiterapia.
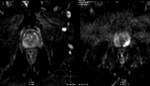
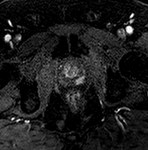
DIFUSION
Se trata de una técnica en la que se detectan variaciones en el movimiento browniano de las moléculas de agua y se cuantifican con el coeficiente de difusión atenuado (ADC).
LA difusión del agua en los tejidos biológicos se correlaciona inversamente con la celularidad y con la integridad de las membranas.
Los tumores malignos presentan una mayor densidad celular y mas membranas tanto intercelulares como intracelulares que restringen el movimiento de las moléculas de agua,
lo que se traduce en una valor bajo de ADC.
Existen pocos estudios que valoren en uso de la difusión en la recidiva tras radioterapia pero se encuentra que la región donde se localiza la recidiva presenta un valor ADC inferior al tejido irradiado que se ecuentra a su alrededor.
Presenta una sensibilidad del 49% y una especificicad del 93%.
Kim et al usan como criterio diagnóstico de la recidiva del cancer de próstata tratado con radiación externa la presencia de hiperintensidad focal en la difusión con valor b= 1000 s/mm2,
que presenta baja señal respecto al resto del tejido de la zona periférica en el mapa ADC y que tiene un tamaño superior a 5 mm de diámetro transverso máximo.
El área bajo la curva con este método es de 0.78 y no existen diferencias significativas entre la difusión aislada o combinada con el estudio dinámico y el T2,
aunque los resultados son ligeramente superiores en el estudio combinado por lo que es el recomendado.
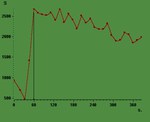
DINAMICO CON CONTRASTE
Es una adquisición del volumen prostático de forma repetida antes y tras la administración de contraste ev.
Se basa en la neoangiogénesis que acompaña al cáncer.
Se usan parámetros semicuantitativos como el realce máximo,
tiempo hasta el pico,
curva de inicio de realce y curva de lavado y otros cuantitativos como el paso de contraste desde el espacio vascular al extravascular (K trans),
el espacio extravascular extracelular (Ve) y la relación entre en el espacio extracelular y el plasma (Kep).
En paciente no tratados el Ca de próstata se asocia con un pico de realce mayor y mas rápido,
así como un rápido lavado y unas Ktrans,
K ep y Ve mayores.
La mayoria de las recurrencias ocurren en el sitio del tumor primario.
Se reconocen como áreas de realce precoz que se diferencian claramente del tejido circundante (con daño vascular y fibrosis) y que por tanto no realza.
Así,
aumenta la S y la E sobre las secuencias T2 aisladas hasta el 74% y 86%.