El colangiocarcinoma intrahepático,
también llamado periférico es un adenocarcinoma que se origina en el epitelio biliar ductal distal a las ramas de segundo orden.
Se revisan retrospectivamente todos los colangiocarcinomas intrahepáticos con diagnóstico anatomopatológico probado,
que han sido diagnosticados en nuestro Hospital desde Enero 2007 hasta Septiembre de 2011,
con un total de 74 pacientes.
Se seleccionan los 13 pacientes que han sido sometidos a ecografía con contraste (CEUS) conjuntamente con tomografía axial computarizada (TAC),
que representan el 17% del total.
Durante la exploración ecográfica se han registrado en vídeo las imágenes de cada colangiocarcinoma en fase arterial,
venosa y tardía,
durante un tiempo máximo de 6 minutos.
Se utiliza un software específico para estudios con contraste ecográfico que permiten un bajo índice mecánico.
Se debe obtener en todo momento una imagen mixta,
en la que se pueda ver al mismo tiempo el realce de la lesión y el realce del parénquima sano adyacente.
En el estudio TAC se ha realizado adquisición de imágenes en fases basal, arterial y portal.
Sólo se hace fase diferida en algunos casos,
por lo que no se evalúa en este estudio.
Se inyectan aproximadamente 100 cc de contraste yodado en embolada.
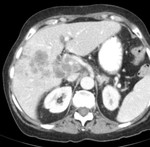
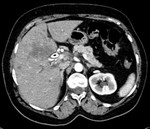
En un primer momento se determina la existencia de hallazgos morfológicos en TAC y ecografía en modo B propios del colangiocarcinoma.
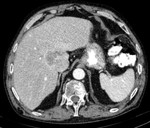
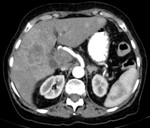
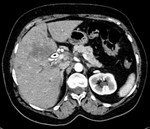
El hallazgo más común en TAC es el hallazgo de una masa sólida focal grande,
con un borde irregular polilobulado y nódulos satélites.
El tamaño medio en nuestra serie es de 7,2 cm.
Presenta un tamaño superior a los 5 cm el 76,9% (10/13).
Cuando se diagnostican con este tamaño es frecuente encontrar nódulos periféricos en el 69,2% (9/13),
bien confluentes (multifocalidad) o bien en otros segmentos (multicentricidad).
Los colangiocarcinomas intrahepáticos de menos de 5 cm representan el 23% (3/13) y suelen ser solitarios.
Pensamos que las lesiones de gran tamaño pueden formarse a partir de nódulos agrupados confluentes o conglomerados (multifocalidad) que terminan por fusionarse en una gran masa a medida que van creciendo,
o menos probablemente por un foco único que se desarrolla progresivamente.
A medida que la lesión principal crece y toma un tamaño suficiente,
comienza la aparición de nódulos distantes (multicentricidad).
Entre los hallazgos secundarios propios del colangiocarcinoma que encontramos en la literatura se encuentra la dilatación biliar periférica distal a la masa,
los cálculos y la retracción de la cápsula hepática adyacente.
En nuestro estudio solamente hemos encontrado dilatación de vía biliar periférica en el 23% (3/13) pacientes,
y ninguno de los otros signos en ningún paciente,
por lo que pensamos que los hallazgos en modo B son menos frecuentes de lo que se piensa,
y en cualquier caso inespecíficos,
porque pueden orientar el diagnóstico hacia un tumor de Klastkin en vez de hacia un colangiocarcinoma intrahepático de rama segmentaria distal.
Pensamos que el mecanismo de dilatación de vía biliar es por compresión/infiltración de una rama central cuando el tumor principal se sitúa cerca del hilio hepático,
más que por ectasia distal a la masa tumoral.
En un segundo tiempo se analiza el patrón de captación de contraste ecográfico o yodado en fase arterial y se clasifica en cuatro tipos:
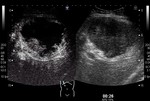
Tipo I: Hipercaptación periférica irregular en anillo.
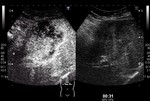
Tipo II: Hipercaptación difusa heterogénea.
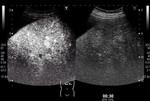
Tipo III: Hipercaptación difusa homogénea.
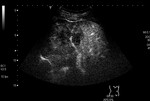
Tipo IV: Hipocaptación difusa heterogénea.
La CEUS tiene la ventaja de caracterizar la captación y el lavado de contraste durante 6 minutos seguidos mediante el estudio del nódulo dominante.
Por otra parte tiene la desventaja de detectar con dificultad lesiones profundas de pequeño tamaño,
o localizadas en áreas de difícil acceso como el segmento VII,
o en áreas ocultas por interposición de gas.
La TAC tiene la ventaja de detectar todas las lesiones focales,
pero la desventaja de no detectar captaciones precoces con lavado rápido,
lo que limita su sensibilidad.
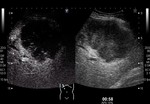
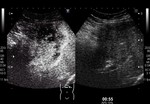
Mostramos varios pacientes con patrones de captación arterial en CEUS tipo I (Fig 1),
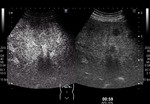
tipo II (Fig 2),
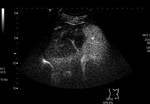
tipo III (Fig 3) y tipo 4 (Fig 4).
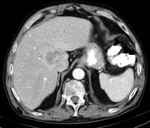
También se exponen ejemplos de TAC de otros pacientes con patrones de captación arterial tipo I (Fig 5),
tipo II (Fig 6) y tipo IV (Fig 7).
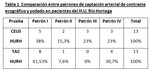
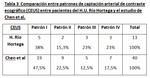
En primer lugar se analizan los porcentajes de cada patrón de captación arterial en ecografía y en TAC por separado y se comparan entre ellos (Tabla 1).
Se determina que el patrón tipo I es el más frecuente en ambas técnicas,
aunque más marcadamente en TAC.
Los patrones II y III son los menos frecuentes en nuestra serie,
no encontrándose ningún patrón tipo III en TAC.
Llama la atención que los patrones tipo II y III son más frecuentes en CEUS que en TAC.
La falta de patrón tipo III en TAC podría explicarse porque los estudios de TAC se hacen con un retraso de 35 segundos,
justo cuando la lesión ya habría comenzado a lavar y se clasificaría como patrón II o IV,
mientras que en CEUS se registra como homogénea a los 30 segundos y se registra como patrón III.
La baja frecuencia del patrón tipo II en TAC podría ser debido a que las lesiones de nuestro estudio con este patrón se comportan realmente como un conglomerado de nódulos independientes con patrón tipo I cada nódulo,
y ello induce a clasificarlas como patrón I.
Los patrones tipo I y IV son los más frecuentes tanto en TAC como en CEUS,
siempre que los analicemos de forma grupal.
Pero cuando correlacionamos el patrón arterial en CEUS y TAC caso por caso,
en ningún paciente hemos encontrado coincidencia entre el patrón de TAC y el patrón de CEUS.
Por el momento no encontramos una explicación a este hallazgo,
aunque quizá tenga que ver el tamaño de nuestro estudio,
o cuestiones que afectan a la perfusión tisular y a la farmacocinética de cada tipo de contraste.
En este trabajo también se estudia el patrón de captación de contraste ecográfico y yodado en fase portal,
clasificándolo como hipercaptante si mantiene las áreas de hiperrealce vistas en fase arterial,
o hipocaptante si no muestra ningún realce mayor que el parénquima sano.
Mostramos las fases portales en CEUS a los 50-70 segundos,
correspondientes a los pacientes con los patrones de captación arterial vistos anteriormente tipo I (Fig 8),
tipo II (Fig 9),
tipo III (Fig 10) y tipo 4 (Fig 11).
También se exponen las fases portales en TAC,
correspondientes a los pacientes de los patrones de captación arterial vistos anteriormente tipo I (Fig 12),
tipo II (Fig 13) y tipo IV (Fig 14).
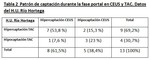
Se obtienen los siguientes resultados (Tabla 2).
Nuestros resultados indican que en TAC es más frecuente la hipercaptación que la hipocaptación en fase portal.
Todas las lesiones de nuestro estudio que muestran hipercaptación en fase arterial (Patrones I y II: 9/13),
la mantienen en fase portal,
mientras que todas las hipocaptantes en fase arterial (Patrón tipo IV: 4/13),
se mantienen hipocaptantes en fase portal.
Mediante CEUS,
también obtenemos que el patrón hipercaptante es más frecuente que el hipocaptante en fase portal.
Todas las lesiones de nuestro estudio que muestran hipercaptación en fase arterial (Patrones I,
II y III: 8/13),
la mantienen en fase portal,
mientras que todas las hipocaptantes en fase arterial (Patrón tipo IV: 5/13),
se mantienen hipocaptantes en fase portal.
La fase final del estudio consiste en buscar coincidencias con los datos publicados por el estudio de Chen et al. “Enhancement patterns of intrahepatic cholangiocarcinoma: Comparison between contrast-enhanced ultrasound and contrast enhanced CT” BJR 81 (2008),
881-889.
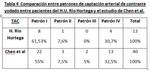
Comparamos los patrones de captación arterial de CEUS y TAC por separado (Tabla 3 y 4). El patrón tipo I es el más frecuente en nuestra serie y en la de Chen et al,
tanto cuando se emplea CEUS como TAC,
manteniéndose el resto de los patrones con unos porcentajes parecidos.
No hemos hallado ningún patrón tipo III de TAC en nuestro estudio,
siendo éste el menos frecuente en el de Chen et al.
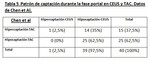
Al comparar el grado de realce en fase portal de TAC (Tablas 2 y 5),
observamos que en nuestro estudio es más frecuente el hiperrealce (69,2%) que el hiporrealce (30,7%),
mientras que en el estudio de Chen et al es a la inversa,
es más frecuente el hiporrealce (62,5%) que el hiperrealce (37,5%).
Del mismo modo,
con CEUS también constatamos que la fase portal nuestro estudio muestra unos porcentajes mayores de hiperrealce (61,5%) que de hiporrealce (38,4%),
también justo a la inversa que Chen et al,
donde el hiperrealce es (2,5%) y el hiporrealce es (97,5%).
Probablemente estos hallazgos sean debidos a que nosotros consideramos hiperrealce en fase portal al hiperrealce que se mantiene desde la fase arterial,
y quizá Chen et al evalúe la lesión en su conjunto,
pero este dato lo desconocemos ya que en el artículo de Chen et al no queda lo suficientemente claro.
En nuestro estudio el porcentaje de aciertos antes del diagnóstico histológico debe desglosarse según se haya realizado CEUS o TAC.
En la CEUS se hizo el diagnóstico correcto en 9/13 casos (69,2%).
Los errores fueron debidos a que el patrón de captación tipo III (3 casos) se confundió con hepatocarcinoma,
y un caso con patrón tipo I se dio de hemangioma cavernoso atípico.
Mediante TAC el porcentaje de aciertos fue menor 7/13 (53 %) ya que 5 colangiocarcinomas multicéntricos fueron diagnosticados de metástasis,
y otro caso fue diagnosticado como un hemangioma atípico.
Pensamos que la ecografía falla menos porque estudia sólo el nódulo dominante a lo largo de 6 minutos seguidos desde el inicio de la captación,
y que el TAC falla más porque la multicentricidad de estas lesiones es frecuente 69,2% (9/13),
y tiende a diagnosticarse como metástasis.
Entre las limitaciones del estudio hay que destacar que nuestra serie es pequeña,
ya que sólo tenemos 13 pacientes con estudio conjunto de CEUS y TAC de un total de 74 pacientes (17%).
En el resto de los casos no se realizó CEUS,
o se realizó el diagnóstico solamente con resonancia magnética o TAC.
Por otra parte,
los radiólogos que realizan la CEUS no son los mismos que realizan la TAC,
lo que puede inducir otros sesgos.
Por esta razón debe estandarizarse el manejo diagnóstico,
realizando protocolos que incluyan CEUS y TAC a todas las lesiones sospechosas de colangiocarcinoma,
y además que sean diagnosticadas por los mismos radiólogos.
Otra limitación es que comparamos nuestro estudio de 13 pacientes con otro de 40 pacientes (Chen et al).
Aún así,
los resultados de los patrones de captación en fase arterial tanto en CEUS como en TAC son parecidos.
Las diferencias encontradas en fase portal podrían ser debidas a un tamaño pequeño de nuestro estudio,
o al concepto de hipercaptación portal ya explicado anteriormente.
Otra cuestión a tener en cuenta es cómo clasificar los nódulos confluentes que forman un conglomerado heterogéneo,
y diferenciarlo de las lesiones únicas heterogéneas,
por lo que sería recomendable revisar los patrones de captación ya establecidos,
y ver si es necesaria la creación de un nuevo patrón.
Otro tema a considerar,
es el hecho de que ni nuestros estudios TAC,
ni los de Chen et al recogen datos de realce en fase diferida,
por lo que sería interesante confirmar si existe realce mantenido en esta fase,
como se ha descrito por otros autores en TAC y RM por ser un tipo de tumor con mucha fibrosis.