INTRODUCCIÓN
El término acuñado por la Organización Mundial de la Salud (OMS) para designar estos tumores es de fibromatosis tipo desmoide (1).
El témino desmoide viene del griego (banda o tendón),
y hace referencia a la consistencia en forma de bandas o tendones de este tipo de tumores (2,3).
Constituyen un amplio espectro de neoplasias fibroblásticas /miofibroblásticas con origen en los tejidos blandos en localización profunda,
con similar apariencia patológica y comportamiento biológico variable (4),
intermedio entre las lesiones fibrosas benignas y el fibrosarcoma (2).
Se caracterizan por presentar crecimiento inflitrativo y tendencia a la recurrencia local pero con incapacidad para metastatizar (1),
por lo que se consideran lesiones benignas (2).
Afectan a adultos entre 25 y 35 años (5),
con discreta preponderancia femenina,
siendo más agresivos en pacientes más jóvenes y presentando mayores tasas de recurrencia (6).
CLASIFICACIÓN/LOCALIZACIÓN Y PRESENTACIÓN
En general,
las fibromatosis pueden clasificarse en función de su localización en superficiales (fasciales) y profundas (músculo-aponeuróticas),
y también en función del grupo de edad afecto (4).
Hemos centrado nuestra revisión en las fibromatosis profundas del adulto,
que a su vez pueden clasificarse de forma arbitraria (ya que su apariencia histológica es similar) en (TABLA 1):
1.- Fibromatosis extraabdominal
2.- Fibromatosis de pared abdominal
3.- Fibromatosis intraabdominal
a) Fibromatosis mesentérica
b) Fibromatosis pélvica
1.-La fibromatosis extraabdominal tiene su origen en el tejido conectivo muscular y sus aponeurosis o fascias.
Previamente esta entidad también había sido conocida como fibromatosis agresiva,
fibromatosis músculo-aponeurótica,
tumor desmoide extraabdominal (4) o fibrosarcoma bien diferenciado no metastatizante (7).
Las localizaciones más frecuentes son el hombro y la extremidad superior (28 al 33% según las series),
seguidas de la pared torácica o región paraespinal,
región glútea y extremidad inferior,
antebrazo y mano,
y cabeza y cuello (1,4,5).
Suelen presentarse como masas de localización profunda,
de crecimiento lento pero mal definidas,
generalmente indoloras.
Pueden dar síntomas adicionales como limitación de la movilidad articular y sintomatología neurológica,
aunque son menos frecuentes (4).
Generalmente son lesiones únicas,
infiltrativas,
con diámetro mayor de 5 cm.
en el momento de presentación,
aunque se han descrito lesiones síncronas multicéntricas en la misma extremidad en un 10- 15% de los casos (5,8).
En casos de fibromatosis multicéntrica,
se ha descrito displasia metafisaria,
con deformidad tipo matraz de Erlenmeyer y escasa tubulación de huesos largos,
hasta en un 19% de los casos (8,9) .
Las lesiones más agresivas generalmente se dan en pacientes menores de 20 años,
que presentan tasas de recurrencia de hasta el 87% (5).
2.-La fibromatosis de pared abdominal afecta a las estructuras musculo-aponeuróticas en esa localización,
generalmente a los músculos recto abdominal y oblicuo interno de pared abdominal anterior (1).
Es similar a la fibromatosis extraabdominal en apariencia y características histológicas,
pero se clasifica aparte por afectar a un grupo exclusivo de población: clásicamente,
a mujeres jóvenes durante o el primer año después del embarazo (7).
En ocasiones cruzan la línea media para afectar a ambos rectos abdominales,
o bien pueden presentar extensión intraabdominal (10).
3.-La fibromatosis intraabdominal es histológicamente similar a las otras fibromatosis,
pero tiene diferente localización y manifestaciones clínicas.
Incluye la fibromatosis mesentérica y la fibromatosis pélvica (de fosa ilíaca y pelvis menor).
La fibromatosis mesentérica afecta a un rango de edad amplio,
entre 14-75 años,
sin predilección de sexo o raza (11).
Aunque la mayor parte de casos son esporádicos,
algunos se asocian con la poliposis adenomatosa familiar (PAF),
epecíficamente con la variante síndrome de Gadner (5,7).
FACTORES DE RIESGO
Existen diferencias genéticas entre las fibromatosis superficiales y profundas,
posiblemente responsables del comportamiento más agresivo de estas últimas.
Se han identificado trisomías de los cromosomas 8 y 20 en muchos casos de fibromatosis profundas,
la primera podría estar asociada con un mayor riesgo de recurrencia (5),
pero no hay consenso en que constituya un factor pronóstico al diagnóstico (1).
La asociación de desmoides extra y sobre todo intraabdominales con la poliposis adenomatosa familiar (PAF) y en concreto con el síndrome de Gadner es bien conocida y ha sido descrita ampliamente en la literatura.
La PAF es una adenomatosis hereditaria colo-rectal,
de herencia autosómica dominante,
causada por una mutación en el gen supresor tumoral de la poliposis colónica adenomatosa (APC) (12).
Gadner describió en 1951 la concurrencia de PAF con manifestaciones extracolónicas de poliposis intestinal: osteomas,
quistes epidermoides y desmoides (síndrome de Gadner).
Los tumores desmoides se presentan en un 9-18% de pacientes con PAF,
en las estructuras musculo-aponeuróticas de pared abdominal particularmente cerca de cicatrices quirúrgicas,
o más frecuentemente en localización intraabdominal,
generalmente en mesenterio del intestino delgado (13).
Se han descrito mutaciones asociadas del gen APC en el cromosoma 5q21-22 (4,5,14).
Existen otros dos enfermedades raras de herencia autosómica dominante que conllevan mutaciones únicas del gen APC y se asocian con fibromatosis mesentérica: la fibromatosis familiar infiltrativa (fibromatosis mesentérica y cancer colorrectal no polipósico) y la enfermedad desmoide hereditaria (fibromatosis multifocal de los músculos paraespinales,
mamas,
occipucio,
brazos,
costillas inferiores,
pared abdominal y mesenterio) (15).
Se han descrito otros factores de riesgo para el desarrollo de fibromatosis tipo desmoide,
como antecedentes traumáticos,
cirugía previa,
embarazo y uso de anticonceptivos (6).
Igual que la fibromatosis tipo desmoide extraabdominal,
los tumores de pared abdominal muestran predilección por desarrollarse en áreas de cicatrización postquirúrgica,
particularmente en incisiones de cesáreas,
pero también se han descrito en incisiones de colostomías previas,
laparoscópicas,
y de catéteres para diálisis peritoneal,
habiéndose llegado a emplear el término “fibromatosis cicatricial” (4).
La cirugía previa es asimismo un importante factor de riesgo en el desarrollo de fibromatosis mesentérica en pacientes con PAF (15).
El 83% de pacientes con PAF y fibromatosis mesentérica tienen historia previa de cirugía abdominal,
más frecuentemente pancolectomía (16),
teniendo lugar generalmente el diagnóstico de fibromatosis mesentérica en estos pacientes dentro de los primeros 4 años tras el proceso quirúrgico (15).
Se cree que los estrógenos están implicados como factor de crecimiento (5,6),
habiéndose realizado estudios sobre la influencia de estos en el crecimiento de tumores desmoides de pared abdominal,
y la regresión de los mismos tras la menopausia u oforectomía (4).
ANATOMÍA PATOLÓGICA
Las fibromatosis de tipo desmoide se presentan como masas firmes,
sobre todo en localización extraabdominal,
hecho que puede complicar la biopsia guiada por imagen.
Macroscópicamente se componen de tejido blanco-grisáceo no encapsulado,
con apariencia firme y blanca brillante al corte recordando al tejido cicatricial (3).
Tienen márgenes espiculados infiltrativos y típicamente se adhieren a estructuras adyacentes (6).
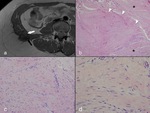
En localización extraabdominal,
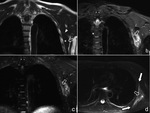
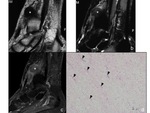
es característica la infiltración del músculo y tejido subcutáneo (Fig. 1),
pudiendo además extenderse a lo largo de los planos fasciales,
en ocasiones a gran distancia del foco tumoral primario (4).
La fibromatosis mesentérica presenta asimismo márgenes infiltrantes a nivel microscópico hacia las estructuras adyacentes,
particularmente la muscular propia del intestino delgado,
característica que se ha descrito como “melting insinuation" (11,15).
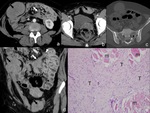
Microscópicamente,
estos tumores se componen de células elongadas de núcleo fusiforme de apariencia uniforme y fibroblastos,
generalmente formando fascículos mal definidos en un estroma colágeno conteniendo vasos prominentes en cantidad variable (Fig. 1,
Fig. 2),
algunas veces con edema perivascular (1).
Las células no tienen hipercromasia ni atipia,
la tasa de mitosis es varible (1),
generalmente baja,
y la necrosis es rara (6).
Pueden presentar colágeno tipo queloide o extensiva hialinización (1).
Algunas lesiones,
particularmente las originadas en el mesenterio o la pelvis,
presentan extensos cambios mixoides en su estroma (1),
o pueden presentar degeneración hemorrágica (4).
La activación de la cadena de la β–catenina se ha implicado en la etiopatogenia de la fibromatosis,
como resultado de mutaciones del gen APC (generalmente en conexión con la PAF o síndrome de Gadner),
o por mutaciones que hacen a la β- catenina resistente a la influencia inhibitoria de dicho gen (1,3,4) .
Ello deriva en la expresión nuclear exagerada de la proteían β-catenina,
empleada en el diagnóstico inmunohistoquímico.
La negatividad para los marcadores CD34 y CD117 permite el diagnóstico diferencial histológico de la fibromatosis mesentérica con los tumores del estroma gastrointestinal (GIST) (15).
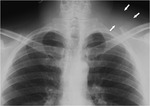
CARACTERÍSTICAS RADIOLÓGICAS
La radiografía puede revelar una masa de partes blandas en tumores de localización extraabdominal o de pared (Fig. 3).
La calcificación es infrecuente,
aunque puede existir afectación ósea adyacente en un 6-37%,
generalmente remodelación cortical sin invasión medular (2,7,8).
Los hallazgos óseos en pacientes con displasia esquelética incluyen deformidad tipo matraz de Erlenmeyer,
engrosamiento cortical,
lesiones focales radiolucentes,
islotes óseos y excrecencias óseas (9).
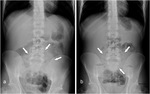
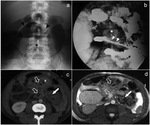
En pacientes con fibromatosis mesentérica,
la radiografía puede demostrar un efecto de masa centrado en el abdomen,
con desplazamiento de segmentos de intestino delgado adyacente (Fig. 4),
siendo menos frecuente la afectación colónica cuando el origen está en el mesocolon,
generalmente transverso (15).
Por su infiltración del intestino delgado adyacente puede ocasionar pseudooclusión u obstrucción intestinal,
formación de fístulas o perforación (Fig. 5).
La infiltración del mesenterio del intestino delgado puede resultar en ulceración mucosa.
La fibromatosis mesentérica puede llegar a rodear completamente a las asas,
generalmente causando disminución de calibre,
aunque se ha descrito patrón de dilatación luminal similar al linfoma.
El tránsito intestinal para la evaluación del intestino delgado puede revelar engrosamiento,
pérdida o distorsión de pliegues con irregularidad o uleración mucosa (15) (Fig. 5).
La ecografía permite valorar lesiones más superficiales (extraabdominales),
si bien su apariencia no es específica,
presentándose como masas de partes blandas mal definidas hipoecoicas generalmente sin realce posterior (4)(Fig. 6),
con vascularización variable en el estudio doppler (6).
Aunque la ecografía no es la técnica de elección para evaluar el mesenterio,
pueden visualizarse incidentalmente masas mesentéricas en estos pacientes como masas sólidas bien circuscritas de variable ecoestructura y homogeneidad (15).
Si bien tanto las dos técnicas mencionadas previamente como estudios de Medicina Nuclear han sido empleados en la evaluación de las fibromatosis tipo desmoide,
en la práctica la TAC y RM ,
por su capacidad multiplanar,
constituyen las técnicas de elección (6) para el estudio de las fibromatosis profundas,
permitiendo además valorar su extensión y la relación con estructuras vecinas,
la planificación preoperaoria y la detección de recidivas.
Vamos a revisar los hallazgos en TAC y RM en cada grupo:
1.FIBROMATOSIS EXTRAABDOMINAL
La TAC revela masas con atenuación variable,
generalmente similar al músculo esquelético (4,
6),
aunque pueden presentar mayor atenuación si el componente colágeno es prominente o menor atenuación en caso de contener mayor componente mixoide,
que Murphey et al.
describieron con mayor frecuencia en lesiones de pared torácica (4).
El grado de realce es variable aunque puede ser importante reflejando el hallazgo histológico de una abundante red capilar.
La RM es la modalidad óptima para evaluar este tipo de lesiones.
Generalmente se encuentran en localización intramuscular ,
y pueden ser bien delimitadas (49-54% de los casos),
rodeadas de un halo graso (signo de la “grasa escindida” o respetada) (),
o presentar márgenes irregulares infiltrativos (46-51%) (4).
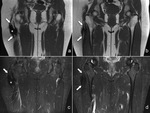
Es frecuente la extensión lineal a lo largo de planos faciales (el signo de la “cola fascial”) (Fig. 7,
Fig. 8,
Fig. 9,
Fig. 11),
que ha sido descrita hasta en un 80% de los casos (5).
La cola fascial puede ser muy prominente y extenderse a gran distancia del foco neoplásico primario,
siendo importante detectarla porque constituye una característica diagnóstica diferencial (es inusual en otros tumores),
y con vistas a la planificación quirúrgica (4).
Presentan intensidad de señal heterogénea que generalmente refleja las diferentes cantidades y distribución variable de las células de núcleo fusiforme,
colágeno extracelular y matriz mixoide (5).
Sundaram et al.
observaron lesiones con baja intensidad de señal en secuencias potenciadas T2 y las relacionaron con menor celularidad y mayor contenido colágeno (17) ( Fig. 1,
Fig. 7),
mientras que algunas series posteriores describen predomino de lesiones hiperintensas con respecto al músculo en secuencias potenciadas en T2 (2) ( Fig. 8, Fig. 9).
Igual que en las fibromatosis superficiales palmar y plantar,
se han descritos tres estadios de evolución histológica (4,
5):
1.-Lesiones más celulares con grandes espacios extracelulares y contenido relativo en colágeno menor: baja intensidad de señal en T1 y alta en T2.
2.-Aumento en la cantidad de colágeno en áreas central y periférica,
lo que aumenta la apariencia heterogénea en T2 (Fig. 10).
3.-Aumento en la composición colágena-fibrosa y disminución de celularidad: baja intensidad de señal en T1 y T2 (Fig. 11).
Se ha descrito hiperseñal T2 por tanto en tumores recurrentes (Fig. 9) o en crecimiento activo (6),
reflejando su contenido más celular.
También el contenido mixoide aumenta la señal T2.
Los estudios con largas series han demostrado que la apariencia más frecuente es intensidad de señal intermedia en secuencias potenciadas en T1 (similar al músculo),
e intermedia (menor que la de la grasa y mayor que la del músculo) en secuencias potenciadas en T2 sin saturación grasa (4,5).
La supresión grasa puede revelar mayor hiperseñal en su interior (Fig. 7).
La presencia de bandas hipointensas en T2,
que parecen corresponder a densos haces colágenos visibles histológicamente (18),
hipocelulares,
que no realzan tras la administración de contraste,
se ha descrito hasta en un 86% (5).
Se pueden ver áres de baja intensidad de señal en otras lesiones (ver sección Diagnóstico Diferencial) así que no se trata de un hallazgo específico.
No obstante,
al morfología en banda de las áres de baja señal añade especificidad al diagnóstico (4).
Las secuencias potenciadas en T2 o T1 post-contraste son óptimas para la detección de estas bandas hipointensas (Fig. 7,
Fig. 8,
Fig. 9) .
Tras la administración de contraste,
estos tumores muestran realce heterogéneo moderado o importante,
mientras que las bandas hipocelulares no realzan resultando más prominentes en el seno de la lesión.
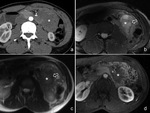
2.FIBROMATOSIS DE PARED ABDOMINAL
Los hallazgos en TAC y RM de la fibromatosis de pared abdominal,
igual que su apariencia patológica,
son idénticos a los de la fibromatosis extraabdominal.
Estas lesiones generalmente afectan al recto abdominal (Fig. 12),
o bien al oblicuo interno de pared abdominal.
La identificación de una masa de intensidad de señal baja o intermedia con extensiones lineales a lo largo de la fascia superficial en sus márgenes (signo de la cola fascial),
o presentando bandas hipointensas que no realzan tras la administración de contraste,
es casi patognomónica (4) (Fig. 13) .
Ambas técnicas de imagen,
sobre todo la RM,
son útiles en el despistaje de extensión intraabdominal y para la planificación quirúrgica (con vistas a la excisión completa).
3.FIBROMATOSIS INTRAABDOMINAL
A)Fibromatosis mesentérica
El mesenterio del intestino delgado es el lugar de origen más frecuente de la fibromatosis intraabdominal,
aunque puede originarse en otras estructuras mesentéricas como el omento,
el mesenterio ileocólico,
el mesocolon transverso o sigmoideo y el ligamento redondo (15).
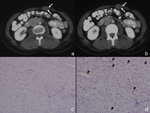
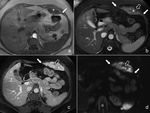
Los hallazgos en la TAC reflejan la composición histológica,
de forma análoga a la fibromatosis tipo desmoide extraabdominal.
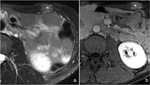
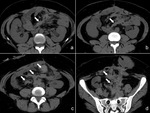
Las lesiones con estroma con alto contenido en colágeno generalmente presentan atenuación homogénea de partes blandas,
mientras que las lesiones con extroma mixoide son hipoatenuantes (15) (Fig. 14).
Algunas lesiones tienen estroma colágeno y mixoide y presentan apariencia estriada o en espiral por la alternancia de ambas (19) (Fig. 15).
Se ha decrito clásicamente que la fibromatosis mesentérica presenta escaso realce en el estudio postcontraste,
pero Levy et al describieron patrones de realce variable,
desde moderado homogéneo hasta mayor realce heterogéno,
con ausencia de realce en lesiones predominantemente mixoides (15).
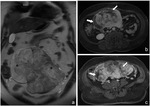
Los hallazgos en RM reflejan asimismo la abundancia de colágeno o estroma mixoide dentro de la lesión (15).
La mayor parte de las lesiones presentan intensidad de señal baja o intermedia en secuencias potenciadas en T1 e intermedia heterogénea o alta en T2 (13).
El estroma mixoide contribuye a la alta intensidad de señal,
dependiendo la relativa hiperseñal T2 del tumor del grado de celularidad y del estroma mixoide dentro de la misma (15) (Fig. 14),
más que de su contenido en colágeno (13).
El realce es asimismo variable.
Se ha descrito que hay lesiones que no realzan con el contraste yodado en la TAC pero sí lo hacen tras la administración de gadolinio en RM ,
probablemente debido a la mayor resolución espacial de la RM y a su capacidad para demostrar vascularización sutil (20).
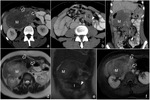
Tumores mesentéricos desmoides asociados al Se de Gadner
Al hablar sobre las características en RM de los tumores desmoides asociados a la PAF,
Azizi et al.
(13) distinguieron 2 formas de presentación:
-en forma de masa: grandes y bien definidos,
midiendo hasta 25 cm.
en el momento del diagnóstico,
comprimiendo o desplazando estructuras adyacentes.
-infiltrativos: tejido mal definido que aparece como una aumento de partes blandas espiculado en la grasa mesentérica generalmente causando angulación o espiculación de las asas intestinales adyacentes.
Ambos pueden estar presentes en el mismo paciente (13) (Fig. 15).
En pacientes con PAF,
la fibromatosis mesentérica suele presentar una apariencia similar en la TAC y RM que los casos esporádicos,
aunque es característica la presencia de varias lesiones,
generalmente de menor tamaño que en los casos esporádicos,
y habitualmente en la proximidad de las regiones quirúrgicas y anastomóticas (15).
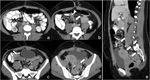
Las formas mesentéricas asociadas a la PAF se caracterizan por su naturaleza infiltrativa pudiendo ocasionar obstrucción ureteral,
de asas intestinales o lesión vascular,
representando una causa mayor de morbi-mortalidad en pacientes con PAF a los que se les ha practicado colectomía profiláctica (13).En estos pacientes,
los desmoides de pared abdominal pueden asociarse con tumores mesentéricos (13,15,20).
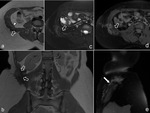
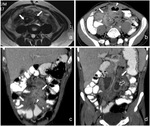
Además,
en nuestra experiencia,
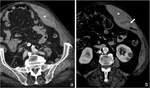
en este tipo de pacientes es más frecuente la multiplicidad de tumores de pared así como la extensión intraabdominal (Fig. 16, Fig. 17).
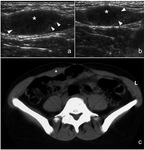
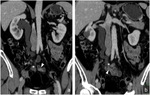
B)Fibromatosis pélvica
La fibromatosis pélvica,
igual que la retroperitoneal,
representa más frecuentemente una extensión de la fibromatosis mesentérica con márgenes difusos infiltrativos (15).
En algunos casos,
los pacientes con PAF pueden presentar una forma difusa de fibromatosis que infiltra el mesenterio,
el retroperitoneo y la pelvis (Fig. 18).
DIAGNÓSTICO DIFERENCIAL
Aunque la imagen sea sugestiva,
en todos los casos se precisa confirmación histopatológica previa al tratamiento (6).
1.FIBROMATOSIS EXTRAABDOMINAL
Diagnóstico diferencial con lesiones con áreas hipointensas: masas densamente calcificadas,
sinovitis villonodular pigmentada,
tumor de células gigantes de la vaina tendinosa,
fibrosarcoma,
sarcoma pleomórfico indiferenciado,
etc.
(4,5).
Como se describió previamente,
la morfología en banda puede añadir especificidad al diagnóstico.
2.FIBROMATOSIS DE PARED ABDOMINAL
Diagnóstico diferencial con lesiones heterogéneas en el espesor de la musculatura de pared,
especialmente hematomas de rectos abdominales en pacientes anticoagulados (Fig. 19) y depósitos metastáticos.
La historia clínica es por tanto fundamental en el diagnóstico.
3.FIBROMATOSIS INTRAABDOMINAL
En base a los hallazgos de imagen exclusivamente,
la fibromatosis mesentérica es difícil de diferenciar de neoplasias mesentéricas malignas como linfoma,
enfermedad metastásica,
o sarcomas de partes blandas con origen en mesenterio o retroperitoneo (leiomiosarcoma,
sarcoma pleomórfico indiferenciado,
etc) (Fig. 20).
Los GIST del intestino delgado,
pueden tener extenso componente mesentérico,
aunque suelen tener áreas de hemorragia o necrosis (planteando el diagnóstico diferencial con fibromatosis mesentéricas con contenido mixoide que puede ser erróneamente interpreteado como áreas de necrosis) (15).
COMPLICACIONES
Las complicaciones de los tumores desmoides son el resultado de su naturaleza agresiva,
que lleva a la compresión e invasión de las estructuras adyacentes.
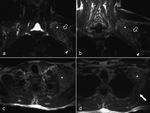
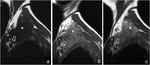
1.FIBROMATOSIS EXTRAABDOMINAL
Presentan complicaciones derivadas de su localización cerca de estructuras vitales,
sobre todo en lesiones de hombro y cuello: plexo braquial (Fig. 21),
tráquea,
vasos axilares.
Las lesiones de cabeza y cuello afectando a pacientes jóvenes (<30 años) tienen comportamiento más agresivo que en otras localizaciones y grupos de edad (4).
2.FIBROMATOSIS DE PARED ABDOMINAL
Por su localización no suelen englobar estruturas vitales,
pero imposibilita su resección con márgenes amplios manteniendo la integridad del tronco abdominal (4),
por lo que puede requerirse radioterapia adyuvante o terapia sistémica.
3.FIBROMATOSIS INTRAABDOMINAL
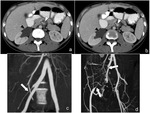
Existen complicaciones potencialmente mortales derivadas a la naturaleza infiltrativa de los tumores desmoides mesentéricos asociados a FAP (6,13,20):
- Lesiones vasculares (Fig. 22)
- Obstrucción de asas intestinales (perforación) (Fig. 23)
- Obstrucción ureteral (Fig. 18,
Fig. 22,
Fig. 24)
Los tumores desmoides representan una de las principales causas de muerte en pacientes sometidos a colectomía profiláctica (20).
MANEJO
Es necesaria una aproximación multidisciplinar ajustada a cada paciente para un manejo óptimo de estos tumores (6,
21).
El tratamiento de elección en desmoides grandes sintomáticos es la resección quirúrgica con márgenes amplios,
aunque depende en gran parte de las consideraciones anatómicas,
reservándose para pacientes en los que pueda lograrse con mínima morbilidad funcional y médica (4).
Además existen grandes tasas de recurrencia local,
con un rango variable entre el 19 y el 77% descrito en la literatura en función de la cirugía más o menos amplia practicada (4).
Se ha propuesto la observación en los casos estables y asintomáticos (22).
Los desmoides intraabdominales asociados al síndrome de Gadner requieren segumiento evolutivo estrecho clínico y por imagen si no son susceptibles de tratamiento quirúrgico.
La RM tiene valor pronóstico ya que la alta intensidad de señal T2 se ha relacionado con más rápido crecimiento (6,20) o mayor riesgo de recidiva (4).
La radioterapia postoperatoria reduce las tasas de recurrencia local,
pero sólo en caso de márgenes quirúrgicos afectos.
La radioterapia como tratamiento (asociado o no a cirugía) es efectiva,
aunque también se asocia con alta tasa de complicaciones,
debiendo valorarse su uso en los caso en que no es posible la resección quirúrgica (21).
El tratamiento sistémico,
aplicable en pacientes con contraindicaciones para la cirugía o radioterapia,
incluye los agentes citotóxicos como las antraciclinas; los agentes moleculares como el imatinib; el interferón; y el tratamiento antiestrogénico como el tamoxifeno (6),
que junto con otros tratamientos hormonales se ha empleado fundamentalmente en tumores de pared abdominal (4).
La RM puede ser útil también para determinar la respuesta a la radioterapia o la terapia sistémica.
Si la respuesta es positiva el tumor se volverá menos celular y más colágeno,
resultando en reducción de su tamaño y su señal T2 (4,
5,8) (Fig. 11).
BIBLIOGRAFÍA
1.
Fletcher CD,
Unni KK,
Mertens F.
WHO classification of tumours: Pathology and genetics of tumours of soft tissue and bone.
France: Lyon : IARC Press,
2002.; 2002.
2.
Lee JC,
Thomas JM,
Phillips S,
Fisher C,
Moskovic E.
Aggressive fibromatosis: MRI features with pathologic correlation.
AJR Am J Roentgenol 2006,
Jan;186(1):247-54.
3. Weiss,
Goldblum.
Fibromatoses.
In: Enzinger and Weiss’s soft tissue tumors.
St Louis,
Mo: Mosby; 2001.
p.
320-9.
4.
Murphey MD,
Ruble CM,
Tyszko SM,
Zbojniewicz AM,
Potter BK,
Miettinen M.
From the archives of the AFIP: Musculoskeletal fibromatoses: Radiologic-Pathologic correlation.
Radiographics 2009,
Nov;29(7):2143-73.
5.
Dinauer PA,
Brixey CJ,
Moncur JT,
Fanburg-Smith JC,
Murphey MD.
Pathologic and MR imaging features of benign fibrous soft-tissue tumors in adults.
Radiographics 2007;27(1):173-87.
6.
Shinagare AB,
Ramaiya NH,
Jagannathan JP,
Krajewski KM,
Giardino AA,
Butrynski JE,
Raut CP.
A to Z of desmoid tumors.
AJR Am J Roentgenol 2011,
Dec;197(6):W1008-14.
7.
McDonald ES,
Yi ES,
Wenger DE.
Best cases from the AFIP: Extraabdominal desmoid-type fibromatosis.
Radiographics 2008;28(3):901-6.
8.
Robbin MR,
Murphey MD,
Temple HT,
Kransdorf MJ,
Choi JJ.
Imaging of musculoskeletal fibromatosis.
Radiographics 2001;21(3):585-600.
9.
Disler DG,
Alexander AA,
Mankin HJ,
O'Connell JX,
Rosenberg AE,
Rosenthal DI.
Multicentric fibromatosis with metaphyseal dysplasia.
Radiology 1993,
May;187(2):489-92.
10.
Casillas J,
Sais GJ,
Greve JL,
Iparraguirre MC,
Morillo G.
Imaging of intra- and extraabdominal desmoid tumors.
Radiographics 1991,
Nov;11(6):959-68.
11.
Burke AP,
Sobin LH,
Shekitka KM,
Federspiel BH,
Helwig EB.
Intra-Abdominal fibromatosis.
A pathologic analysis of 130 tumors with comparison of clinical subgroups.
Am J Surg Pathol 1990,
Apr;14(4):335-41.
12.
Quyn AJ,
Steele RJ,
Carey FA,
Näthke IS.
Prognostic and therapeutic implications of apc mutations in colorectal cancer.
Surgeon 2008,
Dec;6(6):350-6.
13.
Azizi L,
Balu M,
Belkacem A,
Lewin M,
Tubiana JM,
Arrivé L.
MRI features of mesenteric desmoid tumors in familial adenomatous polyposis.
AJR Am J Roentgenol 2005,
Apr;184(4):1128-35.
14.
Wong SL.
Diagnosis and management of desmoid tumors and fibrosarcoma.
J Surg Oncol 2008,
May 1;97(6):554-8.
15.
Levy AD,
Rimola J,
Mehrotra AK,
Sobin LH.
From the archives of the AFIP: Benign fibrous tumors and tumorlike lesions of the mesentery: Radiologic-Pathologic correlation.
Radiographics 2006;26(1):245-64.
16.
Lotfi AM,
Dozois RR,
Gordon H,
Hruska LS,
Weiland LH,
Carryer PW,
Hurt RD.
Mesenteric fibromatosis complicating familial adenomatous polyposis: Predisposing factors and results of treatment.
Int J Colorectal Dis 1989;4(1):30-6.
17.
Sundaram M,
McGuire MH,
Schajowicz F.
Soft-Tissue masses: Histologic basis for decreased signal (short T2) on t2-weighted MR images.
AJR Am J Roentgenol 1987,
Jun;148(6):1247-50.
18.
Kransdorf MJ,
Jelinek JS,
Moser RP,
Utz JA,
Hudson TM,
Neal J,
Berrey BH.
Magnetic resonance appearance of fibromatosis.
A report of 14 cases and review of the literature.
Skeletal Radiol 1990;19(7):495-9.
19.
Magid D,
Fishman EK,
Jones B,
Hoover HC,
Feinstein R,
Siegelman SS.
Desmoid tumors in gardner syndrome: Use of computed tomography.
AJR Am J Roentgenol 1984,
Jun;142(6):1141-5.
20.
Healy JC,
Reznek RH,
Clark SK,
Phillips RK,
Armstrong P.
MR appearances of desmoid tumors in familial adenomatous polyposis.
AJR Am J Roentgenol 1997,
Aug;169(2):465-72.
21.
de Bree E,
Keus R,
Melissas J,
Tsiftsis D,
van Coevorden F.
Desmoid tumors: Need for an individualized approach.
Expert Rev Anticancer Ther 2009,
Apr;9(4):525-35.
22.
Fiore M,
Rimareix F,
Mariani L,
Domont J,
Collini P,
Le Péchoux C,
et al.
Desmoid-Type fibromatosis: A front-line conservative approach to select patients for surgical treatment.
Ann Surg Oncol 2009,
Sep;16(9):2587-93.