Las enfermedades intersticiales suponen un amplio grupo de entidades clĂnico patolĂłgicas,
que pueden solaparse entre sĂ.
Recientemente,
se ha observado relaciĂłn entre la apariciĂłn de ciertas afecciones del intersticio pulmonar y el consumo de tabaco.
El tabaco es capaz de inducir un estado de activación de los macrófagos y las células de Langerhans de manera dosis-dependiente,
ya que la nicotina estimula la producciĂłn por parte de los macrĂłfagos de factor estimulante de colonias granulocito-macrĂłfagos y de osteopontina,
que actĂșa como quimiotĂĄctico,
lo que produce acumulaciĂłn de macrĂłfagos y fibrosis.
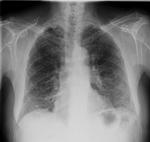
Puesto que la radiologĂa convencional aporta escasa informaciĂłn acerca del intersticio pulmonar,
es necesario realizar TC de alta resoluciĂłn para una aproximaciĂłn diagnĂłstica.
El anĂĄlisis histolĂłgico mediante biopsia pulmonar toracoscĂłpica o abierta aportan el diagnĂłstico definitivo; la biopsia transbronquial no es diagnĂłstica,
y el lavado broncoalveolar Ășnicamente puede aportar datos definitivos en el caso de la histiocitosis de cĂ©lulas de Langerhans.
La inespecificidad de los signos radiolĂłgicos hace que el abordaje de estas entidades desde la perspectiva de la anatomĂa patolĂłgica permita una mejor comprensiĂłn de las mismas,
ya que a veces se presentan de manera solapada o acompañando a otras patologĂas inducidas por el tabaco,
comola EPOCo el cĂĄncer de pulmĂłn.
Existen cinco entidades descritas en la literatura:
1) BRONQUIOLITIS RESPIRATORIA ASOCIADA AL TABACO: descrita por primera vez en 1974 como una afectaciĂłn de la pequeña vĂa debida al consumo de cigarrillos,
no fue asociada a la afectaciĂłn intersticial hasta 1984.
Aparece con frecuencia en pacientes fumadores jĂłvenes (30-40 años) coxistiendo frecuentemente con lesiones enfisematosas; generalmente es asintomĂĄtica y experimenta mejorĂa clĂnico-radiolĂłgica con el cese del tabaquismo.
Se caracteriza por la presencia de inflamación leve y macrófagos pigmentados (citoplasma amarillo-marrón) en el interior de los bronquiolos respiratorios y alvéolos colindantes,
que pueden mostrar engrosamiento parietal y metaplasia bronquiolar.
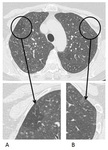
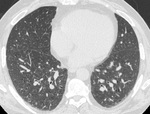
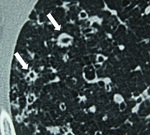
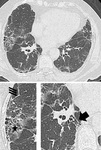
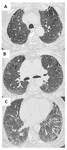
Al tratarse de un proceso bronquiolocéntrico,la TCARmostrarå engrosamiento peribronquial,
nódulos centrilobulillares y atenuación en mosaico debida a fenómenos de atrapamiento aéreo (fig 1).
El engrosamiento de septos alveolares prĂłximos al bronquiolo puede generar imĂĄgenes en vidrio deslustrado en el estudio inspiratorio,
pero no son frecuentes puesto quela BRse caracteriza por respetar el espacio alveolar distal.
Se ha descrito predominancia de los signos en lĂłbulos superiores.
2) NEUMONITIS INTERSTICIAL DESCAMATIVA: Suele aparecer en la 4ÂȘ-5ÂȘ dĂ©cadas de la vida.
Actualmente se prefiere el tĂ©rmino de neumonĂa alveolar macrofĂĄgica,
debido a que la descamaciĂłn de cĂ©lulas epiteliales no es el fenĂłmeno histolĂłgico caracterĂstico,
sino la presencia de macrĂłfagos pigmentados intraalveolares,
con una distribución no tan bronquiolocéntrica sino manera mås difusa que enla BRAT.
Este hallazgo se asocia a discreto engrosamiento de los septos interalveolares y la presencia de infiltrados linfoplasmocitarios.
Aunquela BRATyla NIDson descritas como entidades independientes,
la difĂcil diferenciaciĂłn entre las mismas hace que se consideren dos momentos de la evoluciĂłn natural de un mismo proceso histolĂłgico.
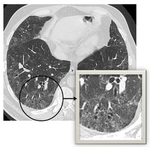
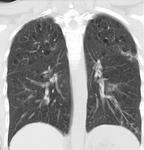
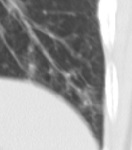
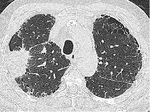
Los hallazgos en TCAR son inespecĂficos en incluyen opacidades bilaterales en vidrio deslustrado y fibrosis de predominio basal y subpleural,
mĂĄs marcados que enla BR,
debido a la extensiĂłn mĂĄs difusa de la afectaciĂłn intraalveolar (fig2).
La presencia de opacidades en vidrio deslustrado no se deben al volumen parcial generado por el engrosamiento de las paredes alveolares (intersticio intralobulillar) como ocurre en algunas afecciones intersticiales,
sino que se correlacionan directamente con la cantidad de macrófagos pigmentados en el interior de los alvéolos y los conductos alveolares.
Hay que tener en cuenta quela NIDpuede aparecer en no fumadores,
asociada a afectaciones sistémicas,
consumo de fĂĄrmacos y drogas,
infecciones,
etc.
ClĂnicamente es mĂĄs agresiva quela BR,
y es caracterĂstica la marcada reducciĂłn en la difusiĂłn de DLCO.
3) HISTIOCITOSIS DE CĂLULAS DE LANGERHANS: coexisten lesiones nodulares esclerosantes bronquiolocĂ©ntricas,
que contienen células de Langerhans e infiltrados celulares con linfocitos y macrófagos,
con ĂĄreas de pulmĂłn normal.
La enfermedad evoluciona con la apariciĂłn de fibrosis de los nĂłdulos,
que va involucrando progresivamente el pulmón adyacente y agrandando el espacio aéreo pericicatricial,
lo que da lugar a lesiones quĂsticas caracterĂsticas dela HCL.
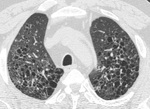
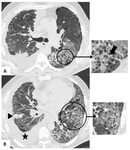
Losquistes presentan morfologĂa irregular y grosor parietal variable,
predominan en lĂłbulos superiores (figs 3,
4 y 5).
La afectaciĂłn esclerosante del bronquiolo se traduce en la apariciĂłn de nĂłdulos centrilobulillares pequeños que pueden cavitar (signo de âcheeriosâ,
fig.
6).
Es tĂpico el respeto de los ĂĄngulos costodiafragmĂĄticos.
La presencia de infiltrados celulares y fibrosis leve puede dar lugar a la apariciĂłn de opacidades en vidrio deslustrado y reticulaciĂłn; con frecuencia esta entidad coexiste con ĂĄreas de NID o BR (figs 7 y 8).
El lavado broncoalveolar es diagnóstico cuando contiene mås del 5% de células de Langerhans.
4) FIBROSIS PULMONAR IDIOPĂTICA: La relaciĂłn entrela FPIy el tabaco fue propuesta en 1969 y secundada por estudios posteriores,
sin embargo la confirmaciĂłn histolĂłgica es poco frecuente,
lo que ha dificultado establecer dicha relaciĂłn.
Aunque existe mayor prevalencia dela FPIen pacientes fumadores,
se ha observado una mayor progresiĂłn de la enfermedad en aquellos que cesan el hĂĄbito tabĂĄquico frente a los que continĂșan fumando.
HistolĂłgicamente se caracteriza por la alveolitis con aumento de la celularidad de las paredes alveolares y presencia de macrĂłfagos en su interior,
proceso inflamatorio que progresivamente conduce a la apariciĂłn de focos fibroblĂĄsticos y fibrosis avanzada en un patrĂłn de panalizaciĂłn.
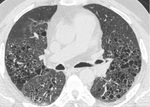
Esto se traduce en las imågenes de TCAR en opacidades reticulares periféricas y basales,
con engrosamiento septal irregular,
bronquiectasias de tracciĂłn y panalizaciĂłn,
hallazgos que predominan en regiones basales y subpleurales y que traducen un proceso fibrĂłtico irreversible en el que el volumen pulmonar se reduce inexorablemente (fig 9).
Es posible observar agudizaciones reversibles,
en las que el proceso inflamatorio estĂĄ activo y se manifiesta radiolĂłgicamente en forma de ĂĄreas de vidrio deslustrado que afecta a las regiones donde hay fibrosis (fig 10).
5) ENFISEMA Y FIBROSIS PULMONAR COMBINADOS: la asociaciĂłn entre ambos hallazgos fue descrita por primera vez hace 30 años; desde entonces mĂșltiples estudios han corroborado su relaciĂłn con el hĂĄbito tabĂĄquico,
sin embargo no ha sido establecida como sĂndrome hasta 2005.
Se debe sospechar en pacientes fumadores con una marcada reducciĂłn del DLCO y preservaciĂłn o leve disminuciĂłn de los volĂșmenes pulmonares.
RadiolĂłgicamente se caracteriza por la presencia de enfisema centrilobular o paraseptal en lĂłbulos superiores y fibrosis en lĂłbulos inferiores con caracterĂsticas de FPI (figs 12 y 13).
A diferencia de la histiocitosis,
las bullas paraseptales son subpleurales y pueden tener paredes mås gruesas debido a la compresión del parénquima adyacente,
y el enfisema centrilobular,
al estar producido por destrucción del espacio aéreo,
mantiene la imagen puntiforme hiperdensa originada por el bronquiolo y los vasos centrilobulillares.