Los tratamientos endobronquiales del enfisema (TEE) pulmonar son métodos novedosos,
mínimamente invasivos que se presentan como una alternativa prometedora en la reducción de la disnea en pacientes con enfisema severo, para los que hasta el momento no se disponía de otro tratamiento salvo el trasplante o la cirugía de reducción del volumen pulmonar (CRVP).
La CRVP ha demostrado obtener una mejoría significativa funcional y de la calidad de vida en pacientes con predominio de enfisema en lóbulos superiores,
pero incluso en centros con gran experiencia conlleva una alta morbilidad (50%) y mortalidad (5-7,9 %),
con menor respuesta y más complicaciones en pacientes con enfisema homogéneo,
para los que no se considera indicado.
En el intento de conseguir los beneficios de la CRVP con un menor riesgo e inclusión de mayor número de pacientes,
se han desarrollado varios procedimientos broncoscópicos que persiguen una reducción del volumen en las regiones pulmonares con enfisema grave,
permitiendo la expansión del parénquima menos dañado y disminuyendo la dinámica que favorece el atrapamiento aéreo.
Estos procedimientos tienen diferente base fisiopatológica por lo que su indicación varía en función de la distribución homogénea o heterogénea del enfisema,
y por supuesto teniendo en cuenta los resultados y complicaciones de cada técnica,
como se explica a continuación.
Las modalidades de las que se dispone son:
Impiden la entrada de aire en la región enfisematosa diana,
permitiendo únicamente un flujo unidireccional de salida de aire y secreciones durante la espiración.
El aislamiento de este segmento pulmonar redirige el flujo a parénquima menos enfisematoso,
y trata de inducir la formación de una atelectasia lobar o segmentaria con la correspondiente pérdida de volumen pulmonar.
Existen dos modelos en el mercado,
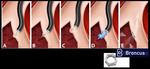
una prótesis con forma de paraguas y mecanismo valvular (Fig.
1),
y un stent autoexpandible que incorpora la válvula en su porción proximal (Fig.
2).
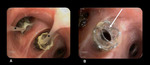
Su inserción,
guiada por visión broncoscópica directa,
se realiza con sedación y anestesia local,
requiriendo una corta estancia hospitalaria (Fig.
3).
Una de las ventajas del tratamiento con válvulas es la posibilidad de retirarlas en caso de mala colocación o disfunción.
Los candidatos son pacientes con enfisema heterogéneo de predominio en lóbulos superiores,
buscando un efecto fisiológico similar a la cirugía de reducción de volumen.
Existe controversia respecto a tratar uno o los dos pulmones,
aunque hay datos a favor del tratamiento unilateral en caso de emplear la válvula soportada por un stent y bilateral si se utiliza la válvula tipo paraguas.
Se ha observado una mejoría de la función respiratoria,
disnea y calidad de vida en estos los pacientes tras 1-3 meses de la implantación de las válvulas,
no obstante sin alcanzar resultados equiparables a la CRVP.
El principal factor limitante de la reducción de volumen es la existencia de comunicaciones anatómicas aéreas entre lóbulos,
consecuencia de la destrucción pulmonar en el enfisema,
que mantienen una ventilación colateral del pulmón tratado a pesar de la obstrucción bronquial.
Las complicaciones son mucho menores que con la CRVP,
siendo los efectos adversos más frecuentes la exacerbación de su EPOC (5%-20%) y el neumotórax (7-11 %) .
- Pegamentos: polímeros biológicos y sintéticos
Su instilación consigue colapsar y remodelar el pulmón hiperinsuflado de forma permanente mediante la formación de una reacción inflamatoria local y posterior cicatrización.
Los polímeros biológicos están formados a partir de una suspensión de fibrinógeno biofarmacéutico y solución de trombina,
que polimeriza in situ dando lugar a un hidrogel.
Este hidrogel contiene complejos de polilisina y condroitín sulfato,
que inician una reacción inflamatoria.
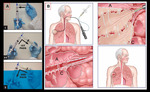
En nuestro hospital se ha optado por la espuma sellante,
formada por la combinación de un polímero sintético (mezcla de soluciones de polivinil alcohol aminado y de glutaraldehído) con aire,
y que consigue los mismos resultados de forma más segura.
(Fig.
4) El procedimiento se lleva a cabo en dos sesiones,
tratando inicialmente 2 ó 3 subsegmentos y tres meses después 2 ó 3 subsegmentos contralaterales.
Se instila un máximo de 3 bronquios subsegmentarios por sesión y no se tratan subsegmentos contiguos para evitar complicaciones debido a una exagerada respuesta inflamatoria.
) La instilación del pegamento,
guiada por visión broncoscópica directa,
se realiza con sedación y anestesia local,
requiriendo una corta estancia hospitalaria.
(Fig.
5)
La cicatrización ocurre a nivel alveolar,
esperando una reducción del volumen pulmonar funcional en un intervalo de tiempo de 6 a 8 semanas.
El pegamento causa la obstrucción los canales interalveolares y bronquioloalveolares tratando de impedir los efectos de la ventilación colateral,
a diferencia de las válvulas endobronquiales.
Ha demostrado mejoría funcional respiratoria,
con eficacia tanto en el enfisema homogéneo como en el heterogéneo.
No obstante,
en los casos de enfisema homogéneo también se han tratado los lóbulos superiores o segmentos apicales de lóbulos inferiores,
y los resultados siguen siendo algo inferiores a los obtenidos tras tratamiento de enfisema heterogéneo.
Su mayor desventaja es la irreversibilidad del procedimiento.
Por otro lado,
no se dispone de estudios a largo plazo que permitan saber si la degradación del material puede llevar a una disminución de la consolidación y recuperación del volumen.
En un gran número de pacientes se observa leucocitosis,
fiebre y/o malestar en las 12-24 horas posteriores a la intervención.
El paciente puede presentar dolor torácico tipo pleurítico,
especialmente cuando el tratamiento es periférico,
y la respuesta inflamatoria se encuentra en proximidad o contacto con pleura.
El siguiente efecto adverso más frecuente es la exacerbación de la EPOC (22%),
seguido de la broncoaspiración y la neumonía.
Otras modalidades empleadas con menor frecuencia son:
- Ablación térmica por vapor
La emisión de vapor caliente en vía aérea aislada por un balón en un bronquio genera una reacción inflamatoria con la consecuente pérdida de volumen del segmento tratado.
Actúan,
como los polímeros,
a nivel alveolar,
evitando parte del problema de la ventilación colateral de las válvulas.
Los pocos pacientes a los que se les ha realizado han referido mejoría de sus síntomas,
pero escasa mejoría en pruebas funcionales y de imagen,
observando igualmente exacerbaciones de EPOC y neumonitis.
- Coils en vía aérea (Fig.
6)
Obstruyen la vía aérea,
obteniendo la máxima reducción de volumen pulmonar en 2-4 semanas,
con la intención de tratar tanto el enfisema heterogéneo como el homogéneo.
Los resultados hasta ahora,
con pocos pacientes,
muestran mejoría funcional y en calidad de vida,
sin complicaciones severas ni neumotórax.
No obstante se sospecha que la distorsión de los bronquios puede ocasionar la formación de bronquiectasias y tortuosidad de los vasos con potencial riesgo de trombosis e infarto.
Otros métodos actualmente abandonados:
- By-pass de vía aérea mediante stents (Fig.
7)
Se crean fenestraciones bronquiales de baja resistencia,
donde se colocan stents con el objetivo de permitir la salida de aire atrapado a través de ventilación colateral,
evitando el paso por la vía aérea con alta resistencia al flujo.
Los resultados son variables,
lo cual sumado a que requiere anestesia general,
hay fallos en la implantación y más complicaciones descritas que con otros procedimientos,
no se emplean en la actualidad.
- Bloqueadores bronquiales (balones de silicona,
stents con esponja oclusiva).
Obstruyen la luz bronquial impidiendo la entrada y salida de aire y secreciones al pulmón aislado. Actualmente en desuso por la alta tasa de migraciones del material descritas y casos de neumonía postobstructiva.
Ver Tabla 1: resumen de las modalidades de tratamiento endobronquial,
indicaciones y complicaciones más frecuentes.
PROTOCOLO DE ESTUDIO Y SEGUIMIENTO
En los pacientes con enfisema avanzado y síntomas que no responden al tratamiento,
la combinación de parámetros funcionales y hallazgos de imagen permiten seleccionar a aquellos que se beneficiarán de un tratamiento de reducción de volumen pulmonar.
Ver Tabla 2,
en la que se muestran las pruebas requeridas y parámetros aceptados para la inclusión de pacientes.
Los criterios de exclusión principales que seguimos en nuestro hospital se exponen en la Tabla 3.
Por protocolo,
a los candidatos a TEE,
les realizamos una TC torácica previa al procedimiento y controles sucesivos a los 3,
6 meses y 12 meses.
Las imágenes se adquieren con colimación de 0,8 mmy pitch de 1,
enviando al PACS reconstrucciones de 1 mm sin solapamiento,
con filtro y ventana adecuados para pulmón y reconstrucciones de 2 mm de grosor y 1 mm de solapamiento con filtro y ventana adecuados para mediastino.
A partir de las imágenes con solapamiento generamos imágenes minIP de 5-10 mmde grosor en transversal y coronal,
que nos ayudan a identificar el enfisema.
En pacientes con complexión media,
la TC se obtiene con técnica de baja dosis (120kV y 70 mAs de referencia),
que se mantiene como una constante para el seguimiento.
Como ya algunos autores han demostrado,
la baja dosis no nos ha impedido identificar el enfisema,
pero emplear la misma técnica es importante para que los datos sean más reproducibles,
especialmente si se cuantifica el enfisema.
No obstante si el paciente tiene una TC de tórax estándar reciente (120mAs) no repetimos el estudio previo a la intervención.
La inyección de contraste iv no es necesaria e incluso puede producir artefactos por endurecimiento del haz de RX alterando los resultados en el post-proceso,
pero sí lo empleamos en casos indicados por sospecha clínica.
A los pacientes se les realiza también un examen clínico y pruebas respiratorias funcionales previamente al tratamiento (basal) y a los 3,6,
9 y 12 meses post-intervención.
TC TÓRAX PREVIA AL PROCEDIMIENTO
El estudio por imagen del tórax es importante en la selección de los candidatos al TEE y en la elección de la técnica adecuada.
La Tomografía Computarizada (TC) permite identificar el enfisema como focos ó áreas de baja atenuación por destrucción pulmonar y disrupción vascular,
y muestra su extensión y distribución.
La cuantificación del enfisema es útil si se dispone de un software robusto,
por su mayor consistencia y reproducibilidad frente a la graduación visual.
Normalmente se consideran con enfisema aquellos vóxels con densidad por debajo de -950 UH.
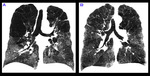
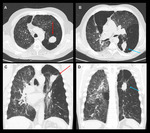
Los pacientes que más se benefician de una reducción de volumen son aquellos con enfisema heterogéneo de predominio en lóbulos superiores.
(Fig.
8a).
El tratamiento se dirige normalmente al lóbulo o pulmón más heterogéneo,
evitando tratar áreas con enfisema bulloso extenso o con bullas de tamaño superior a 10 cm,
en el que no se esperan buenos resultados.
(Fig.
9)
El enfisema homogéneo responde peor al tratamiento mostrando menor disminución de volumen pulmonar y se piensa que está condicionado por mayor ventilación colateral.
(Fig.
8b).
En estos pacientes la reducción con pegamentos bronquiales biológicos o sintéticos es la técnica disponible actualmente que ha ofrecido los mejores resultados funcionales y clínicos.
La ausencia de cisuras también indica la presencia comunicaciones interlobares que permiten la ventilación colateral,
lo cual se ha asociado con menor posibilidad de reducción de volumen con válvulas endobronquiales (Fig.
10).
No obstante como se explica más adelante,
la reducción de volumen no es probablemente el único mecanismo responsable de la mejoría con estas terapias.
La TC también aporta información sobre la posible presencia de hipertensión arterial pulmonar,
frecuente en pacientes con enfisema severo y reflejada en imagen por un aumento del diámetro de la arteria pulmonar (>30 mm) con posible sobrecarga y dilatación de ventrículo derecho.
Se deben descartar nódulos sospechosos de malignidad y señalar la presencia de nódulos indeterminados,
otras lesiones pulmonares y pleurales,
así como la presencia de calcificaciones coronarias,
que si bien no constituyen por sí solos un criterio de exclusión para el tratamiento endobronquial,
deben ser considerados a la hora de planificar la terapia de estos pacientes.
Ver Tabla 4,
en la que se muestran los puntos que deben describirse en el informe radiológico de TC torácica previa a la intervención.
TC TÓRAX DE SEGUIMIENTO
La TC es útil post-tratamiento ya que permite evaluar la respuesta identificando consolidaciones inflamatorias,
atelectasias y pérdida de volumen pulmonar,
y descarta posibles complicaciones.
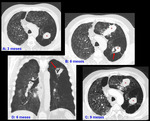
Hallazgos post-TEE
- Las válvulas se colocan e
 [LF1] n bronquios generalmente segmentarios o subsegmentarios,
dependiendo de la anatomía valorada en el momento de la intervención.
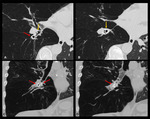
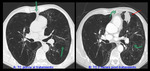
En la TC de control se confirma la correcta disposición de estas válvulas (Fig.
11) y se busca la atelectasia segmentaria o subsegmentaria consecuencia de la obstrucción bronquial.
En la mayoría de los casos no se consiguen atelectasias lobares debido a la presencia de ventilación colateral y cisuras lobares incompletas.
[LF1] n bronquios generalmente segmentarios o subsegmentarios,
dependiendo de la anatomía valorada en el momento de la intervención.
En la TC de control se confirma la correcta disposición de estas válvulas (Fig.
11) y se busca la atelectasia segmentaria o subsegmentaria consecuencia de la obstrucción bronquial.
En la mayoría de los casos no se consiguen atelectasias lobares debido a la presencia de ventilación colateral y cisuras lobares incompletas.
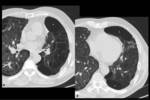
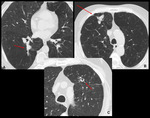
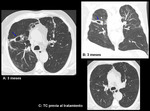
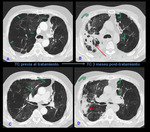
- En el caso de pegamentos y ablación con vapor,
se identificarán unas consolidaciones en los segmentos tratados,
constituidas por tejido inflamatorio reactivo y atelectasia del parénquima adyacente.
Estas consolidaciones suelen presentar una morfología redondeada o alargada,
con bordes bien definidos y sin broncograma aéreo,
y pueden simular masas pulmonares si se desconoce el antecedente de tratamiento endobronquial.
(Fig.
12).
En ocasiones el tejido inflamatorio reactivo es más escaso y se observan únicamente pequeñas opacidades nodulares sin atelectasia y pérdida de volumen valorable (Fig.
13).
En algunos casos no hemos apreciado ningún cambio en el segmento tratado por una probable falta de respuesta inflamatoria.
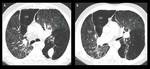
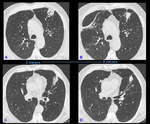
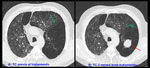
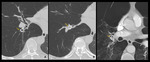
- En los pacientes tratados en nuestro hospital con pegamento sintético hemos observado espacios rellenos de aire en el seno de las consolidaciones.
Estas pseudocavitaciones corresponden probablemente a enfisema residual atrapado,
o entrada de aire por comunicación con bronquios aireados,
consecuencia del remodelado y retracción producidos por el tejido inflamatorio (Fig.
14 y Fig.
15).
Pueden aparecer tanto a los 3 como a los 6 meses,
y suelen resolverse o disminuir de tamaño espontáneamente,
no obstante no disponemos de controles a largo plazo.
Por el momento no hemos objetivado una repercusión de estos cambios sobre la clínica y las pruebas funcionales.
Es importante saber que este hallazgo es frecuente y no confundirlo con una sobreinfección.
Si se desconoce el antecedente de tratamiento con pegamento endobronquial se puede interpretar erróneamente como una aspergilosis u otras infecciones invasivas,
o incluso con un adenocarcinoma.
- Por otro lado,
en la formación de estos espacios con aire puede participar también la necrosis como consecuencia de una respuesta inflamatoria exagerada.
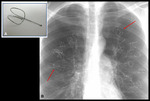
Hemos recogido un caso en el que se produjo una cavitación extensa por necrosis estéril.
La RX tórax de control se interpretó como neumonía con formación de absceso,
por falta de datos clínicos.
No obstante,
la discordancia clínico-radiológica y la rápida mejoría radiológica permitieron descartar este diagnóstico.
(Fig.
16 y 17)
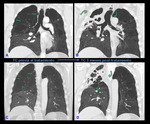
- La pérdida de volumen puede reconocerse cualitativamente por el desplazamiento de cisuras,
vasos,
mediastino y línea pleural anterior (ejemplos Fig.
18,
19,
20a y 20b).
Si se dispone del software adecuado se puede cuantificar la reducción de volumen del lóbulo tratado comparando con el estudio basal.
Sin embargo hay que tener en cuenta que debido a la complejidad del intercambio gaseoso en pacientes con enfisema severo,
puede no haber correlación entre clínica,
la pruebas funcionales y la pérdida de volumen pulmonar.
En nuestra experiencia,
todavía con una pequeña población y la mayoría con polímeros,
hay pacientes presentan una mejoría clínica y funcional sin una reducción significativa del volumen pulmonar,
como el ejemplo de la figura 13.
Esto puede explicarse porque incluso en ausencia de atelectasia,
la exclusión de la ventilación de las partes más afectadas reduce fisiológicamente el espacio muerto,
redirigiendo el aire hacia segmentos menos enfisematosos.
Complicaciones post-TEE
- En el caso de las válvulas la principal complicación que hay que descartar es el neumotórax.
El mecanismo de formación no ha sido aclarado,
pudiendo deberse a adherencias pleurales,
a rotura de blebs y bullas tras la relajación en segmentos no tratados o a un retraso en el remodelado tras una atelectasia significativa de los segmentos tratados.
El neumotórax puede ser muy pequeño,
oculto en RX tórax y sólo visible en TC.
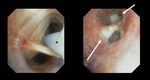
- Con frecuencia se observa retención de secreciones en la porción distal de los stent de las válvulas (Fig.
22).
En ocasiones puede observarse un tejido hiperplásico de granulación en la porción proximal donde se ubica la válvula.
- Tras el tratamiento con pegamentos los principales eventos adversos que hay que descartar por imagen son la broncoaspiración,
la neumonía y con mucha menos frecuencia el neumotórax.
Hasta hoy no hemos detectado estas complicaciones por imagen
Ver Tabla 5,
en la que se muestran los puntos que deben describirse en el informe radiológico de TC torácica posterior a la intervención.
BIBLIOGRAFIA
- Mordechai R.
Kramer FCCP,
Yael Refaely MD,
Moshe-Nimrod Maimon MD,
Bilateral Endoscopic Sealant Lung Volume Reduction.
Pulmonary Institute Rabin Medical Center,
Beilinson Medical Center,
Petah Tikva 49100,
Israel.
Emails: [email protected];
 [email protected] Department of Thoracic Surgery,
Soroka Medical Center,
Be’er Sheva 49100,
Israel 5 de mayo del 2011..
Email: [email protected]
[email protected] Department of Thoracic Surgery,
Soroka Medical Center,
Be’er Sheva 49100,
Israel 5 de mayo del 2011..
Email: [email protected]
- 2. Herth FJ,
Gompelmann D,
Stanzel F,
Bonnet R,
Behr J,
Schmidt B,
Magnussen H,
Ernst A,
Eberhardt R.
Treatment of advanced emphysema with emphysematous lung sealant (AeriSeal®).
Respiration.
2011;82(1):36-45.
Epub 2011 Jan 11.
- Magnussen H,
Kramer RM,
Kirsten AM,
et al.
Effect of fissure integrity on lung volume reduction using a polymer sealant in advanced emphysema.
Thorax 2012.
doi:10.1136/thoraxjnl-2011-201038.
- Refaely Y,
Dransfield M,
Kramer MR,
Gotfried M,
Leeds W,
McLennan G,
Tewari S,
Krasna M,
Criner GJ.
Biologic lung volume reduction therapy for advanced homogeneous emphysema.
Eur Respir J.
2010 Jul;36(1):20-7.
Epub 2009 Nov 19.
- 5. Criner GJ,
Pinto-Plata V,
Strange C,
Dransfield M,
Gotfried M,
Leeds W,
McLennan G,
Refaely Y,
Tewari S,
Krasna M,
Celli B.
Biologic lung volume reduction in advanced upper lobe emphysema: phase 2 results.
Am J Respir Crit Care Med.
2009 May 1;179(9):791-8.
Epub 2009 Jan 29.
- 6. Reilly J,
Washko G,
Pinto-Plata V,
Velez E,
Kenney L,
Berger R,
Celli B.
- Chest.
2007 Apr;131(4):1108-13.
Biological lung volume reduction: a new bronchoscopic therapy for advanced emphysema.
- Coxson HO,
Nasute Fauerbach PV,
Storness-Bliss C,
Müller NL,
Cogswell S,
Dillard DH,
Finger CL,
Springmeyer SC.
Computed tomography assessment of lung volume changes after bronchial valve treatment.
Eur Respir J.
2008 Dec;32(6):1443-50.
- Fishman A,
Martinez F,
Naunheim K,
Piantadosi S,
Wise R,
Ries A,
Weinmann G,
Wood DE: A randomized trial comparing lung- volume-reduction surgery with medical therapy for severe emphysema.
The New England journal of medicine 2003,348(21):2059-2073.
- Ingenito EP,
Reilly JJ,
Mentzer SJ,
et al.
Bronchoscopic volume reduction: a safe and effective alternative to surgical therapy for emphysema.
Am J Respir Crit Care Med 2001;164:295e301.
- Robert L.
Berger ,
MD; Malcolm M.
DeCamp ,
MD; Gerard J.
Criner ,
MD,
FCCP; and Bartolome R.
Celli ,
MD,
FCCP.
Lung Volume Reduction Therapies for Advanced Emphysema.
Chest 2010;138;407-417.
- Antonio D’Andrilli a,
Laura Vismara b,
Matilde Rolla c,
Mohsen Ibrahim a,
Federico Venuta c,Ilaria Pochesci b,
Raffaele Masciangelo d,
Erino Angelo Rendina.
Computed tomography with volume rendering for the evaluation of parenchymal hyperinflation after bronchoscopic lung volume reduction.
European Journal of Cardio-thoracic Surgery 35 (2009) 403—407.
- Edward P.
Ingenito1,
Douglas E.
Wood2,
and James P.
Utz3.
Bronchoscopic Lung Volume Reduction in Severe Emphysema.
PROCEEDINGS OF THE AMERICAN THORACIC SOCIETY VOL 5 2008.
- The National Emphysema Treatment Trial Research Group,
Rationale and design of The National Emphysema Treatment Trial (NETT) : a prospective randomized trial of lung volume reduction surgery.
Chest 1999; 116: 1750–1761.