El SVCS es debido a una dificultad en el drenaje venoso de cabeza y cuello y extremidades superiores [1,
2].
Tiene una clínica muy característica que incluye el edema facial y la reticulación venosa superficial.
Ante su sospecha es necesario realizar pruebas de imagen para su evaluación.
La correlación entre las imágenes y la clínica sugiere que la severidad de los síntomas depende del nivel de obstrucción (por encima o por debajo del cayado de la ácigos) y de un abundante desarrollo de colaterales.
El TC multidetector (TCMD) puede detectar la obstrucción de la VCS subclínica en pacientes relativamente asintomáticos [3].
En esta revisión analizamos las diferentes causas del SVCS en casos de nuestro centro y su fisiopatología,
así como la circulación colateral que se puede identificar,
destacando la afectación de la vena ácigos.
Es necesario el conocimiento de la anatomía para entender las características de la circulación colateral.
También se revisan los hallazgos radiológicos en el TCMD y la flebografía antes y después del tratamiento del SVCS.
La flebografía convencional ha pasado de ser la técnica de imagen de referencia para el diagnóstico del SVCS a usarse para la intervención terapéutica y ser reemplazada en el diagnóstico por técnicas no invasivas como el TCMD.
El TCMD combina las imágenes axiales para el diagnóstico del SVCS con las reconstrucciones multiplanares,
mejorando la detección del nivel y extensión de la obstrucción.
Es muy útil para planear el manejo por el cirujano,
el oncólogo radioterápico o el radiólogo intervencionista.
Independientemente de su causa,
el diagnóstico del SVCS mediante TCMD incluye [4]:
- Falta de opacificación de la VCS.
- Estenosis severa de la VCS.
- Canales vasculares colaterales.
- Defecto de repleción intraluminal,
si existe trombosis asociada.
CAUSAS
Este síndrome se trata con mayor frecuencia de una entidad adquirida,
y las diferentes causas son:
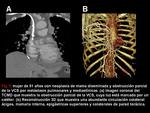
- Maligna: la más frecuente,
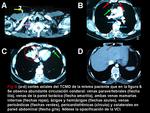
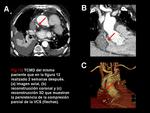
pudiendo ser neoplasias (Figuras 1-6) o metástasis (Figura 7) con afectación mediastínica.
El cáncer es la causa más frecuente de SVCS.
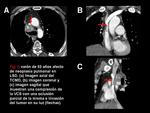
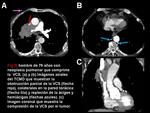
El cáncer de pulmón,
de célula pequeña o grande,
puede invadir directamente la VCS (Figura 1).
El linfoma,
Hodgkin o no Hodgkin,
tiende a comprimir el vaso.
Otros tumores mediastínicos,
incluyendo el timoma maligno,
el tumor germinal y las metástasis o tumores pleurales,
como el mesotelioma,
también pueden causar SVCS [1].
La mayoría de tumores malignos de la vena cava,
como el leiomiosarcoma o angiosarcoma,
afectan a la VCI.
La afectación de la VCS es muy rara.
Si existe realce arterial del trombo es muy sugestivo de trombo tumoral.
- Benigna: incluye infecciones,
mediastinitis fibrosante (Figuras 8-11),
bocio tiroideo endotorácico,
aneurisma aórtico,
tumores benignos,
hematoma mediastínico (Figuras 12 y 13),
sarcoidosis o fibrosis inducida por radiación [5].
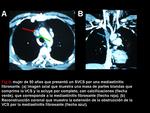
La mediastinitis fibrosante es una enfermedad benigna rara debida a la proliferación de tejido colágeno y a la fibrosis del mediastino.
Puede ser idiopática,
causada por una respuesta inmunológica anómala a una infección por Histoplasma capsulatum o por tuberculosis,
o puede asociarse a una fibrosis retroperitoneal,
especialmente en su forma difusa.
En el TCMD la mediastinitis fibrosante aparece como una masa de partes blandas mal definida obliterando la grasa normal.
El que se afecta con más frecuencia es el mediastino medio.
Existe otra forma más focal con calcificaciones [6] (Figura 8).
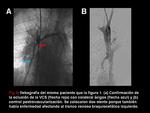
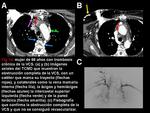
La enfermedad de Behçet es una enfermedad sistémica rara que afecta más frecuentemente a la población del Mediterráneo,
oriente medio y Asia.
Causa úlceras genitales y orales recurrentes y uveítis.
Es una enfermedad inflamatoria asociada a vasculitis leucocitoclástica que afecta a arterias y venas sistémicas y pulmonares.
La estenosis u oclusión de la VCS en el Behçet puede ser causada por tromboflebitis o por una mediastinitis fibrosante,
aunque la afectación de grandes venas no es frecuente.
- Iatrogénica: como una cateterización venosa.
Esta causa ha aumentado debido al incremento del uso de catéteres intravasculares [1],
que producen una reacción de la pared venosa como respuesta a un trauma repetido.
Los catéteres venosos centrales grandes,
como los catéteres de diálisis,
los catéteres Hickman,
los de nutrición parenteral y los cables de marcapasos cardiaco permanente transvenoso (Figura 14),
se han visto relacionados con el SVCS.
CIRCULACION COLATERAL
Al producirse una oclusión crónica de la VCS se debe desarrollar una circulación colateral para mantener el drenaje venoso [1],
cuyo patrón es predecible según el nivel de la obstrucción.
La mayoría de venas que drenan las extremidades superiores y la cabeza y el cuello,
que son los troncos venosos braquiocefálicos,
la VCS,
y el sistema ácigos-hemiácigos,
están conectadas por una abundante red de pequeños plexos venosos que normalmente están colapsados.
En la oclusión de la VCS el flujo sanguíneo se redistribuye a través de la red de canales colaterales,
que en el TCMD,
destacan como vasos tortuosos aumentados de calibre que se opacifican con el contraste.
Los sistemas ácigos y hemiácigos redistribuyen la sangre de la VCS a la VCI,
pudiendo también dilatarse y adoptar un trayecto tortuoso.
La presencia de los vasos colaterales es un importante hallazgo en el TCMD del SVCS,
con una sensibilidad del 96% y una especificidad del 92% [7].
Su extensión y localización es muy variable pero habitualmente afecta a las venas del tórax,
abdomen,
e incluso de la pelvis.
El desarrollo de abundantes colaterales protege al paciente de desarrollar síntomas más severos.
El TCMD junto con las reconstrucciones multiplanares y 3D permite una visión anatómica de las diferentes vías colaterales redistribuyendo el flujo sanguíneo desde la obstrucción.
Aunque los cortes axiales permiten realizar un diagnóstico del SVCS,
las reconstrucciones multiplanares dan una información muy valiosa sobre el nivel y grado de la obstrucción,
la extensión del segmento afectado,
y la presencia o ausencia de trombo intraluminal distal a la obstrucción,
permitiendo al radiólogo intervencionista escoger el tratamiento más óptimo [4].
Colaterales venosas torácicas:
En el TCMD hay varios plexos venosos mayores torácicos que se opacifican y son visibles.
Aunque hay muchos factores que influyen en la opacificación de las venas colaterales,
la detección de los canales dominantes puede dar la clave del nivel de la oclusión venosa [8].
Las colaterales venosas visibles más frecuentes son [1,9]:
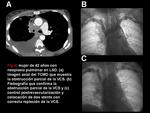
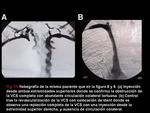
- Sistema ácigos-hemiácigos-hemiácigos accesoria (Figura 2): las venas ácigos y hemiácigos pueden redistribuir la sangre desde la VCS (Figura 7,
9 y 11).
Si la obstrucción es por encima del cayado de la ácigos se produce un flujo anterógrado desde la ácigos a la aurícula derecha,
con una transición abrupta entre una ácigos superior densamente opacificada (debido al drenaje a través de las venas intercostales) y una ácigos inferior no opacificada.
Si la obstrucción de la VCS es por debajo del cayado,
toda la ácigos y hemiácigos están opacificadas (Figura 5),
con un flujo sanguíneo retrógrado hacia la VCI [8].
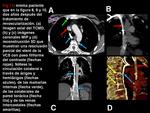
- Plexos vertebral y subescapular: el plexo venoso vertebral de las venas paravertebrales,
intervertebrales y epidurales da colaterales al sistema ácigos o a la VCI vía las venas lumbares ascendentes (Figura 3 y 9).
- Plexo venoso mediastínico,
esofágico y diafragmático: incluye las venas mediastínicas,
pericárdicas y pericardiofrénicas (Figura 9) drenando en la VCI,
o más caudalmente en las venas frénicas inferiores o vía colaterales transhepáticas [1].
- Plexos venosos torácico lateral y tóraco-abdominal superficial: las venas mamarias internas y torácicas laterales comunican con las venas tóraco-epigástricas y epigástricas superficiales.
Las venas colaterales de la pared torácica y de la mama también se pueden opacificar indicando un SVCS (Figura 5,
7,
9,
11 y 14).
Colaterales venosas abdominales:
Además de la opacificación de canales vasculares tortuosos o redondeados en la pared abdominal (Figura 9),
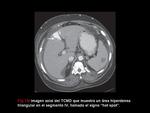
se pueden ver anomalías en la perfusión hepática y el llamado “hot spot” (una opacificación hiperdensa en el segmento IV),
que son resultado de la comunicación entre las venas epigástricas superficiales y la vena porta izquierda (Figura 15).
La localización del área de realce es característica y no se debe confundir con una masa hipervascular.
Otro posible canal colateral afecta a las venas frénicas inferiores y hepáticas subcapsulares con una opacificación intensa de la porción subdiafragmática del hígado.
Existen otras vías menos usuales como son vía colaterales venosas sistémico-pulmonares (que pueden provocar un shunt derecha-izquierda) e intrahepáticas (que producen patrones de realce inusuales en el hígado) [5].
Es esencial que entendamos los cambios hemodinámicos en el SVCS y éstas vías colaterales para una correcta interpretación de los hallazgos radiológicos antes y después del tratamiento.
TRATAMIENTO
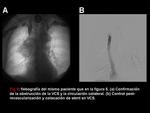
El tratamiento de elección en pacientes con SVCS es el tratamiento endovascular mediante angioplastia o colocación de stent [1].
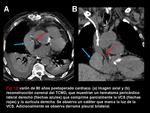
Las endoprótesis de VCS son muy efectivas en el tratamiento de las causas benignas (Figura 10),
incluso si se es portador de un marcapasos,
pero estos pacientes requerirán antiagregación y /o anticoagulación por largos períodos para evitar la trombosis.
Por este motivo,
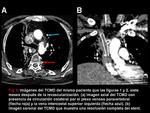
inicialmente se prefiere el tratamiento con angioplastia y diferir la colocación del stent siempre que sea posible. También se usan las endoprótesis para pasar obstrucciones malignas porque mejoran la calidad de vida significativamente (Figura 2,
4 y 6).
El TCMD permite ver si el stent es permeable si hay contraste en su luz (Figura 11) o si está ocluido (Figura 3).
Si además hay circulación colateral,
es un signo indirecto de que el stent no es funcionante.