El estudio de la patología cortical mediante técnicas de susceptibilidad magnética se ha desarrollado en los últimos años,
desde el desarrollo de la técnica por parte del grupo de Haacke (1).
El esquema de revisión se divide en:
1.
La secuencia de susceptibilidad.
2.
Patología cortical en susceptibilidad.
1.
La secuencia de susceptibilidad.
1.1.
Características técnicas.
La secuencia de susceptibilidad magnética (SSM) es una secuencia ponderada en T2 con unas características diferenciales.
Se trata de una secuencia T2 gradiente 3D con compensación de flujo,
con TR y TE cortos,
y a la que posteriormente se aplica un post-procesado.
Se obtienen por separado los mapas de magnitud y fase de la adquisición,
de tal forma que se pueden obtener datos directamente de la imagen de fase (por ejemplo cuantificar hierro en vóxel),
además de usar la fase como máscara.
esta máscara,
resultado de la multiplicación iterativa de la fase se suma a la magnitud,
obteniendo una nueva imagen,
que es más homogénea y que discrimina más entre ssutancias paramagnéticas-diamagnéticas.
Por tanto se homogeneizan las estructuras diamagnéticas y resaltan de forma sustancial la caída de señal de las paramagnéticas.
Finalmente se puede aplicar un nuevo filtro en forma de reconstrucción de mínima intensidad (minIP) que permite en un solo corte delimitar mejor las estructuras vasculares (venosas),
así como las lesiones aisladas (hemorragias).
Las características de la secuencia hacen que sea especialmente sensible en la detección de sustancias paramagnéticas,
que en el cerebro están representadas principalmente por el hierro.
Este hierro básicamente es el dependiente de la hemoglobina,
aunque también se encuentra el hierro parenquimatoso de depósito.
Con respecto al hierro ligado al grupo hemo,
es la desoxihemoglobina y los derivados de la destrucción de la misma los productos con mayor grado de paramagnetismo (la oxihemoglobina es diamagnética).
Por lo que todas aquellas estructuras/patologías en las que intervenga el componente hemático serán detectadas con mayor sensibilidad por esta secuencia.
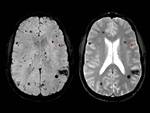
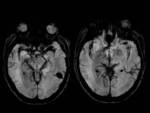
Se ha comparado la SSM con la secuencia de eco de gradiente / hemosiderina (T2*) en diferentes patologías y se ha observado como detecta mayor número de lesiones y además presenta una mejor conspicuicidad (discriminación entre tejidos paramagnéticos y no paramagnéticos).
Fig. 1
1.2.
Utilidades generales.
La SSM se desarrolló en un principio como técnica vascular venográfica.
Se ha usado en el estudio de las malformaciones vasculares con un mayor componente venoso,
desde las anomalías del desarro venoso,
malformaciones arteriovenosas,
fístulas arteriovenosas y especialmente cavernomas.
También se ha analizado su papel en el estudio del ictus agudo y otras patologías ictales.
La presencia de tejido con perfusión de miseria se acompaña de un aumento de la extracción de oxígeno.
Estos cambios en la proporción de oxi-desoxihemoglobina concurren en una disminución de la señal de resonancia en SSM en estas áreas.
Donde la SSM ha desmostrado una sensibilidad hasta 3 veces superior a las secuencias clásicas hemo T2* es en la detección de lesiones focales hemorrágicas.
Se ha estudiado tanto en la presencia de cavernomas como en las microhemorragias asociadas a hipertensión,
angiopatía amiloide a incluso en las hemorragias traumáticas.
Además del hierro asociado al grupo hemo,
el hierro de depósito se puede analizar en RM.
Se puede estudiar el depósito en los núcleos profundos así como el córtex,
e incluso por ejemplo,
en sustancia blanca (depósito en lesiones de esclerosis múltiple).
2.
Patología del córtex.
A continuación se presenta una revisión del espectro de aquellas lesiones que afectan al córtex cerebral y cuyas manifestaciones en susceptibilidad magnética permiten un diagnóstico más sensible y específico de cada una de ellas.
2.1.
Cambios normales.
El envejecimiento normal comporta depósito de hierro en las capas neuronales del córtex.
Estos cambios son más evidentes en el córtex motor y ya se habían descrito en otras secuencias ponderadas en T2 y T2*.
2.2.
Enfermedades degenerativas.
Los cambios degenerativos corticales descritos en el envejecimiento se pueden observar de forma más marcada y precoz en diferentes patologías degenerativas (2).
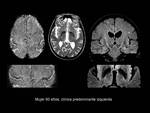
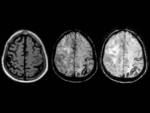
En la esclerosis lateral amiotrófica la SSM se observa una mayor hiposeñal en el córtex motor que la alteración normal producida por el envejecimiento,
que puede incluso llegar a ser asimétrica entre hemisferios.
Fig. 2
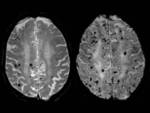
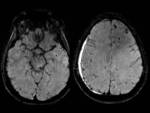
También se pueden observar estos cambios corticales en otras patologías degenerativas,
por ejemplo en el Alzheimer con patrón posterior se puede observar una asimetría cortical parieto-occipital.
Fig. 3
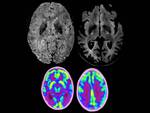
La cuantificación de hierro (3) se ha estudiado en varias patologías: como el Parkinson (depósito en el ára lateral de la sustancia negra) o el Alzheimer (depósito en el hipocampo,
pálido ventral y sustancia de Meynert),
y en otras patologías menos prevalentes como la neuroferritinopatía,
la aceruroplasminemia,
etc.
En cuanto a las lesiones focales hemorrágicas corticales,
debido a su sensibilidad,
la SSM permite identificar mayor número de microsangrados corticales en la angiopatía amiloide que las técnicas convencionales T2* (4).
2.3.
Lesiones isquémicas y vasculares.
La sensibilidad aumentada de la SSM permite identificar focos de transformación hemorrágica petequial de forma más conspicua que otras secuencias T2*.
Y en fases más tardías también permite estudiar la extensión de la necrosis laminar cortical.
Fig. 5
De la misma forma que en otras secuencias gradiente,
además de los cambios corticales descritos,
también la SSM permite identificar el trombo en la fase aguda,
tanto a nivel arterial como venoso (5).
En pacientes afectos de hemorragia subaracnoidea aguda y siderosis meníngea,
la SSM perfila mejor la extensión de la misma que otras secuencias gradiente.
La SSM es capaz de detectar pequeñas lesiones hemorrágicas corticales en el contexto de pacientes con cavernomatosis.
Fig. 6 Además permite valorar la afectación cortical en pacientes afectos de malformaciones arteriovenosas,
fístulas,
anomalías del desarrollo venoso,
Sturge-Weber (6),
etc.
2.4.
Lesiones tumorales.
La SSM permite detectar focos de microsangrado y calcificaciones (para distinguir entre ambas se puede aprovechar la imagen de fase).
Además se ha descrito cambios en la señal de la pared tumoral y en relación a la angiogénesis (7 y 8).
2.5.
Lesiones infecciosas.
Recientemente se ha publicado un artículo que analiza el papel de la SSM en la pared de los abscesos (9).
Permite también identificar con mayor conspicuicidad microsangrados o calcificaciones en diferentes patologías infecciosas (10).
2.6.
Lesiones traumáticas.
Como en los otros grupos patológicos,
la SSM detecta mayor número de lesiones hemorrágicas de menor tamaño y perfila con mayor exactitud la extensión de la hemorragia subaracnoidea.
Debido a la importancia del pronóstico en la lesión axonal difusa y la evaluación del grado de daño cerebral,
la SSM resulta de especial interés en este apartado.
Fig. 7
Referencias:
1.
Mittal S,
Wu Z,
Neelavalli J,
Haacke EM.
Susceptibility-weighted imaging: technical aspects and clinical applications,
part 1 and 2.
AJNR Am J Neuroradiol.
2009
2.
Larsen JP,
Britt W,
Kido D,
et al.
Susceptibility weighted magnetic resonance imaging in evaluation of dementia. Radiology Case Reports 2007;2:102
3.
Haacke EM,
Cheng NY,
House MJ,
et al.
Imaging iron stores in the brain using magnetic resonance imaging. Magn Reson Imaging 2005;23:1–25
4.
Schrag M,
McAuley G,
Pomakian J,
Jiffry A,
Tung S,
Mueller C,
Vinters HV,
Haacke EM,
Holshouser B,
Kido D,
Kirsch WM.
Correlation of hypointensities in susceptibility-weighted images to tissue histology in dementia patients with cerebral amyloid angiopathy: a postmortem MRI study.
Acta Neuropathol.
2010 Mar;119(3):291-302.
5.
Chalela JA,
Haymore JB,
Ezzeddine MA,
et al.
The hypointense MCA sign. Neurology 2002;58:1470
6.
Hu J,
Yu Y,
Juhasz C,
et al.
MR susceptibility weighted imaging (SWI) complements conventional contrast enhanced T1 weighted MRI in characterizing brain abnormalities of Sturge-Weber syndrome. J Magn Reson Imaging 2008;28:300–07
7.
Sehgal V,
Delproposto Z,
Haddar D,
et al.
Susceptibility-weighted imaging to visualize blood products and improve tumor contrast in the study of brain masses. J Magn Reson Imaging 2006;24:41–51
8.
Christoforidis GA,
Kangarlu A,
Abduljalil AM,
et al.
Susceptibility-based imaging of glioblastoma microvascularity at 8 T: correlation of MR imaging and postmortem pathology. AJNR Am J Neuroradiol 2004;25:756–60Wu Z,
Mittal S,
Kish K,
et al.
Identification of calcification with magnetic resonance imaging using susceptibility-weighted imaging: a case study.
J Magn Reson Imaging 2009;29:177–82
9.Toh CH,
Wei KC,
Chang CN,
Hsu PW,
Wong HF,
Ng SH,
Castillo M,
Lin CP.
Differentiation of Pyogenic Brain Abscesses from Necrotic Glioblastomas with Use of Susceptibility-Weighted Imaging. AJNR Am J Neuroradiol.
2012
10.
Gasparetto EL,
Pires CE,
Domingues RC.
Susceptibility-weighted MR phase imaging can demonstrate retrograde leptomeningeal venous drainage in patients with dural arteriovenous fistula. AJNR Am J Neuroradiol.
2011 Mar;32(3):E54.