La Gliomatosis cerebri(GC) la OMS la clasifica dentro de las neoplasias neuroepiteliales de origen desconocido y en ocasiones la subclasifica en primaria cuando aparece sin antecedentes de neoplasia y secundaria cuando aparece a partir de tumor cerebral previo.
A su vez la GC primaria se puede subdividir en tipo 1, si es una infiltración difusa sin masa tumoral y en tipo 2 si tiene masa tumoral asociada.
La forma más frecuente de presentación es la GC primaria tipo I.
Tanto las manifestaciones clínicas: cefalea,
déficits focales,
convulsiones como los hallazgos radiológicos en TC y RM son inespecíficos siendo necesaria la biopsia para un diagnóstico definitivo.
Por todo ello puede retrasarse el diagnóstico de 1 mes a 1 año.
La edad de presentación y el sexo tampoco nos ayuda pues se puede presentar desde la edad infantil hasta la ancianidad aunque mayormente aparece entre la tercera y la quinta década de la vida.
Tiene la misma incidencia en hombres y mujeres aunque hay estudios que han encontrado una incidencia mayor en hombres.
Con todo lo dicho hasta ahora nosotros como radiólogos debemos estar alerta para sospecharlo ante algunos hallazgos aunque no sean específicos ya que el tratamiento con quimioterapia,
Temozolomida y radioterapia(RT) mejora el pronóstico en estos pacientes.
La GC es una enfermedad que tiene predilección por la sustancia blanca,
que siempre está afectada,
aunque también puede afectar a la sustancia gris y corteza,
siendo la afectación de esta última en sólo un 20% de los casos.
Tiene preferencia por algunas localizaciones siendo por orden de frecuencia las siguientes: hemisferios cerebrales, mesencéfalo,
protuberancia,
tálamo,
ganglios de la base y muy infrecuentemente el cerebelo y médula espinal.
Siendo necesario para el diagnóstico el que tenga afectación de dos o más lóbulos cerebrales.
Las células neoplásicas invaden los tractos de mielina pero los axones y las neuronas sobreviven lo que hace que la citoarquitectura se mantenga,
por lo que no produce a penas efecto masa.
La barrera hematoencefálica se mantiene íntegra en la mayoría de los casos por lo que no hay un realce de la lesión tras la administración de contraste.
Este comportamiento (las características que han sido resaltadas en cursiva) tiene una traducción en las manifestaciones radiológicas.
En la Tomografía Computarizada(TC) pueden ser hallazgos tan sutiles como asimetría en el tamaño de los ventrículos y una hipodensidad que dificulta la diferenciación entre sustancia blanca y gris sin o poco efecto masa y con buena deliniación de la zona tumoral con respecto al cerebro sano.
Estos hallazgos podemos encontralos tanto en una lesión isquémica como en un tumor astrocitario grado II.
En la lesión isquémica se restringe la Difusión, en cambio en el caso de la GC y el astrocitoma grado II no se restringe la Difusión habitualmente.
Además en la GC no suele mostrar realce tras la administración de contraste y en una lesión isquémica puede tener un realce giral desde el 3º-4º día y persistir semanas aunque si este realce se mantiene más allá de la 6º semana hay que descartar que no se trate de otra patología.
En cambio en el astrocitoma grado II tampoco capta contraste como en la GC.
TABLA 1.
| |
GC |
Astrocitoma gradoII |
Lesión isquémica |
| DIFUSION |
No restringe |
No restringe |
Restringe |
| REALCE |
No realza |
No realza |
Realza |
DIAGNOSTICO DIFERENCIAL
El establecimiento de la clínica también nos ayuda al diagnóstico diferencial con la isquemia ya que en ésta la presentación es aguda y en la GCes más larvada.
Con lo dicho hasta ahora en una lesión isquémica será la secuencia de DIFUSION por la que podremos hacer el diagnóstico diferencial en el momento agudo ya que no habrá todavía captación de contraste i.v.. y en la isquemia se produce restricción de la DIFUSION mientras que en la GC no.
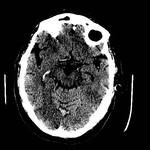
Fig.
1: TC de isquemia en territorio de la cerebral posterior derecha.
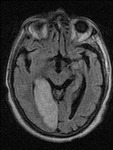
Fig.
2: secuencia FLAIR de la isquemia en fase subaguda.Fig. 2
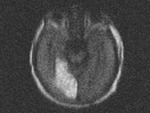
Fig.
3: secuencia de DIFUSION b-1000.Fig.
15
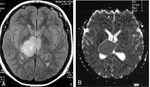
En la Fig.
4 mostramos un astrocitoma de bajo grado en secuencias FLAIR y ADC y como hemos señalado en la tabla 1 el diágnostico diferencial resulta díficil.
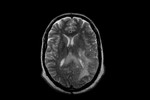
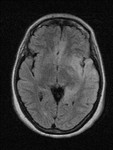
Bien es cierto que en la GC la afectación es más difusa y unos de los criterios para el diagnóstico es que haya una afectación de dos o más lóbulos cerebrales como el caso que presentamos de un varón de 52 años que ingresó en nuestro Centro por convulsiones del que presentamos imágenes de RM en secuencias T2,
FLAIR y DIFUSION b-1000.
El equipo de resonancia de nuestro centro es:SIEMENS,
0,2 Teslas,
abierta.
Fig.
5 secuencia T2.
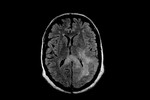
Fig.
6 secuencia FLAIR.
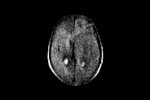
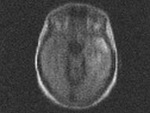
Fig.
7 secuencia DIFUSION b-1000.
Este paciente es la representación típica de una GC primaria tipo I,
la forma más frecuente de presentación de esta infrecuente patología.
Llegado este punto la espectroscopia nos ayudará al diagnóstico diferencial entre el astrocitoma de bajo grado y la GC.
La espectroscopia permite una medida relativa de los metabolitos de interés en el parénquima cerebral.
Los metabolitos más importantes son el NAA(n-acetetil-aspartato),
Colina(Cho),
Creatina(Cr),
Mio-inositol(mI),
Lactato(Lac) y Lípidos.
El NAA es un marcador muy sensible de la integridad neuronal,
por lo que disminuye ante cualquier agresión neuronal.
La Cho es un índice de replicación neuronal,
luego asciende en cualquier proceso tumoral.
La Cr es un metabolito que se mantiene relativamente estable por lo que se utiliza de referencia para otros metabolitos.
El mI es un metabolito localizado en los astrocitos y no se sabe su función exacta.
El Lac se genera en situaciones de glucolisis anaerobia como abscesos,
isquemia y necrosis tumoral.
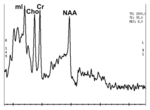
Fig.
8: representación gráfica de una espectroscopia de tejido cerebral normal.
La espectroscopia nos revela los cambios metabólicos por lo que ayuda en el diagnóstico de la progresión tumoral,
determinación del grado de malignidad y respuesta al tratamiento,
ya que es indistinguible por imágenes convencionales la radionecrosis de la recidiva tumoral.
Se establecen unos cocientes:NAA/Cr,
Cho/Cr,
mI/Cr de tal manera que cuanto menor sea el cociente de NAA/Cr mayor destrucción neuronal y en el caso de Cho/Cr cuanto mayor sea el cociente mayor recambio celular de tal manera que a mayor grado de malignidad menor nivel de NAA y mayor de Cho.
En la GC se han descrito mayores niveles de Cr y mI que en un espectro normal aunque también ocurre en el astrocitoma de bajo grado pero también hay una cierta disminución de NAA y aumento de Cho.
Fig.
9: espectroscopía típica de GC.
La GC puede ser confundida desde un punto de vista radiológico y clínico con la encefalitis bien viral o límbica siendo también difícil el diagnóstico entre ellas.
En las encefalitis se afectan los lóbulos temporales,
en la herpética se afectan de forma asimétrica y suele afectarse las regiones frontobasales y circunvolución cingular.
En su evolución puede haber fenómenos hemorrágicos.
En la encefalitis límbica es muy infrecuente los fenómenos hemorrágicos.
En ambas encefalitis pueden tener captación de contraste i.v.
y restringir la DIFUSION,
fenómenos que no suelen ocurrir en la GC. Presentamos un caso de nuestro centro que tuvo una evolución favorable con tratamiento antiviral.
Fig.
10: secuencia FLAIR de encefalitis herpetica.
Fig.
11: secuencia DIFUSION b-1000.
Fig.
12: secuencia T1 con contraste i.v.
Nosotros tuvimos un paciente que se sospechó de encefalitis límbica por afectación en corteza de lóbulos temporales de forma asimétrica,
hipocampos y tálamos con mínima restricción de la DIFUSION que con la evolución acabó presentando una masa en cuerpo calloso con realce de contraste.
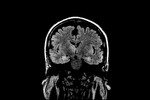
Fig.
13: secuencia FLAIR coronal.
Fig.
14: secuencia DIFUSION b-1000.
Con estas primeras imágenes que acabó de mostrar no se sospechó la posibilidad de una GC lo que retrasó el diagnóstico.
En posterior estudio realizado un mes después ya se demostró una masa hipercaptante en el cuerpo del cuerpo calloso que no restringia la DIFUSION,
por lo que ya se sospechó una GC primaria tipo II.
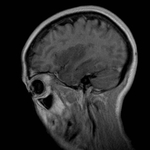
Fig.
15: secuencia sagital T1 tras la administración de contraste i.v.
Fig.
16: secuencia DIFUSION b-1000.
Los tres casos que hemos tenido en nuestro centro uno de ellos como GC primaria tipo I y los otros dos tipo II,
fallecieron al poco tiempo de la confirmación histológica.
BIBLIOGRAFIA:
1.
Nevin S.
Gliomatosis cerebro.
Brain,1938;61:170-91.
2. Yip M.,
Fisch C.,
Lamarche J.B.
AFIP archives: gliomatosis cerebri affecting the entire neuroaxis.
Radiographics 2003;23(1):247-53.
3.
Novillo López M.E.,
Gómez-Ibañez A.,
Rosenfeld M.,
Dalman J.
Gliomatosis cerebral: estudio de 22 pacientes.
Neurología 2010;25(3):168-73.
4.
Al-Okaili RN.,
Kreiza J.,
Wang S.,
Woo J.H.,
Melhem ER.Advanced MR imaging techniques in the diagnosis of intraaxial brain tumors in adults.
Radiographics 2006;26 Suppl:S173-89.
5.
Yang S.,
Wetzel S.,
Law M.,
Zaq zaq D.,
Cha S.
Dynamic contrast-enhaced T2*-weighted MR imaging of gliomatosis cerebri.
AJNR 2002;23(3):350-5.
6.
Méndez-Cendón J.C.
Aplicaciones clínicas de la espectroscopia in vivo en el estudio de los astrocitomas.
Neurocirugía 2004;15(3):258-68.
7.
Santos S.,
López- García E.,
Ríos C.,
Espada- Oliván F.,
Iñiguez-Martínez C.,
Mostacero E.,
Ramón y Cajal S.,
Morales F.
Gliomatosis cerebral.
Presentación de tres casos y revisión de la literatura.
Rev.
Neurol.
2002 Feb 1-15;34(3):248-52.
8.
Bruna J.,
Velasco R.
Gliomatosis cerebri.
Neurología 2010; 25(3):143-47.
9.
Taillibert S.,
Chodkiewicz C.,
Laigle-Donadey F.,
Napolitano M.,
Cartalat-Carel S.,
Sanson M.
Gliomatosis cerebri: a review of 296 cases from the ANOCEF database and the literature.
J.
Neuroocol,
2006;76(2):201-5.
10.
Ladrón de Guevara J.F.,
García-Moncó J.C.,
Polo Esteban J.M.,
González- Mandly A.,
Val-Vernal J.F.
Encefalopatía subaguda de evolución fatal.
Acesso:http//www.
Patología.es/volumen35/vol35-num4/35-4n3 l.htm.