La neumonía organizada criptogenética (NOC) pertenece al grupo de las neumonías intersticiales idiopáticas (NII) que actualmente agrupa 7 entidades Table 1 . El término NII,
propuesto por primera vez por Liebow y Carrington,
en 1983 se aplica a un grupo de trastornos pulmonares que comparten aspectos histológicos y radiológicos característicos,
pero que carecen de una causa conocida1.
La publicación en 2002 del documento de consenso internacional multidisciplinario auspiciado por la American Thoracic Society (ATS) y la European Respiratory Society (ERS),
ha permitido la elaboración de una nueva clasificación de este complejo grupo de enfermedades,
destacando la importancia de establecer una adecuada correlación clínico-radio-patológica2.
Como consecuencia de esta clasificación de la ATS/ECR se ha sustituido el término de bronquiolitis obliterante con neumonía organizada (BONO) por el de NO ya que la afectación es sobre todo alveolar y el bronquiolo rara vez se afecta,
y además creaba confusión con la broquiolitis obliterante.
ETIOPATOGENIA
La NO es una enfermedad pulmonar poco frecuente,
con una prevalencia de 12/100.00 ingresos hospitalarios3.
Es la tercera NII en frecuencia.
La edad media de los pacientes es de 55 años y la incidencia por sexos es similar.
Hasta en un 50% de los casos se ha podido constatar un antecedente de un cuadro pseudogripal en los días previos,
seguido de la enfermedad que suele cursar con tos no productiva y persistente,
disnea de esfuerzo,
malestar general,
fiebre y pérdida de peso.
Su duración varía entre una semana y varios meses.
En aproximadamente el 50% de los casos es de etiología desconocida y se denomina neumonía organizada criptogenética (NOC)4. En el resto de los casos la neumonía organizada es secundaria a otros procesos5 Table 2 .
Entre ambos grupos no se han encontrado características distintivas ni clínicas,
ni radiológicas,
ni tampoco desde el punto de vista histológico.
Sin embargo,
sí hay diferencias en cuanto al pronóstico,
de manera que las formas secundarias presentan en general un peor pronóstico que la NOC6.
Las causas de NO secundaria más frecuentes en la práctica clínica son las colagenosis (especialmente la dermatomiositis/polimiositis y la artritis reumatoide),
los fármacos Table 3 y el trasplante de médula ósea y de pulmón.
El diagnóstico de NO requiere un consenso entre clínicos,
radiólogos y patólogos puesto que pueden encontrarse focos de neumonía organizada asociados a múltiples procesos pulmonares tales como infecciones y tumores2.
En la mayoría de los casos la NO presenta un buen pronóstico,
con recuperación completa tras el tratamiento con corticoides.
En ocasiones puede resolverse de forma espontánea.
Por otra parte,
se ha registrado una tasa de recaídas del 15%,
sobre todo en los 3 primeros meses y tras suspender la corticoterapia7.
PATRÓN HISTOLÓGICO
Desde el punto de vista histológico,
la NO se puede considerar como una respuesta inespecífica del pulmón frente a una agresión,
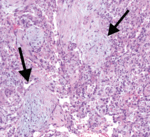
caracterizada por la aparición de células inflamatorias y tejido conectivo organizado en el interior del espacio aéreo distal (bronquíolos,
conductos alveolares y alvéolos) Fig. 1.
La distribución es parcheada,
y por lo general,
la arquitectura pulmonar queda preservada.
Habitualmente el diagnóstico histológico se realiza mediante biopsia transbronquial,
teniendo que recurrir en caso de duda a la biopsia pulmonar quirúrgica.
Existe alguna controversia con respecto a su clasificación como NII,
ya que la afectación es más del espacio aéreo que del intersticio.
Sin embargo,
su naturaleza idiopática y su asociación con colagenopatías así como la posibilidad de presentar hallazgos superponibles con otras NII,
sobre todo con la neumonía NIA,
hace que se haya incluido en la clasificación de la ATS/ERS dentro de las NII.
PATRONES RADIOLÓGICOS
La tomografía axial computarizada de alta resolución (TACAR) es la técnica de elección para orientar el diagnóstico de sospecha.
Es una herramienta muy útil tanto para sugerir el diagnóstico como para seguir la evolución de la enfermedad8.
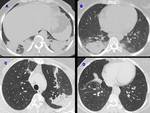
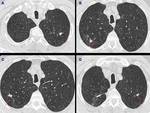
- El patrón radiológico más característico y frecuente (60-80%) son las opacidades alveolares bilaterales,
periféricas y parcheadas.
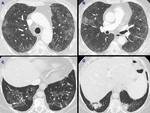
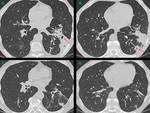
La densidad de estas opacidades puede variar desde la verdadera condensación Fig. 2 hasta la opacidad en vidrio deslustrado Fig. 3 .
La consolidación no suele ser segmentaria,
a menudo sigue una distribución peribronquial o subpleural y tiende a ser migratoria.
Algunas series han descrito un predominio de la afectación en los lóbulos inferiores.
(Tabla 4) En nuestro estudio hallamos 18 casos de consolidaciones y 9 casos de opacidad en vidrio deslustrado.
Hasta en el 10-50% de los casos,
se han encontrados otros hallazgos radiológicos "atípicos",
bien de forma aislada o asociados a las consolidaciones.
Dentro de estos hallazgos se pueden enumerar:
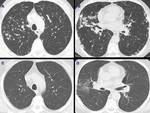
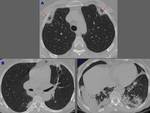
- Nódulos pulmonares: Puede visualizarse un nódulo o incluso una masa pulmonar solitaria o múltiples nódulos con un tamaño variable que oscila entre escasos milímetros a 3 cm. Fig. 4 y Fig. 5 .
Habitualmente son de bordes lisos,
bien definidos,
de distribución simétrica y aleatoria.
En nuestro estudio encontramos 15 casos con este hallazgo: en 4 de estos pacientes se describieron nódulos mayores de 5 mm y en 1 caso se identificó una masa pulmonar.
- Afectación reticular con engrosamiento septal que se asocia a una peor respuesta terapéutica con mayor probabilidad de desarrollar una fibrosis pulmonar.
En nuestra serie se identificaron 4 casos de engrosamiento septal y 2 de ellos con fibrosis pulmonar asociada.
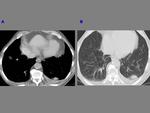
- Derrame pleural uni-bilateral Fig. 6 .
En nuestra serie se objetivaron 5 casos.
- Cavitación de las consolidaciones en relación con sobreinfecciones o vasculitis asociadas Fig. 7 .
Nosotros encontramos 3 casos de los 17 que presentaban consolidaciones.
- Otro hallazgo atípico descrito en la literatura que hemos identificado en nuestro estudio ha sido 1 caso de halo invertido9 Fig. 8 .
DIAGNÓSTICO DIFERENCIAL
El diagnóstico diferencial dela NOincluye una serie de procesos que pueden presentarse con un cuadro clínico-radiológico similar.
El diagnóstico definitivo requiere la valoración conjunta de los datos clínicos,
radiológicos y anatomopatológicos.
En el diagnóstico diferencial clínico-radiológico se incluyen fundamentalmente:
- Infecciones pulmonares: bacterianas,
micobacterianas
- Neumonía eosinófila crónica
- Vasculitis granulomatosas
- Sarcoidosis
- Neoplasias: adenocarcinoma,
linfoma
En la práctica diaria,
la sospecha diagnóstica inicial ante unas opacidades alveolares bilaterales es la de una bronconeumonía,
por lo que el paciente recibe tratamiento con antibióticos,
sin que el cuadro remita.
Cuando el patrón radiológico de presentación de la enfermedad es el de múltiples nódulos de gran tamaño,
debe excluirse la posibilidad de linfoma o de adenocarcinoma.
Por otra parte,
la posibilidad de que estas consolidaciones tengan un carácter migratorio o alcancen la regresión espontánea,
plantean otras alternativas como la neumonía eosinófila,
la hemorragia pulmonar y las vasculitis pulmonares10.
Desde el punto de vista anatomopatológico puede existir confusión entre NOC y neumonía intersticial usual (NIU).
La diferencia fundamental radica en que ambas presentan una afectación pulmonar parcheada,
sin embargo,
este infiltrado en la NIU se dice que es temporalmente heterogéneo (alternan zonas de pulmón sano con inflamación,
fibrosis etc...),
mientras que en la NOC es temporalmente homogéneo. En este caso es fundamental ya que el pronóstico en la NOC es favorable y responde a una terapia,
no así en el caso de la NIU.
BIBLIOGRAFIA
- Davidson AG,
Heard BE,
McAllister WA,
Turner-Warwick ME.
Cryptogenic organizing pneumonitis.
Q J Med 1983; 52: 382-394.
-
American Thoracic Society/European Respiratory
Society International Multidisciplinary Consensus
Classification of the Idiopathic Interstitial Pneumonias.
Am J Respir Crit Care Med,
2002; 165: 277–304.
-
Alasaly K,
Müller N,
Ostrow DN.
Cryptogenic organizing pneumonia.
A report of 25 cases and a review of the literature.
Medicine 1995; 74: 201-211.
-
Epler GR,
Colby TV,
McLoud TC,
Carrington CB,
Gaensler EA.
Bronchiolitis obliterans organizing pneumonia.N EnglJ Med,
1985; 312: 152-158.
-
Hansell D,
Armstrong P,
Lynch DA,
Page H.
Imaging of diseases of the chest.
In: David Hansell et al,
editors.
Elsevier,Oxford.
2005; 553-610.
-
Lee J,
Lynch D,
Sharma S.
Organizing pneumonia: prognostic implication of high resolution-CT features.
J Comput Assist Tomogr 2003; 27:260-65.
-
Robert H.
Lohr,
Benoit J.
Boland,
William W.
Douglas,
David H.
Dockrell,
Thomas V.
Colby,Stephen J.
Swensen,
Peter C.
Wollan,
Marc D.
Silverstein.
Organizing pneumonia.
Features and prognosis of cryptogenic,
secondary and focal variants.
Arch Intern Med 1997; 157: 1323-1329.
-
GotwayMB,
Reddy GP,
Webb WR,
Elicker BM,
Leung JW.
High-resolution CT of the lung: patterns of disease and differential diagnoses.
Radiol Clin North Am,
2005; 43(3):513-542.
-
Kim SJ,
Lee KS,
Ryu YH,
Yoon YC,
Choe KO,
Kim TS,
Sung K.J.
Reversed halo sign on high-resolution CT of cryptogenic organizing pneumonia: diagnostic implications.
AJR.
2003; 180:1251-4.
-
Benjamin J.
Roberton,
David M.
Hansell.
Organizing pneumonia: a kaleidoscope of concepts and morphologies.
Eur Radiol 2011,
21: 2244-2254.