1.INTRODUCCIÓN
Las neoplasias hepáticas,
ya sean primarias o secundarias,
constituyen un importante problema asistencial debido tanto a su incidencia como a su refractariedad al tratamiento,
morbilidad y mortalidad asociadas.
El CARCINOMA HEPATOCELULAR (CHC) supone el 80% de las neoplasias hepáticas primarias y es uno de los tumores malignos más frecuentes.
Actualmente representa más del 5% de las neoplasias en todo el mundo.
El desarrollo del CHC está vinculado fundamentalmente con la exposición a factores víricos como la infección por el virus de la hepatitis B y el de la hepatitis C.
La presencia y grado de la enfermedad hepática previa es el factor de riesgo más importante para el desarrollo del CHC y,
así,
el 90% surgen en hígados cirróticos,
sea cual sea su etiología.
Es un tumor con una elevada mortalidad,
constituyendo la primera causa de muerte en la población de pacientes cirróticos y la tercera asociada a cáncer.
Las NEOPLASIAS HEPÁTICAS SECUNDARIAS son,
incluso,
más frecuentes que los tumores primarios y se observan en más del 40% de los pacientes que mueren por cáncer.
El hígado constituye la localización más frecuente de metástasis de origen gástrico,
mamario,
pulmonar y,
especialmente,
colorrectal.
El 50% de los pacientes con tumores colorrectales desarrollan metástasis hepáticas a los cinco años del diagnóstico inicial.
Sin embargo,
son numerosos los casos en los que las metástasis hepáticas se descubren ya en el momento del diagnóstico del tumor primario.
Dichas lesiones y la disfunción hepática que conllevan son la causa más importante de morbilidad y mortalidad de los pacientes con neoplasias gastrointestinales y de otros orígenes primarios.
La resección quirúrgica constituye el tratamiento estándar con intención curativa de los pacientes con neoplasias hepáticas,
ya sean primarias o secundarias,
al que se suma el trasplante hepático en el caso del CHC.
Sin embargo,
sólo una minoría de pacientes (aproximadamente un 20%) son susceptibles de las mismas.
En la mayoría de los casos,
la presencia de enfermedad multifocal,
enfermedad extrahepática,
escasa reserva funcional hepática o existencia de comorbilidad contraindican la cirugía.
En este grupo de pacientes el manejo de las lesiones hepáticas ha sufrido un importante cambio en los últimos años debido al desarrollo de terapias antitumorales mínimamente invasivas,
que buscan lograr el máximo grado de necrosis tumoral,
basándose en el principio de que la reducción del volumen tumoral o la prevención de un nuevo crecimiento podría mejorar el pronóstico.
Estos procedimientos se conocen globalmente con el nombre de técnicas de ablación tumoral y hacen referencia a la aplicación directa de un tratamiento,
ya sea químico o térmico,
en el interior de la lesión,
guiado con técnicas de imagen:
- Técnicas de ablación química: Inyección de sustancias químicas en el interior del tumor,
como son el etanol,
ácico acético,
suero salino caliente y agentes quimioterápicos
- Tecnicas de ablación térmica (termocoagulación): láser,
radiofrecuencia (RF),
microondas y ultrasonidos de alta intensidad de maneral focal con aplicación de calor,
y crioablación con aplicación de frío.
De todas ellas,
los más difundidos en la actualidad son la inyección de etanol y la radiofrecuencia,
basados en el coste bajo,
la eficacia y la simplicidad técnica.
En los últimos años,
la RF ha ido ganando terreno a la inyección de etanol,
debido a su capacidad para tratar una mayor variedad de tumores y de mayor tamaño,
su versatilidad para emplearse sóla o asociada a otros procedimientos terapeúticos (como la cirugía abierta o laparoscópica,
embolización portal,
quimiembolización,
alcoholización,
etc) y la posibilidad de repetición tantas veces como sea necesario.
Gracias a estas nuevas técnicas,
y,
en especial,
a la RF,
ya sea sóla o combinada con otras terapias,
se ha abierto ampliamente el abanico de pacientes susceptibles de tratamiento con intención curativa,
cerrado hasta ahora exclusivamente a aquellos que eran candidatos a cirugía.
A pesar de que la RF ha sido ampliamente introducida en la práctica clínica diaria,
no se conoce con exactitud su papel real en el manejo de los tumores hepáticos,
dado que ni su eficacia ni su seguridad clínicas están aún claramente definidas.
2.ASPECTOS TÉCNICOS
♦ Proceso Físico
La RF se basa en ondas electromagnéticas que pertenecen al dominio de las radioondas,
producidas por el paso de una corriente alterna a través de un electrodo,
que es insertado bajo control radiológico en la lesión tumoral.
En el interior de los tejidos estas ondas producen una agitación de los iones celulares,
que crea una fricción a nivel molecular y ocasiona un incremento de la temperatura intracelular que origina la desnaturalización de las proteínas y la disolución de la bicapa lipídica de membrana,
con la consiguiente destrucción celular y necrosis coagulativa del tejido. Las células tumorales son más sensibles a la ablación por calor que el parénquima hepático sano circundante.
El daño térmico a nivel celular es directamente proporcional a la temperatura alcanzada por el electrodo y la duración de la aplicación,
así se considera que la temperatura citotóxica,
es decir,
la temperatura mínima a la que debe ser sometido todo el volumen tumoral durante toda la duración del tratamiento para obtener una necrosis adecuada es superior a 45-50°.
Una temperatura de 50-55ºC durante 4 a 6 minutos ocasiona un daño celular irreversible.
A medida que la temperatura empleada aumenta,
el tiempo necesario para conseguir la necrosis disminuye.
Así,
con una temperatura de 60-100 º C la necrosis es inmediata y con temperaturas superiores a 100º C se consigue la evaporación y carbonización del tejido; sin embargo,
este efecto disminuye la difusión del calor desde la aguja hasta el resto de la masa tumoral,
lo cual es negativo para el adecuado desarrollo de la necrosis coagulativa deseada en la radiofrecuencia.
♦ Sistemas de Aplicación de Energía
El sistema a través del cual se realiza la RF consiste en un generador externo o fuente,
que es el productor de energía,
desde el que se transmite la corriente eléctrica a una o más agujas o electrodos,
que son los que se colocan en el seno del tumor que se quiere tratar.
Estos electrodos están aislados eléctricamente,
excepto en su porción distal,
para que la corriente pueda ser transmitida al tejido.
Generalmente,
las agujas/electrodos empleadas tienen un calibre de 14-15 G.
Los generadores empleados suelen tener una potencia que oscila entre 50 y 200 W,
y producen una corriente oscilante de alta frecuencia (400-500 KHz).
Existen dos sistemas fundamentales para la aplicación de la radiofrecuencia,
los circuitos monopolares y los bipolares (Fig. 1 y Fig. 2).
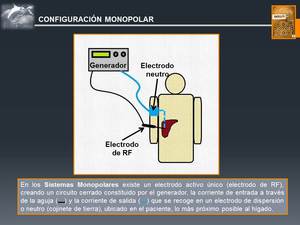
Fig. 1: Configuración Monopolar
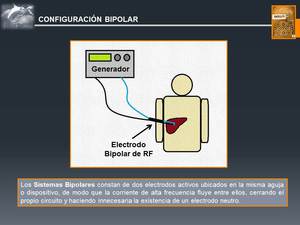
Fig. 2: Configuración Bipolar
El volumen de ablación está limitado por dos factores:
- La dispersión del calor,
que hace que la necrosis se produzca sólo en un diámetro de 1’5 cm alrededor del electrodo.
- El calentamiento del tejido alrededor del electrodo tiende a desecarlo,
aumentando su impedancia a la transmisión de la energía y reduciendo el grado de necrosis logrado.
El desarrollo tecnológico ha permitido superar estos problemas técnicos mediante la creación de diferentes tipos de electrodos, entre los que destacan los electrodos enfriados internamente,
los electrodos perfundidos y los electrodos multipolares. (Fig. 3)
En nuestro centro la ablación tumoral se realiza mediante un sistema de radiofrecuencia bipolar,
con un electrodo que está provisto de un circuito interno cerrado de infusión de suero salino,
a un flujo de 30 ml/min,
y con un generador que obtiene un pico de potencia de 250 W.
Los electrodos tienen un calibre de 15 G con agujas de diferentes longitudes y distintos volúmenes de ablación.
(Fig. 4)
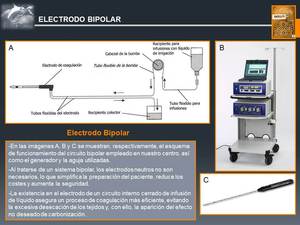
Fig. 4: Electrodo Bipolar
References: Olympus 2012.Celon Power System y Celon Prosurge
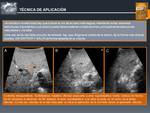
♦ Técnica de Aplicación
El tamaño y la forma del volumen de coagulación que se puede conseguir dependen de:
- Geometría del electrodo
- Cantidad y orden en que se disponen los electrodos
- Potencia y duración de la aplicación
Dependiendo del tipo de aguja utilizado,
el tamaño de necrosis variará generalmente entre 2 y 4 cm en una única inserción.
Para el tratamiento de tumores mayores es necesario emplear múltiples electrodos o dispositivos que permitan abarcar un radio mayor.
El OBJETIVO FINAL es conseguir la necrosis completa de la masa tumoral con un margen peritumoral circunferencial,
que,
siguiendo los criterios oncológicos de resección,
debe ser de,
al menos,
1 cm.
Por todo ello,
es muy importante que,
antes de comenzar,
se tenga perfectamente planificado,
en función de la forma y el tamaño de la lesión a tratar y la vía de abordaje seleccionada,
el tipo de aguja,
la cantidad necesaria de las mismas y el modo en que las vamos a colocar.
(Fig. 5)
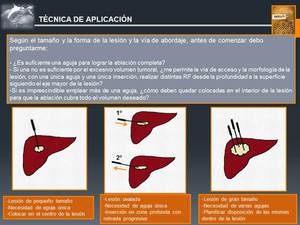
Fig. 5: Técnica de Aplicación
Con la ayuda del método de imagen seleccionado,
el electrodo o electrodos se colocan adecuadamente en el interior de la lesión,
evitando entrar y salir repetidamente del tumor,
para disminuir el riesgo de siembra tumoral y de sangrado.
Una vez colocado,
se aplica la corriente desde el generador y se sigue el protocolo recomendado por el fabricante (Fig. 6).
Cada sistema tiene su propio protocolo para determinar cuándo se finaliza el tratamiento.
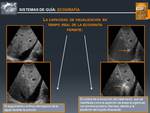
Existen dos tipos diferentes:
- Sistemas basados en el tiempo de tratamiento: la ablación se mantiene durante un tiempo determinado una vez alcanzada la temperatura intralesional prefijada.
- Sistemas basados en la impedancia: el tratamiento se mantiene hasta que se produce un aumento brusco en la resistencia a la transmisión de la corriente eléctrica,
que indica que ya se ha obtenido la necrosis.
Para el tratamiento de una lesión es suficiente una única sesión de RF,
a diferencia de otras técnicas percutáneas como la inyección de etanol.
En el mismo acto puede realizarse la ablación de varias lesiones,
repitiendo para cada una de ellas los pasos que hemos descrito previamente.
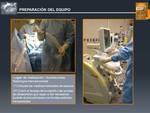
♦ Lugar de Realización
El procedimiento de radiofrecuencia debe llevarse a cabo en un quirófano o en una sala de radiología intervencionista adecuadamente equipada.
Deben tomarse todas las medidas habituales de asepsia,
al igual que en cualquier otra intervención quirúrgica.
El ecógrafo y las sondas deben ser recubiertas con fundas transparentes especiales estériles.
(Fig. 7)

Fig. 7: Preparación del Equipo
En cuanto al grado de anestesia necesario,
la anestesia local no suele ser suficiente para un control adecuado del dolor.
Generalmente se realiza bajo una sedación consciente asociado con anestesia local en los casos por vía percutánea o anestesia general cuando la vía es la laparotomía o laparoscopia; siendo siempre indispensable la presencia de un anestesista.
En nuestro centro,
la ablación por RF SIEMPRE se realiza en el quirófano,
con presencia de un médico anestesista y de cirujanos,
independientemente de que la vía de acceso a la lesión vaya a ser percutánea o por laparotomía.
Gracias a esta estrecha colaboración y ayuda mutua entre radiólogos y cirujanos,
conseguimos minimizar al máximo la aparición de complicaciones y es posible,
en el mismo momento,
modificar la actitud terapéutica y cambiar la vía de acceso del procedimiento si las circunstancias así lo precisan.
3.
TÉCNICAS DE IMAGEN
Las técnicas de imagen van a ser necesarias en momentos diferentes del proceso de ablación.
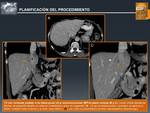
♦ Planificación del Procedimiento
Inicialmente,
para la planificación del procedimiento se van a emplear el TC y la RM.
Con ello,
se van a determinar,
con la mayor exactitud posible:
- Número,
tamaño y localización de las lesiones
- Relación de las lesiones con estructuras anatómicas claves: sistema portal,
vía biliar y tubo digestivo.
(Fig. 8)
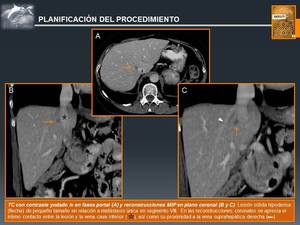
Fig. 8: Planificación del Tratamiento
♦ Sistema de Guía
El sistema de guía empleado para la ablación tumoral puede ser la ecografía,
el TC o la RM.
La ECOGRAFÍA es la técnica más utilizada,
debido a su bajo coste,
amplia disponibilidad y capacidad de visualización en tiempo real (Fig. 9 y Fig. 10).
Pueden utilizarse guías de punción o técnica de manos libres.
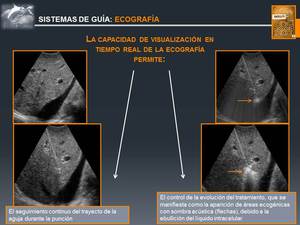
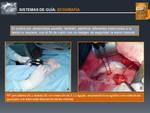
Fig. 9: Sistemas de Guía: ECOGRAFÍA
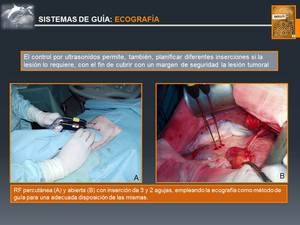
Fig. 10: Sistemas de Guía: ECOGRAFÍA
Además,
otra ventaja que convierte a la ecografía en la técnica de elección es que puede emplearse sea cual sea la vía de acceso seleccionada para el abordaje de las lesiones (percutánea,
laparotomía o laparoscopia).
En este aspecto,
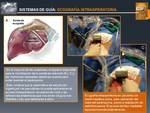
hay que hacer especial mención a la ECOGRAFÍA INTRAOPERATORIA,
cuya metodología difiere en parte de la técnica percutánea,
y requiere de un aprendizaje específico para llevarse a cabo de forma adecuada.
(Fig. 11,
Fig. 12 y Fig. 13)
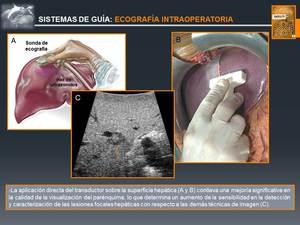
Fig. 11: Sistemas de Guía: ECOGRAFÍA INTRAOPERATORIA
References: John Hopkins Medicine. © M. Gamo Gallego; RADIODIAGNÓSTICO, Hospital Universitario Príncipe de Asturias, Alcalá de Henares, SPAIN
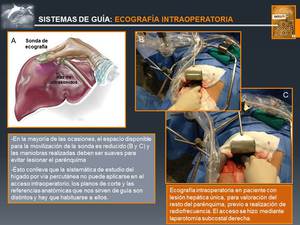
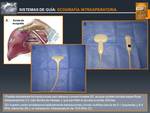
Fig. 12: Sistemas de Guía: ECOGRAFÍA INTRAOPERATORIA
References: John Hopkins Medicine. © M. Gamo Gallego; RADIODIAGNÓSTICO, Hospital Universitario Príncipe de Asturias, Alcalá de Henares, SPAIN
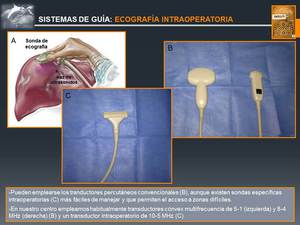
Fig. 13: Sistemas de Guía: ECOGRAFÍA INTRAOPERATORIA
References: John Hopkins Medicine. © M. Gamo Gallego; RADIODIAGNÓSTICO, Hospital Universitario Príncipe de Asturias, Alcalá de Henares, SPAIN
El TC ofrece pocas ventajas con respecto a la ecografía,
puede ser útil en el caso de lesiones no visibles por ecografía,
en lesiones de difícil acceso,
como segmento VII-VIII o muy próximas al tubo digestivo.
La RM ofrecería la ventaja de poder identificar cambios en el tejido como respuesta a la acción coaguladora de la RF y,
por tanto,
poder monitorizar el tratamiento,
sabiendo si al final se ha realizado cobertura del todo el tumor; pero debido a su alto coste,
escasa disponibilidad y necesidad de material específico no ferromagnético,
es una técnica muy poco empleada.
En nuestro centro la RF siempre se realiza empleando la ecografía como método de imagen,
usando la técnica de manos libres.
♦ Eficacia al Tratamiento
Para la valoración de la eficacia al tratamiento las técnicas más empleadas son el TC y la RM.
Aunque no existe un protocolo establecido,
el primer control postablación suele realizarse a las 4 semanas del procedimiento.
No se recomienda realizar estudios de forma precoz,
ya que es muy frecuente la aparición de una captación perilesional debido a fenómenos hiperémicos y a la presencia de tejido de granulación.
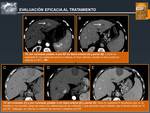
Mediante TC se considera buena respuesta la existencia de una lesión con ausencia de captación de contraste en todas las fases,
que puede ser de mayor tamaño que la lesión inicial (Fig. 14).
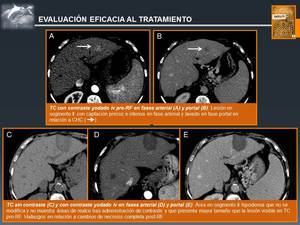
Fig. 14: Evaluación de Eficacia al Tratamiento
Mediante RM las lesiones aparecen hiperintensas en secuencias potenciadas en T1 (por la necrosis coagulativa) e hipointensas en T2 (por la deshidratación),
con ausencia de áreas de captación de contraste.
En fases más tardías,
las lesiones correctamente necrosadas involucionan y disminuyen su tamaño.
En general,
el hallazgo radiológico más importante que sugiere un tratamiento completo es la desaparición de la vascularización tumoral existente previo al tratamiento termoablativo.
4.
VÍAS DE ACCESO
La vía de acceso a las lesiones también presenta varias posibilidades.
Tradicionalmente la radiofrecuencia se ha realizado mediante abordaje percutáneo o vía directa mediante laparotomía; en los últimos años el acceso mediante laparoscopia también está siendo utilizado.
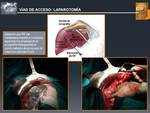
♦ Radiofrecuencia Abierta mediante Laparotomía (Fig. 15 y Fig. 16):
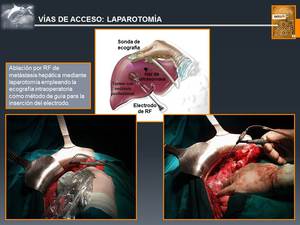
Fig. 15: Vías de Acceso: LAPAROTOMÍA
References: John Hopkins Medicine. © M. Gamo Gallego; RADIODIAGNÓSTICO, Hospital Universitario Príncipe de Asturias, Alcalá de Henares, SPAIN

Fig. 16: Vías de acceso: LAPAROTOMÍA
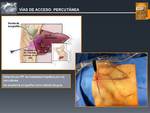
♦ Radiofrecuencia Percutánea (Fig. 17 y Fig. 18)
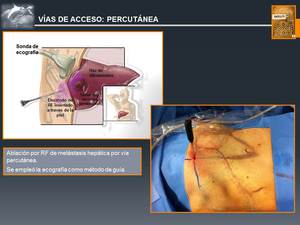
Fig. 17: Vías de Acceso: PERCUTÁNEA
References: John Hopkins Medicine. © M. Gamo Gallego; RADIODIAGNÓSTICO, Hospital Universitario Príncipe de Asturias, Alcalá de Henares, SPAIN

Fig. 18: Vías de Acceso: PERCUTÁNEA
♦ Radiofrecuencia por Laparoscopia
Recientemente introducida para algunos casos de lesiones yuxtavesiculares,
adyacentes a colon o estómago y que no pueden ser tratadas percutáneamente por temor a lesionar estos órganos de vecindad.
Ofrece buenos resultados aunque la complejidad técnica es importante y los medios técnicos necesarios no están disponibles en todos los centros sanitarios.
Con respecto a la radiofrecuencia abierta presenta las ventajas de ser menos invasiva,
con disminución de la estancia hospitalaria y con recuperación precoz del paciente.
Nosotros empleamos la vía percutánea y la laparotomía.
En cada caso,
la vía de acceso se seleccionó en función de la localización anatómica de la lesión y su accesibilidad a la punción percutánea ("ventana ecográfica") y la combinación o no con resección quirúrgica en el mismo acto.
5.
INDICACIONES
En general,
la radiofrecuencia se va a emplear para el control local de los tumores hepáticos primarios y metastásicos en pacientes con enfermedad limitada y no candidatos a cirugía por tamaño,
localización y número de lesiones,
enfermedad extrahepática,
comorbilidad asociada o reserva funcional hepática limitada (por cirrosis o por QT).
En el caso del CHC estas indicaciones están bien establecidas:
- CHC en estadios muy inicial (0) e inicial (A) según el sistema de estadificación BCLC (Barcelona-Clinic-Liver-Cancer) (Fig. 19) cuando los pacientes no son candidatos a cirugía o trasplante.
Los requerimientos necesarios son:
-Lesión única o máximo de 3 lesiones menores de 3 cm cada una
-No evidencia de invasión vascular o diseminación extrahepática
-Paciente asintomático
-Cirrosis hepática en estadios Child-Pugh A o B
- Pacientes con CHC en lista de espera de trasplante para prevenir crecimiento y progresión del mismo cuando el tiempo de espera va a superar los 6 meses.
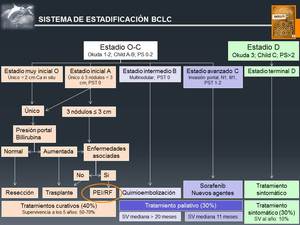
Fig. 19: Sistema de Estadificación del CHC
References: Forner A, Ayuso C, Isabel Real M, Sastre J, Robles R, Sangro B, et al. Diagnosis and treatment of hepatocellular carcinoma. Med Clin (Barc). 2009; 132:272-87
En el caso de las metástasis hepáticas las indicaciones no están bien definidas.
Generalmente la RF se plantea en pacientes no susceptibles de cirugía con metástasis de carcinoma colorrectal limitadas al hígado.
El número de lesiones no debe considerarse una contraindicación absoluta si puede conseguirse el tratamiento adecuado de todos los depósitos metastásicos.
Sin embargo,
la mayoría de los centros establecen el límite en 5-6 lesiones.
En cuanto al tamaño de las lesiones tampoco existen indicaciones concretas.
Está demostrado que los mejores resultados en cuanto a datos de respuesta completa se obtienen en lesiones con tamaño menor o igual a 3 cm,
y que dichos resultados empeoran progresivamente según aumenta el tamaño tumoral.
Es importante recordar el papel fundamental de la RF en el tratamiento de las metástasis de origen colorrectal en 2 situaciones:
-Como complemento a la resección quirúrgica en lesiones no accesibles a la misma
-Como terapia de rescate tras quimioterapia en lesiones y pacientes que previamente no eran susceptibles de cirugía ni ablación
En nuestro centro,
resultado de la experiencia propia,
se ha determinado el límite para realizar radiofrecuencia en un máximo de 6 en cuanto al número de metástasis y de 6 cm en cuanto al tamaño,
siempre que la reserva funcional hepática que vaya a quedar de forma residual sea adecuada y suficiente.
También se ha empleado la RF para el tratamiento de metástasis hepáticas de otros tumores primarios (neuroendocrinos,
esófago,
pulmón,
mama y páncreas),
generalmente en pacientes con enfermedad exclusiva hepática,
que se benefician de la citorreducción del tumor cuando otros tratamientos han fracasado.
6.CONTRAINDICACIONES y PRECAUCIONES PREPROCEDIMIENTO
Existen muy pocas condiciones que supongan una contraindicación absoluta para la realización de un procedimiento de radiofrecuencia.
Sin embargo,
existen determinados factores o situaciones especiales que conllevan un mayor riesgo de desarrollar complicaciones y que,
por lo tanto,
deben ser analizados y tenidos en cuenta antes de decidir la posibilidad de llevarla a cabo y bajo que tipo de precauciones específicas.
A continuación,
vamos a describir tanto las contraindicaciones absolutas como esas situaciones,
que,
como hemos comentado,
constituirán o no una contraindicación según la evaluación concreta de cada paciente en particular.
(Fig. 20)
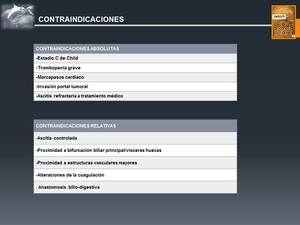
Fig. 20: Contraindicaciones
References: Valls C. et al. Ablación por radiofrecuencia de tumores hepáticos. Radiología, 2006; 48(2):53-69
♦ Portador de Marcapasos
Constituye una contraindicación absoluta debido al riesgo de interferencia con las ondas de RF.
♦ Trastorno de Coagulación
La realización de cualquier intervención sobre el hígado conlleva un riesgo de sangrado que,
en el caso de pacientes con hepatopatía,
aumenta significativamente.
De hecho,
las alteraciones de la coagulación constituyen la contraindicación más frecuente para la realización de una RF.
Por ello,
a todos los pacientes hay que realizarles un estudio de coagulación completo antes del procedimiento,
incluyendo tiempo de protrombina,
recuento plaquetario e índice normalizado internacional (INR).
Los valores aceptados como normales son aquellos usados para otros procedimientos intervencionistas que son tiempo de protrombina > 50%,
INR < 1’3 y plaquetas > 50.000/ml.
Las alteraciones de estos parámetros no suponen una contraindicación absoluta,
pero requieren llevar a cabo ciertas actuaciones para tratar de corregirlas y así permitir la realización de la radiofrecuencia,
como son la administración de plaquetas,
vitamina K o plasma fresco.
En pacientes con coagulopatía o tratamiento anticoagulante,
los análisis deben obtenerse menos de 24 horas antes de realizar la RF.
En pacientes con tratamiento antiagregante o anticoagulante debe suspenderse la medicación el tiempo establecido para cada uno de ellos.
Por todo ello,
los trastornos de la coagulación no suponen una contraindicación absoluta,
pero siempre hay que valorar minuciosamente su estado,
especialmente en pacientes con patología hepática basal,
y en casos de alteraciones severas de la coagulación,
no susceptibles de corrección,
si que supondrían una contraindicación absoluta para la realización de la RF.
♦ Ascitis Clínica a pesar de Tratamiento Médico
La ascitis no es una contraindicación absoluta,
sin embargo,
al ser un indicador de la función hepática,
debe plantear la idoneidad de llevar a cabo el procedimiento si existe un deterioro severo de la misma.
Si la cuantía de la ascitis es moderada permite realizar la RF de manera habitual.
Si es severa,
puede realizarse previamente una paracentesis evacuadora.
♦ Anastomosis Bilio-Digestiva
La realización de RF en pacientes sometidos previamente a este tipo de intervenciones supone un importante aumento en el riesgo de desarrollar complicaciones infecciosas (abscesos,
sepsis),
debido a que existe una colonización de la vía biliar por gérmenes procedentes del tracto digestivo.
En esta situación debe estudiarse cada caso en particular,
constituyendo en algunos centros una contraindicación absoluta.
♦ Estadio Funcional Hepático Avanzado
Aquellas situaciones en las que,
debido al estadio clínico del paciente,
la actuación sobre el tumor no va a aportar ningún beneficio,
también contraindican el procedimiento.
Por ello,
pacientes con cirrosis en estadio C de Child no son candidatos a dicha terapeútica.
♦ Proximidad de Vísceras Huecas/Vía Biliar Principal:
La proximidad de una lesión con la vesícula biliar o el tubo digestivo puede plantear problemas e implica tener en cuenta una serie de precauciones para evitar la aparición de complicaciones.
La proximidad de la lesión con la VESÍCULA BILIAR no suele constituir una contraindicación,
pero si es necesario ser cuidadoso en la introducción y colocación de la aguja,
evitando la introducción de la misma en el interior de la vesícula.
Es normal el desarrollo de una colecistitis térmica como consecuencia de la irritación térmical local ocasionada por la radiofrecuencia,
pero generalmente es una inflamación leve que se resuelve con tratamiento médico.
En el caso del TUBO DIGESTIVO ocurre algo similar.
Cuando la lesión a tratar está próxima al colon existe un riesgo real de perforación,
especialmente si existen antecedentes de cirugía previa con formación de adherencias locorregionales,
ya que puede inducirse una lesión térmica de la pared del tubo digestivo.
Para la mayoría de los autores,
se considera que un margen de seguridad de 15 mm es suficiente para llevar a cabo la radiofrecuencia.
Existen medidas que pueden ayudar,
como colocar al paciente en decúbito lateral para intentar separar las diferentes estructuras,
o inyectar una solución acuosa de dextrosa al 5% en espacio subhepático,
que actúa como solución protectora de la pared intestinal.
La VÍA BILIAR intrahepática próxima a la lesión no contraindica la radiofrecuencia.
Es habitual encontrar en los controles de imagen postRF dilatación focal de radicales intrahepáticos en la zona de la ablación,
como hallazgo incidental y sin repercusión clínica.
Sin embargo,
la ablación de lesiones próximas al hilio,
constituyen un riesgo potencial de estenosis de la vía biliar.
Se considera que la distancia mínima de la lesión con el hilio hepático debe ser de 1 cm,
si no cumple este criterio,
deben plantearse otras terapias alternativas.
♦ Proximidad de Estructuras Vasculares Mayores
La localización de la lesión próxima a una estructura vascular mayor no supone una contraindicación,
si bien,
es necesario tener en cuenta la posibilidad de tratamiento incompleto de la lesión debido al efecto de lavado del calor de los vasos (heat sink effect).
En diferentes estudios se ha demostrado que el porcentaje de necrosis tumoral completo alcanzado en lesiones próximas a grandes estructuras vasculares es menor que en aquellos tumores sin contacto vascular.
De hecho,
se considera que un vaso de más de 3-4 mm produce una refrigeración tal que las células cercanas al mismo quedan indemnes.
El riesgo de trombosis debido a la radiofrecuencia es mayor en pacientes con cirrosis,
sobre todo si se asocia maniobra de Pringle durante el procedimiento,
aunque está establecido que en vasos de diámetro superior a 3 mm en condiciones normales el riesgo es realmente bajo.
7.
COMPLICACIONES:
Aunque los hallazgos preliminares sugieren que se trata de un procedimiento seguro y efectivo,
estos resultados proceden de estudios con un número de casos muy limitado para establecer la tasa real de complicaciones.
A pesar de los beneficios obtenidos,
la RF es un procedimiento complejo,
y es necesaria una experiencia considerable para llevarla a cabo de forma segura.
En general,
la mortalidad asociada es inferior al 1%,
mientras que su morbilidad oscila entre el 10-15%,
con una tasa de complicaciones mayores que ronda el 8%.
Se han relacionado varios factores con un mayor riesgo de desarrollar complicaciones,
entre los que destacan el tamaño,
la multiplicidad,
el grado de diferenciación histológica y la localización tumorales,
así como el número de inserciones y sesiones necesarias y la experiencia de los profesionales que realizan el procedimiento.
Las complicaciones pueden clasificarse en mayores y menores.
Las primeras se definen como aquellas complicaciones que,
si no se tratan,
pueden comprometer la vida del paciente,
llevar a una importante morbilidad y discapacidad o resultar en una larga estancia hospitalaria.
Las menores pueden requerir tratamiento mínimo o una corta estancia hospitalaria para observación y no conllevan secuelas.
Los efectos adversos se consideran consecuencias comunes perjudiciales que no requieren terapia o prescripción medicamentosa.
También pueden clasificarse en tempranas (< 30 días) y tardías (> 30 días).
Una complicación relacionada con la RF se describe como cualquier problema encontrado dentro del periodo periprocedimiento (30 días),
al igual que complicaciones adicionales identificadas en el seguimiento de imagen y juzgadas como posiblemente causadas por la ablación.
Las complicaciones más frecuentes relacionadas con la ablación por radiofrecuencia son:

Fig. 21: Complicaciones: DOLOR Y FIEBRE

Fig. 22: Complicaciones: HEMORRAGIA
- Complicaciones infecciosas (Fig. 23)

Fig. 23: Complicaciones: COMPLICACIONES INFECCIOSAS
- Perforación intestinal (Fig. 24

Fig. 24: Complicaciones: PERFORACIÓN INTESTINAL
- Complicaciones torácicas (Fig. 25)

Fig. 25: Complicaciones: COMPLICACIONES TORÁCICAS

Fig. 26: Complicaciones: LESIÓN DE LA VÍA BILIAR

Fig. 27: Complicaciones: HEMORRAGIA Y MUERTE

Fig. 28: Complicaciones: SIEMBRA METASTÁSICA