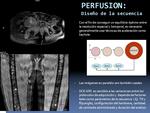
DISEÑO DE LAS SECUENCIAS FUNCIONALES DE RM FUNCIONAL EN LOS TUMORES DE PARTES BLANDAS:
1) SECUENCIAS DE DIFUSION:
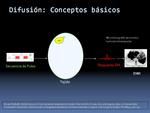
* La secuencia de difusión permite el estudio de los movimientos micoscópicos de las moléculas de agua.
* La RM permite la evaluación del movimiento browniano del agua libre.
La difusión es el resultado de someter un voxel a una secuencia de pulso de difusión.
(Fig 2)
* La secuencia de difusión refleja el comportamiento de la difusión del agua en el organismo.
El movimiento neto de las moléculas de agua se relaciona directamente con el movimiento del agua entre los espacios intra y extracelular y el espacio intravascular.
* La difusión aporta una estimación indirecta de la celularidad tisular y de la integridad de la membrana celular.
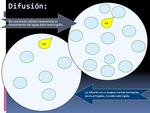
* La difusión en un tejido normal es isotrópica,
como el movimiento del LCR. (Fig.
3).
Cuando las moléculas de agua son forzadas a moverse en una dirección predeterminada,
como es el caso de las fibras nerviosas,
hablamos de una difusión anisotrópica.
* Es posible encontrar restricción de la difusión isotrópica debido a barreras físicas como células,
proteínas....
Este es el caso de los tumores o abscesos.
( Fig.
4)
1.
DISEÑO DE LA SECUENCIA DE DIFUSION:
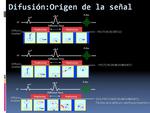
Los parámetros de análisis de la secuencia DWI debe optimizarse con el fin de aumentar la SNR y CNR.
( Figuras 5-7)
Esta secuencia es propensa a los artefactos por movimiento y de susceptibilidad magnética ya que la mayoría de las secuencias de difusión se basan en secuencias EPI.
Como regla general,
la secuencia de difusión convencional tiene una resolución espacial limitada.
Con el fin de aumentar la calidad de esta secuencia se deben seguir varias reglas:
- Uso de secuencias de supresión grasa: el uso de técnicas de supresión grasa nos permite aumentar el rango dinámico de la DWI la reducción del desplazamiento químico por artefactos "gosthing".
Aunque los enfoques de inversión-recuperación,
tales como STIR son útiles para áreas de imagen de gran tamaño,
el uso de saturación selectiva de la grasa es más apropiada (por ejemplo: SPAIR, CHESS ...) para las pequeñas áreas de interés debido a su mejor SNR. Por lo tanto, la supresión selectiva de la grasa es mejor para los estudios de los tejidos blandos
- Minimizar la saturación T1: El TR debe ser suficientemente largo para evitar efectos de saturación de T1, pudiendo dar lugar a valores de ADC falsamente bajos.
- Utilizar TE corto: se puede hacer aumentando el ancho de banda (hasta un máximo de 1500 MHz),
utilizando imágenes en paralelo (factor SENSE hasta 2) y por aumento de la intensidad de gradiente en las antenas de gradiente.
- Aumentar el número de Adquisiciones (NEX).
- Disminuir el campo de visión (FOV) a un mínimo en la dirección de codificación de fase.
- No aumentar la resolución en plano a niveles en los que el ruido aumenta de manera significativa o la calidad de imagen disminuye gravemente,
ya que disminuirá la calidad de los mapas ADC. Aumenta el FOV puede tener un resultado similar.
- Aproximación TRACE/ gradient overplus: El uso de tres gradientes ortogonales al movimiento permite obtener una dirección de difusión única que nos permite mejorar la fuerza de gradiente por la raíz cuadrada de tres. Por lo tanto,
este enfoque reduce la eficacia de TE,
aumenta la susceptibilidad SNR y reduce al mínimo,
el EPI,
o los artefactos de movimiento.
- SNR se puede aumentar mediante el uso de mayor intensidad de campo (imanes 3T),
reduciendo el TE,
aplicando un gradiente de mayor potencia,
utilizando un tren corto EPI,
y el uso de bobinas phase-array con un mayor número de elementos.
B) ASPECTOS TECNICOS DE LA SECUENCIA DE DIFUSIÓN.
Selección de valores b/ Mapas ADC/Modelos IVIM
Actualmente, un valor de b de 1000 s/mm2 se puede conseguir perfectamente,
permitiendo una mejor diferenciación entre lesiones benignas y malignas
Las mediciones de ADC obtenidas con valores de b más altos son generalmente menores que los obtenidos utilizando los valores b más bajos.
Los cálculos de ADC de las lesiones de partes blandas se ven significativamente afectados por los fenómenos de perfusión,
como se ha demostrado en otros órganos. Con el fin de evitar la contaminación parcial de perfusión,
es recomendable evitar valores de b inferiores a 100 s/mm2 en la cuantificación de ADC
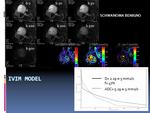
Un enfoque más correcto,
es utilizar el modelo de caída de la señal de difusión del movimiento intravoxel incoherente (IVIM),
también conocido como modelo bicompartimental. Este modelo se ha demostrado que la perfusión microvascular se detecta en los valores de b bajos (inferiores a 100 s/mm2),
permitiendo calcular el parámetro de perfusión libre difusión (D).
Los valores de ADC suelen ser mucho más altos que los valores D,
como se ha demostrado en varios órganos abdominales
En nuestra experiencia,
el modelo IVIM es factible en en los tejidos blandos y músculo,
lo que permite la diferenciación de la difusión y perfusión de los tumores de partes blandas,
aunque si este método mejora la caracterización lesional aún no ha sido demostrado.
Con el fin de aislar el efecto del flujo de sangre a partir de la estimación del coeficiente de difusión,
LeBihan et al propuso el IVIM,
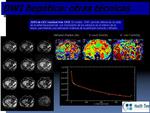
modelo de la señal de difusión. Este modelo separa la caída de la señal de difusión en dos compartimientos de difusión diferentes. Para valores bajos b,
entre 0 y 100 s/mm2,
los experimentos de difusión de señal una caída rápida debido al flujo de sangre a lo largo de la microcirculación,
mientras que para valores de b más altos,
más de 100 s/mm2, la caída de la señal corresponde a la difusión convencional del tejido (Fig 8).
Este modelo ha sido evaluado con éxito en varias patologías,
como tumores cerebrales y cirrosis hepática. La diferencia entre los valores de ADC y D son probablemente secundarios a los efectos de perfusión en la caída de la señal de difusión. Por lo tanto,
el enfoque IVIM permite evitar los efectos de perfusión.
C) DIFUSIÓN HEPATICA: otras técnicas.
IVIM : método desarrollado por Le Bihan et al.,
para evaluar cuantitativamente los movimientos microscópicos de traslación que se producen en cada voxel de la imagen en la RM.
Posteriormente, Le Bihan también demostró que la difusión molecular y microcirculacion pura (también conocido como perfusión de la sangre) se pueden distinguir por medio de las secuencias de difusión IVIM,
utilizando varios valores b menores y mayores a 100 s/mm2,
a fin de evaluar la caída de la señal biexponencial de la intensidad de la señal en los órganos abdominales al tiempo que aumentan los valores de b.
La caída rápida (Fig.
9) de la primera se debe a los efectos de difusión y perfusión (valores b inferiores a 100 s/mm2) y la difusión real de las moléculas de agua demuestra una caida más lenta. El cálculo y la cuantificación de D* (la contribución de la perfusión a la caída de la señal),
D (la verdadera difusión de moléculas de H20) y f (la contribución de la perfusión a la señal de difusión) son posibles con este enfoque,
y son un indicador más fiable de la difusión de los tejidos que el anteriormente utilizado mapa de ADC.
Recientemente,
Luciani et al.
ha demostrado en pacientes cirróticos, restricción de la difusión disminución de la perfusión y alteración en el la difusion del agua.
IVIM también puede ser utilizada para evaluar la difusión y la perfusión de lesiones focales hepáticas.
( Fig.
10).
Mostramos un ejemplo de la caída de la señal según modelo IVIM de un schwannoma benigno.
(Fig.
11).
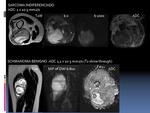
D) APLICACIONES CLÍNICAS DE LA SECUENCIA DE LA DIFUSIÓN
Al igual que en otras regiones del cuerpo, como una regla general,
los tumores malignos muestran mayor restricción del movimiento del agua libre (valores de ADC más bajos) que los benignos.
( Fig.
12)
Por otra parte,
los tumores malignos muestran un incremento en la fracción de perfusión ( modelo IVIM) que los tumores benignos.
Sin embargo, existe una superposición significativa en los valores de ADC de tumores benignos como malignos , ya que el ADC está influenciado no sólo por la celularidad,
sino también por otros factores como la matriz extracelular.
Los tumores mixoides,
independientemente de si son benignos o malignos, muestran los valores de ADC más altos de todos los tumores sólidos de partes blandas.
De una forma similar,
los tumores cartilaginosos o condroides tanto benignos como malignos,
muestran típicamente una ausencia de restricción de la difusión debido a su matriz extracelular condroide. Existen estudios que describen el condrosarcoma mesenquimal como el único tumor cartilaginoso con difusión restringida.
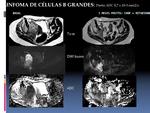
Los tumores de celulas redondas son un grupo agresivo de tumores con un origen embrionario incluyendo: el linfoma no Hodgkin,
sarcoma de Ewing,
el neuroblastoma y rabdomiosarcoma. Estos tumores debido a la alta celularidad y la relación de nucleo/citoplasma muestra una señal elevada en difusión con alto valor de b y valores de ADC característicamente bajos.
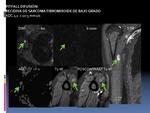
Dentro de los tumores fibrosos o fibrohistiocíticos de partes blandas,
la difusión puede ayudar en la diferenciación benigno/maligno y graduación histológica ( tumores malignos,
valores mas bajos de ADC).
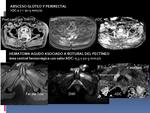
En el diagnóstico diferencial de las lesiones necróticas,
la difusión es una herramienta útil para la distinción entre tumores malignos necróticos y lesiones benignas. Los tumores malignos mostrarán un incremento en la difusión en el área necrótica y difusión restringida en la pared periférica. Por el contrario,
los hematomas o los abscesos presentarán restricción de la difusión en su núcleo central.
( Fig.
13)
Los tumores de células gigantes de la vaina tendinosa y los tumores difusos de células gigantes muestran un reducido espacio extracelular y difusión restringida.
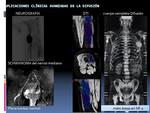
Otras aplicaciones clínicas de la difusión es la realización de secuencias de difusión whole body (cuerpo completo) para la detección de metástasis asi como RM-neurografía para la detección de síndromes compresivos neurales.
( Fig.
14).
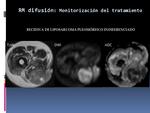
E) MONITORIZACIÓN DEL TRATAMIENTO
La difusión puede ayudar en los estudios de monitorización postratamiento, en la distinción entre tejido tumoral necrótico y viable,
y también en la diferenciación entre cambios post-tratamiento y recidiva tumoral.
(Fig.
15) Los cambios posttratamiento dan lugar a lesiones inflamatorias,
como los higromas y cambios edematosos e inflamatorios después de la radioterapia,
y la osteomielitis,
muestran una fuerte caída de la señal en difusión.
Al aumentar el factor b,
los cambios postto perderán señal de forma más manifiesta que las lesiones tumorales.
La difusión aumenta poco despues de la quimioterapia en pacientes con respuesta favorable con sarcomas de partes blandas,
y la disminución del ADC se correlaciona con la falta de respuesta y con el aumento de tamaño del tumor (Fig.
16-17).
2.
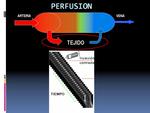
ESTUDIOS DINÁMICOS: PERFUSIÓN
Esta técnica permite estudiar las caracteristicas de la microcirculación en un tejido normal y de los tumores mediante secuencias dinámicas eco de gradiente T1 durante la inyección del contraste ( DCE-MRI)
Es necesaria una alta resollución temporal,
siendo un tiempo óptimo para cada dinámico entre 3-6 segundos. (Fig 18 y 19).
A) ANALISIS DE LA PERFUSION
MODELO MONOCOMPARTIMENTAL
En el análisis de los estudios de perfusión monocompartimental sólo se tiene en cuenta el paso de contraste desde la arteria a la vena
Este es un método semi-cuantitativo que permite realizar una rápida evaluación de la vascularización del tumor .
Las mediciones obtenidas directamente de la intensidad de señal pueden ser obtenidas y presentadas en mapas paramétricos,
tales como: máximo realce (relativo), tasa de realce precoz, área bajo la curva, tiempo de pico maximo o curva inicial de captación (Fig.
20 y 21).
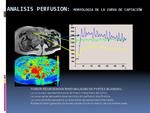
El análisis de la curva de captación tiempo / intensidad se basa en la observación visual de la curva tiempo-intensidad (TIC) generada a partir de la colocación de un ROI elegido en la lesión por el radiologo.
Aunque no cuantitativo,
este enfoque es menos sensible a las variaciones en el protocolo de resonancia magnética, por lo que es más adecuado para un meta-análisis comparativo.
El análisis TIC ha sido a menudo utilizado como sustituto en el análisis cuantitativo, habiéndose demostrado la morfología de la curva equivalente a los parámetros fisiológicos obtenidos a partir de los modelos compartimentales.
- El aumento de la angiogénesis del tumor a menudo se ha asociado con un patrón específico de la TIC, caracterizado por una captación precoz y lavado rápido del contraste,
que corresponde a un Ktrans elevado en estos modelos compartimentales .
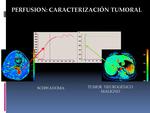
- La morfología de la curva indicará el grado de vascularización tumoral y consecuentemente ayuda a la caracterización tumoral (Fig.
22).
Como regla general,
los tumores malignos muestran un realce inicial rápido y posterior lavado.
Este patron se puede ver también en lesiones benignas.Sin embargo,
en los tumores de MSK existe una superposición de patrones de realce entre tumores benignos muy vascularizados y lesiones malignas hipovasculares.
Por contra,
otros estudios han demostrado diferencias claras en la permeabilidad entre tejidos benignos y malignos.
( fig.
23 y 24).
MODELO BICOMPARTIMENTAL
Varios modelos farmacocinéticos se han propuesto, como son los de Tofts,
Brix y Larsson independientemente,en una intención de obtener mediciones absolutas del proceso de la microcirculación, tal como la permeabilidad de los vasos.
Estos modelos consideran la fuga de contraste desde el espacio intersticial capilar y viceversa.
Aunque, teóricamente estas medidas absolutas,
como Ktrans, Kep,
Ve y VP, tienen un mejor ajuste en la comparación entre los estudios,
la falta de estandarización del modelo aplicado y el diseño de la secuencias han impedido su introducción en el ámbito clínico ( Fig.
25).
B) EVALUACIÓN POST-TRATAMIENTO
La perfusión puede ayudar a la monitorización terapéutica,
distinción entre tejido necrótico y viable,
diferenciación entre cambios post-ttto y recidiva.
(Fig.
26)
La radioterapia induce neovascularización y aumento de la perfusión del área irradiada.
Tamto los cambios posttratamiento como lesiones inflamatorias,
como abscesos,
mostrarán una perfusión aumentada,
pero en menor grado que en área de tumor viable residual/recidivado.
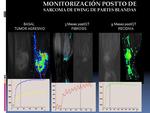
La perfusión disminuye tras la quimioterapia en el sarcoma de partes blandas y tumores de células redondas en pacientes con respuesta positiva al tratamiento (Fig.
27).
En la detección de recidiva tumoral,
DCE-MR demuestra áreas de neovascularización en el lecho quirúrgico o cicatriz.
Es importante la diferenciación entre tumor viable y necrosis,
ya que la presencia de mucha necrosis se vincula a radioresistencia.
La RM perfusión es un arma interesante en la monitorización terapeutica con fármacos antiangiogénicos de los TPB.
3.
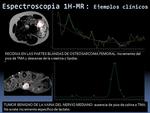
ESPECTROSCOPIA H1
Existe una experiencia muy limitada en la espectroscopia clínica de los tumores de tejidos blandos.
Metabolitos:
La colina (Cho): Se incrementa en los tumores malignos
La creatina (Cr)
Trimetilamina (TMA): Se incrementa en los tumores malignos
NAA (N-acetil-acetato)
Lac (lactato): indica metabolismo anaeróbico.
Se ha relacionado con tumores en otras anatomías, pero no esta clara su relación con los tumores malignos de partes blandas.
Relaciones metabólicas:
* Cho / Cr: aumento en los tumores malignos de partes blandas
* TMA / Cr: aumento en los tumores malignos de partes blandas.
*NAA / Cr: no es una relación útil para distinguir tumor de tejidos blandos
* Lip1/Cr: un descenso puede indicar malignidad
* Lip2/Cr: un descenso puede indicar malignidad
Marcadores metabólicos malignos:
* El pico muy aumentado de colina,
por lo general más alto que el pico de Cr.
* Descenso del pico de lípidos puede ser obviamente reducida.
* La mayoría de los tumores benignos no tienen pico de colina o TMA.
ASPECTOS TECNICOS Y EJEMPLOS EN LA ESPECTROSCOPIA.
(Fig.
28 y 29).