A pesar de que las enfermedades parasitarias son poco frecuentes en nuestra práctica diaria,
en Europa Occidental algunas de estas parasitosis están aumentando su incidencia debido principalmente a la inmigración desde regiones endémicas tropicales.
Además,
algunas de estas enfermedades son aún endémicas en ciertas regiones europeas.
Conocer los hallazgos característicos por imagen de estas enfermedades es importante no solamente para hacer un diagnóstico preciso,
sino también para realizar un manejo clínico adecuado.
Los parásitos son organismos que viven a expensas de otro organismo (hospedador),
originando en ocasiones en éste una enfermedad.
Estos huéspedes inesperados son muy heterogéneos,
a veces ocasionan enfermedades sistémicas y otras quedan confinados a órganos específicos.
Muchos tienen ciclos vitales complejos que pueden variar en función del hospedador al que parasiten sea éste el hospedador final o uno intermediario.
El diagnóstico de las enfermedades parasitarias requiere una alta sospecha clínica existiendo dos métodos principales de diagnóstico: identificar el parásito o detectar antígenos específicos del mismo.
Clasificación de algunos parásitos y sus formas de transmisión.
Tabla 1.
Hallazgos por imagen
Se revisaron todos los casos de enfermedades parasitarias que han sido detectados en nuestro centro desde el año 2002 al año 2012 y se seleccionaron aquellos a los que se les realizaron pruebas de imagen.
Revisamos las imágenes de nuestro archivo informático y seleccionamos los casos con imágenes representativas,
mostrando los principales hallazgos descritos en la literatura.
EQUINOCOCOSIS O HIDATIDOSIS:
La Equinococosis está ocasionada por diversas formas de tenias (E.
granulosus y E.multilocularis principalmente,
y también por E.
vogeli y E.
oligarthrus).
Los cánidos son los hospedadores definitivos de estos nematodos,
pero el ganado y los humanos pueden ser hospedadores intermediarios.
La Equinococosis humana se produce tras la ingesta de huevos de la tenia presentes en las heces de los perros.
Estos huevos se desarrollan hasta convertirse en larvas que se introducen en la circulación portal y terminan formando lesiones quísticas en diferentes tejidos.
Podemos encontrar estos quistes en cualquier órgano del cuerpo humano,
pero las localizaciones más frecuentes son el hígado y el pulmón.
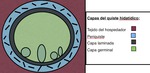
La estructura de los mismos es muy característica y está compuesta por diferentes capas.
Fig.
1
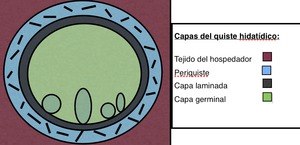
Fig. 1: La estructura de los quistes hidatídicos es muy característica, identificando diferentes capas.
Los quistes hidatídicos suelen calcificar cuando las larvas mueren,
aunque debemos tener presente que a veces los quistes hidatídicos calcificados pueden contener larvas vivas.
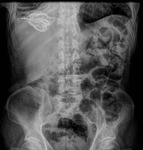
En muchas ocasiones estos quistes son detectados incidentalmente como lesiones calcificadas en las radiografías simples de abdomen.
Fig.2
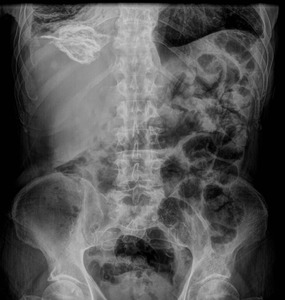
Fig. 2: Radiografía anteroposterior de abdomen identificando incidentalmente un quiste hidatídico hepático calcificado en un paciente de 75 años.
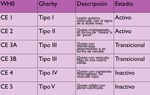
Hay dos clasificaciones internacionales de los quistes hidatídicos basadas en patrones ultrasonográficos que se correlacionan con la evolución y la viabilidad de los quistes.
Tabla 2.
- Clasificación de Gharby de 1981
- Clasificación de la WHO (“Informal Working Group on Echinococcosis”) de 2003
Aparte del estudio ecográfico,
la tomografía computarizada (TC) también es una herramienta útil para el diagnóstico y clasificación de esta enfermedad.
La resonancia magnética (RM),
también puede demostrar de forma precisa los patrones morfológicos del quiste.
Ejemplos de quistes hidatídicos por ecografía,
TC y RM: Fig.3,4,5,6,7,8,9 y 10.
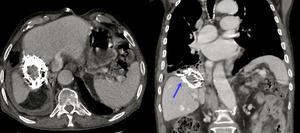
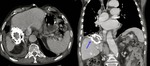
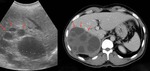
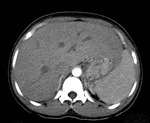
Fig. 3: Imágenes de tomografía computarizada en los planos axial y coronal mostrando un quiste hidatídico hepático calcificado con migración transdiafragmática del quiste hacia el tórax. Se trata de una rara complicación en pacientes con hidatidosis hepática.

Fig. 3: Imágenes de tomografía computarizada en los planos axial y coronal mostrando un quiste hidatídico hepático calcificado con migración transdiafragmática del quiste hacia el tórax. Se trata de una rara complicación en pacientes con hidatidosis hepática.
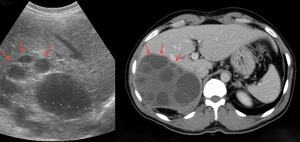
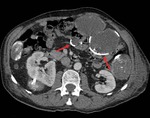
Fig. 4: Ecografía en el plano axial oblicuo y tomografía computarizada en el plano axial con contraste intravenoso mostrando un quiste hidatídico multivesicular. Nótese la localización periférica de las vesículas hijas en el quiste principal (flechas rojas).
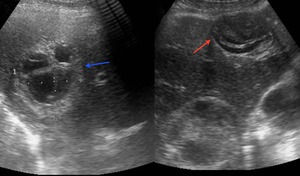
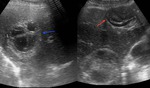
Fig. 5: Imágenes de ecografía mostrando dos quistes hidatídicos. Nótese que uno contiene membranas desprendidas con apariencia serpigiforme (flecha roja). El otro (flecha azul) muestra una apariencia distinta, con vesículas hijas que ocupan casi la totalidad del quiste hidatídico "madre" o principal (signo de la roseta).
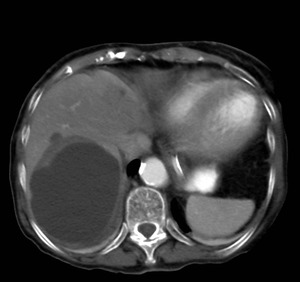
Fig. 6: TC con contraste intravenoso en el plano axial mostrando un quiste hidatídico unilocular.
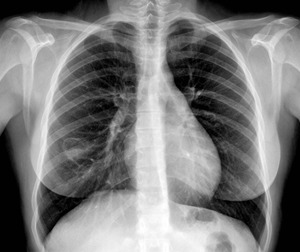
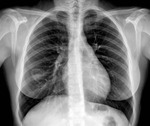
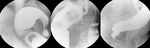
Fig. 7: Radiografía de tórax posteroanterior mostrando una lesión cavitada en el lóbulo inferior derecho con contenido denso en su porción más declive en relación con quiste hidatídico.
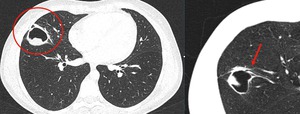
Fig. 8: TC de tórax de alta resolución mostrando el quiste hidatídico con contenido sólido en su interior descrito en la fig.7. En la reconstrucción multiplanar axial se confirma comunicación de la cavidad con la vía aérea (flecha roja).
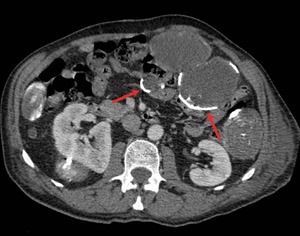
Fig. 9: Múltiples quistes hidatídicos peritoneales secundarios a siembra debida a ruptura de un quiste hidatídico hepático. Nótese las calcificaciones periféricas de los quistes (flechas rojas).
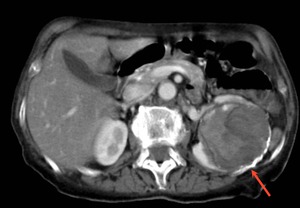
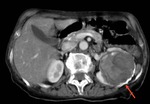
Fig. 10: Quiste hidatídico renal izquierdo con contenido heterogéneo en una TC con contraste intravenoso. Nótese la calcificación periférica del quiste (flecha roja).
ESTRONGIOLOIDIASIS:
La estrongiloidiasis es una enfermedad prevalente en todo el mundo originada por S.
stercolaris. La larva filariforme de este parásito penetra en la piel humana para comenzar aquí su ciclo parasitario.
Es importante destacar que este nematodo suele producir enfermedad a pacientes inmunodeprimidos.
Otro aspecto característico de este parásito es que es capaz de llevar a cabo un ciclo vital completo en el cuerpo humano condicionando una infección grave denominada autoinfección o hiperinfestación que finalmente puede producir un síndrome de hiperinfestación fatal.
Fig.11
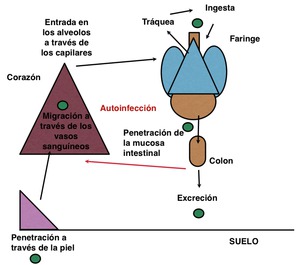
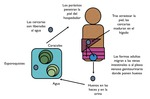
Fig. 11: Ciclo vital del S. stercolaris en el cuerpo humano.
El síndrome de hiperinfestación consiste en una infección parasitaria masiva que lleva a un síndrome de respuesta inflamatoria sistémica generalmente en pacientes inmunocomprometidos.
Los hallazgos radiológicos de este síndrome consisten en opacidades pulmonares extensas debidas al parásito en sí mismo o bien a la respuesta del huésped al parásito (edema no cardiogénico,
hemorragia o ambos).
En el tracto gastrointestinal podemos encontrar signos inespecfíficos como engrosamiento de la pared intestinal.
Fig.12 y Fig.13
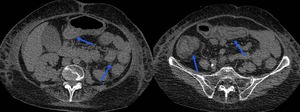
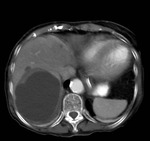
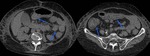
Fig. 12: TC sin contraste intravenoso en el plano axial de un paciente inmunocomprometido de 45 años con un síndrome de hiperinfestación severo. Podemos apreciar el engrosamiento difuso de la pared intestinal y discreta dilatación de asas (flechas azules).
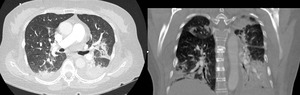
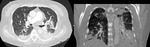
Fig. 13: TC torácico en el plano axial con reconstrucción en el plano coronal realizado a un paciente inmunodeprimido de 45 años con un síndrome de hiperinfestación severo. El estudio muestra opacidades bilaterales de predominio en ambas bases.
CISTICERCOSIS:
La cisticercosis está originada por la larva de la tenia porcina Taenia solium la cual es responsable de una infección prevalente en todo el mundo.
La infección se produce al ingerir carne cruda o poco cocinada de un animal infectado por el parásito.
Esta enfermedad se ha clasificado en tres estadios diferentes dependiendo del estado de desarrollo del mismo y de la respuesta del hospedador al parásito.
Tabla 3.
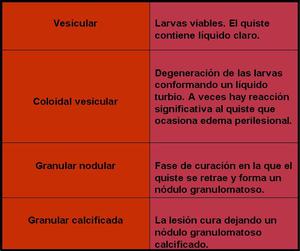
Table 1: Estadios de desarrollo de la neurocisticercosis.
La neurocisticercosis es la enfermedad parasitaria más frecuente del sistema nervioso central y la causa de epilepsia adquirida más habitual,
constituyendo así un problema de salud muy importante a nivel mundial.
El diagnóstico de la neurocisticercosis se basa en la combinación de hallazgos clínicos y de imagen (TC y RM) por lo que los radiólogos juegan un papel relevante en la detección y monitorización de esta enfermedad.
La mejor técnica para el estudio de la neurocisticercosis es la RM,
siendo el test diagnóstico más sensible para detectar todos los estadios parasitarios,
a excepción del último,
la fase nodular calcificada,
donde la TC sin contraste presenta mayor sensibilidad.
Fig.14,
15,
16 y 17.
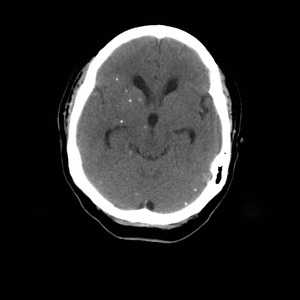
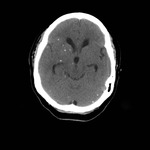
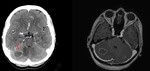
Fig. 14: TC craneal sin contraste intravenoso mostrando múltiples nódulos puntiformes calcificados cerebrales en relación con neurocisticercosis en fase granular calcificada.
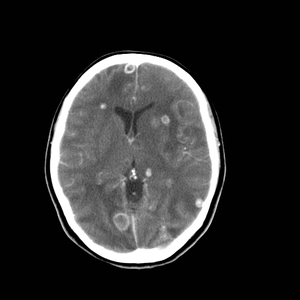
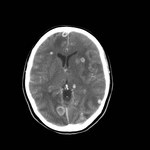
Fig. 15: TC craneal con contraste intravenoso mostrando múltiples lesiones con realce en anillo y edema en un paciente con neurocisticercosis en fase coloidal vesicular.
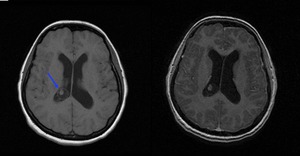
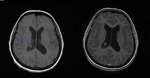
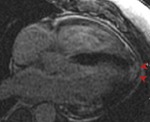
Fig. 16: Neurocisticercosis vesicular subarcnoidea. Imágenes de RM, secuencia potenciada en T1 y T1 con gadolinio intravenoso mostrando una lesión quística en el trígono ventricular conteniendo un escólex excéntrico (flecha azul) hiperintenso con respecto al líquido cefalorraquídeo sin edema y sin realce en anillo.
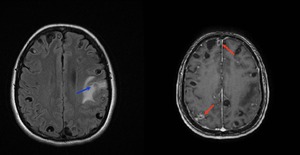
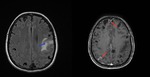
Fig. 17: Secuencias de RM potenciadas en FLAIR y T1 con gadolinio intravenoso mostrando múltiples lesiones corticales y subcorticales algunas con realce anular (flechas rojas) y otras con edema perilesional (flechas azules) en un paciente con neurocisticercosis en fase coloidal vesicular.
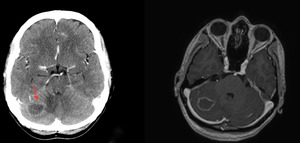
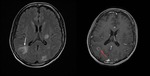
Fig. 18: Toxoplasmosis intracraneal en un paciente de 45 años con SIDA. TC con contraste intravenoso y RM potenciada en T1 con gadolinio intravenoso mostrando una lesión con realce en anillo (flecha roja), discreto efecto de masa y edema perilesional en el hemisferio cerebeloso derecho.
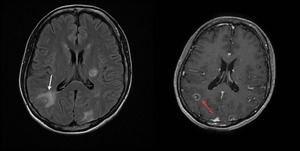
Fig. 19: Imágenes de RM (secuencias FLAIR y T1 con gadolinio intravenoso) mostrando múltiples lesiones con edema perilesional (flecha blanca) y realce en anillo (flecha roja).
TOXOPLASMOSIS:
La toxoplasmosis es una infección originada por un protozoo prevalente mundialmente,
el T.
gondii.
Es más frecuente en los trópicos y en áreas donde los felinos son numerosos.
El ciclo vital del T.
gondii tiene dos fases diferenciadas.
La denominada fase sexual tiene lugar en el felino,
que es el hospedador principal del parásito.
La siguiente fase,
la asexual,
puede ocurrir en otros animales de sangre caliente,
incluyendo los humanos.
La infección en humanos puede ocurrir de dos formas diferentes,
ingiriendo heces infectadas de gatos o a través de la transmisión sanguínea materna del parásito al feto.
La infección primaria es asintomática en el 90% de los pacientes aunque en algunos casos puede dar lugar a un síndrome pseudogripal.
Después de la infección por T.
gondii puede quedar latente en el organismo.
La infección fetal a veces ocasiona toxoplasomosis congénita y en individuos imunocomprometidos este parásito puede dar lugar a formas más agresivas de esta enfermedad,
especialmente en el sistema nervioso central.
Los estudios radiológicos son útiles en el diagnóstico tanto de las formas congénitas como en la enfermedad del adulto.
Este parásito afecta al sistema nervioso central en aproximadamente el 10% de los pacientes con SIDA,
localizándose las lesiones en los ganglios basales,
unión corticomedular o en la sustancia blanca periventricular.
En la infección congénita podemos encontrar calcificaciones,
hidrocefalia o microcefalia.
Sin embargo,
las calcificaciones son raras en la forma adulta,
donde normalmente encontramos lesiones rodeadas de edema con efecto de masa y que suelen realzar tras la administración de contraste intravenoso.
Fig.18 y 19.

Fig. 18: Toxoplasmosis intracraneal en un paciente de 45 años con SIDA. TC con contraste intravenoso y RM potenciada en T1 con gadolinio intravenoso mostrando una lesión con realce en anillo (flecha roja), discreto efecto de masa y edema perilesional en el hemisferio cerebeloso derecho.

Fig. 19: Imágenes de RM (secuencias FLAIR y T1 con gadolinio intravenoso) mostrando múltiples lesiones con edema perilesional (flecha blanca) y realce en anillo (flecha roja).
ESQUISTOSOMIASIS:
La esquistosomiasis es un grupo de enfermedades parasitarias endémicas en África,
en Oriente Medio y en algunas regiones de América del sur.
Está ocasionada por varios trematodos del género Schistosoma,
siendo el único trematodo que invade el ser humano a través de la piel (los otros solo infectan a través de la ingesta).
El hospedador intermediario de estos parásitos son los caracoles y otros moluscos de agua dulce,
siendo el hombre el hospedador definitivo.
Fig.20
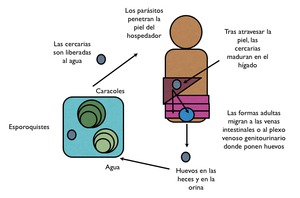
Fig. 20: Ciclo vital de la especie Schistosoma.
Hay dos formas principales de esquistosomiasis: la intestinal y la genitourinaria,
siendo la última la más frecuente.
La esquistosomiasis genitourinaria está causada por S.
haematobium,
una de las cinco especies de trematodos que pueden infectar y originar esquistosomiasis en humanos,
afectando principalmente al uréter y la vejiga. Fig.21 y 22.
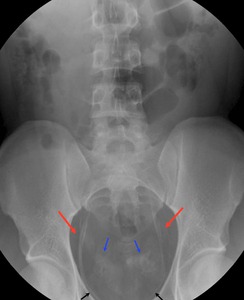
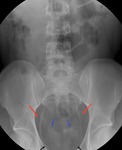
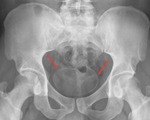
Fig. 21: Radiografía de abdomen anteroposterior mostrando calcificación de la porción pelviana de ambos uréteres (flechas rojas), calcificación de los conductos deferentes (flechas azules) y de la pared de la vejiga. (flecha negra). Caso cortesía del Dr. Barrera/ES.
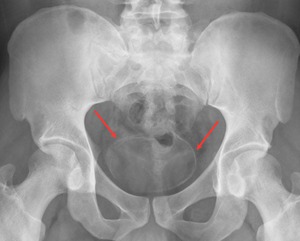
Fig. 22: Radiografía anteroposterior de pelvis mostrando calcificación completa de la pared vesical en una forma crónica de esquistosomiasis.
Los riñones no suelen afectarse hasta estadios avanzados de la enfermedad.
En estadios tempranos,
el parásito infecta la vía urinaria condicionando edema y hemorragia en la mucosa.
Más tarde,
el tejido se fibrosa y aparecen granulomas calcificados (huevos muertos calcificados).
Hay un signo patognomónico clásico de esquistososmiasis genitourinaria: la pared de la vejiga calcifica de forma completa y semeja la cabeza de un feto en la pelvis.
Fig.
22.
AMEBIASIS:
La amebiasis es una enfermedad extendida ampliamente por todo el mundo estimándose que el 10% de la población mundial está infectada por Entamoeba histolytica.
Es más prevalente en la India,
en los países del Este de Europa,
África y en América Central y del Sur.
E.
histolytica infecta el tracto gastrointestinal permaneciendo en ocasiones en un estadio latente durante muchos años,
pero en ocasiones origina formas más agresivas de la enfermedad que pueden variar desde una colitis hasta una disentería amebiana con desarrollo de abscesos hepáticos.
Los abscesos hepáticos amebianos son la complicación extraintestinal más frecuente de esta enfermedad.
Éstos tienen a veces características indistinguibles de los abscesos piógenos,
sin embargo,
los datos clínicos y epidemiológicos,
así como títulos positivos para amebas pueden ayudar a realizar el diagnóstico.
La ecografía,
la TC y la RM son útiles para detectar lesiones hepáticas.
Fig.23.
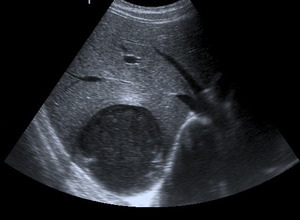
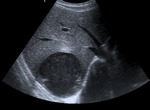
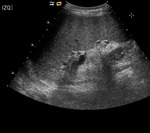
Fig. 23: Ecografía en el plano axial mostrando una lesión redondeada quística con contenido ecogénico localizada en el lóbulo derecho en relación con absceso amebiano hepático.
Estos abscesos tienden a localizarse en áreas periféricas próximas a la cápsula de Gleason,
pueden asociar edema perilesional y suelen presentar una pared gruesa que realza tras la administración de contraste intravenoso.
Fig 24.
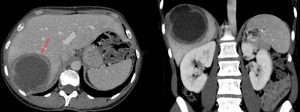
Fig. 24: TC abdominal con contraste intravenoso en el plano axial y coronal mostrando una gran masa quística en el lóbulo hepático derecho en relación con quiste amebiano. Nótese el marcado grosor y realce de la pared del absceso (flecha roja).
DRACUNCULIASIS:
La dracunculiasis está originada por el Gusano de Guinea,
(Dracunculus medinensis).
Esta enfermedad está limitada a zonas remotas de pueblos rurales en el África subsahariana.
Por fortuna,
los programas de erradicación han reducido de manera muy notable esta enfermedad en las últimas dos décadas.
La infección humana ocurre tras la ingesta de agua contaminada conteniendo larvas de estos parásitos,
que eventualmente migran a los tejidos subcutáneos.
La infección de este parásito generalmente afecta a las articulaciones de los miembros inferiores,
especialmente a la rodilla.
Es muy característico encontramos incidentalmente este parásito como calcificaciones de tejidos blandos con forma de gusano.
Fig.
25.
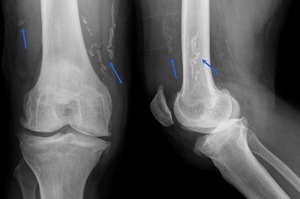
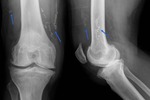
Fig. 25: Radiografía posteroanterior y lateral de la rodilla mostrando múltiples gusanos de Guinea calcificados en partes blandas en un paciente subsahariano de 45 años.
TRYPANOSOMIASIS:
El Tripanosoma cruzi es el agente etiológico de la enfermedad de Chagas.
Este parásito se adquiere a través de un vector del parásito,
un insecto de la familia Reduviidae (principalmente la T.
infestans popularmente conocida como vinchuca),
que defeca las heces en la piel y pica al individuo. Posteriormente la herida de la picadura favorece la inoculación del parásito que consigue introducirse en el torrente sanguíneo.
La enfermedad de Chagas está ampliamente extendida en América Central y del Sur.
Alrededor de un 15-30% de los individuos infectados desarrollan formas crónicas de la enfermedad,
generalmente afectando al corazón,
al tracto digestivo y al sistema nervioso central.
La enfermedad de Chagas tiene diferentes estadios.
En las fases tempranas de la enfermedad,
el paciente puede presentar síntomas cardiológicos o neurológicos (miocarditis o meningoencefalitis).
Más tarde,
en la fase subaguda,
la hepatoesplenomegalia y las linfadenopatías son los hallazgos más frecuentes.
El megaesófago (acalasia chagasiforme) o el megacolon pueden observarse en la fase crónica de la enfermedad.
Fig.
26.
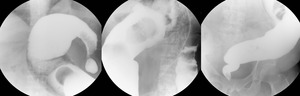
Fig. 26: Enema de bario en un paciente boliviano de 42 años mostrando megacolon, fundamentalmente a expensas del colon sigmoide. Se confirmó enfermedad de Chagas serológicamente.
La enfermedad de Chagas crónica puede afectar también al corazón,
ocasionando necrosis miocárdica y fibrosis tanto por la persistencia del parásito como por la afectación autoinmunitaria al mismo.
La fibrosis miocárdica o la necrosis son visualizadas en RM de forma característica como áreas de realce tardío tras la administración de contraste intravenoso. 27 y 28.
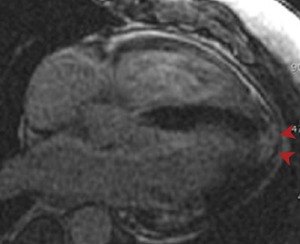
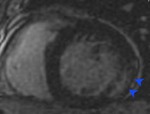
Fig. 27: Enfermedad de Chagas cardíaca crónica. Paciente diagnosticado de infección por T. cruzi. Plano de cuatro cámaras en secuencia de RM de realce tardío donde podemos apreciar realce transmural tardío en el ápex cardíaco indicando fibrosis o necrosis miocárdica (puntas de flecha azules). Caso cortesía de la Dra.Cabeza y de la Dra.Bustos/ES
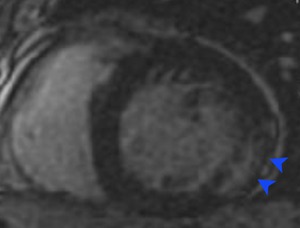
Fig. 28: Enfermedad de Chagas cardíaca crónica. Varón diagnosticado de infección por T. cruzi. Imagen de dos cámaras en eje corto en secuencia de RM de realce tardío mostrando realce transmural en un territorio no coronario (segmento basal infero-lateral), indicando fibrosis y necrosis miocárdica (puntas de flecha rojas). Caso cortesía de la Dra.Cabeza y la Dra.Bustos/ES
LEISHMANIASIS:
La leishmaniasis es una enfermedad causada por un protozoo que origina un espectro amplio de sintomatología y hallazgos clínicos,
desde ulceraciones cutáneas hasta una grave enfermedad sistémica,
y es transmitida por la picadura de ciertas especies de mosquitos del género Phlebotomus.
Estos parásitos se han identificado en todo el mundo,
sin embargo,
algunas especies de Leishmania existen en regiones endémicas.
Este es el caso de la L.
infantum,
una especie particular que afecta al sistema reticulo-endotelial de diferentes órganos incluyendo el hígado y el bazo,
y que puede encontrarse con más frecuencia en el Mediterráneo y en Oriente Próximo.
Los hallazgos por imagen de la Leishmaniasis son inespecíficos,
generalmente identificando hepatoesplenomegalia y aumento del tamaño de los ganglios linfáticos.
Fig.29 y 30.
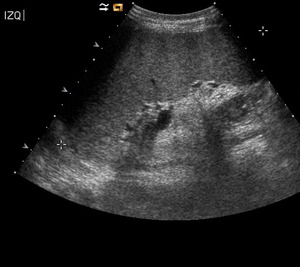
Fig. 29: Ecografía mostrando esplenomegalia en un paciente de 52 años con fiebre, pérdida de peso y pancitopenia. Los exámenes serológicos confirmaron leishmaniasis visceral.
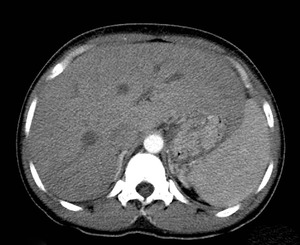
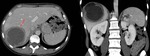
Fig. 30: TC abdominal con contraste intravenoso mostrando hepatoesplenomegalia en un paciente con leishmaniasis visceral.