El término carcinomatosis peritoneal (CP) incluye toda diseminación tumoral que afecta,
de forma localizada o masiva,
la serosa peritoneal y las estructuras anatómicas vecinas.
El tamaño y la extensión de la enfermedad peritoneal no influyen en la definición del término CP.

Fig. 1: Incidencia de carcinomatosis al diagnóstico
Tradicionalmente,
la CP era considerada como fase terminal de la enfermedad neoplásica.
A finales de la década de 1980,
se produce un cambio de paradigma al considerar la CP como una enfermedad locoregional y por lo tanto potencialmente curable.
Sugarbaker estableció las bases de un tratamiento multidisciplinar en la CP que asocia la cirugía radical y la administración inmediata de quimioterápicos intraperitoneales,
con o sin hipertermia,
orientados a erradicar el tumor microscópico residual a la cirugía.
Tratamiento multidisciplinar de CP
1.-Cirugia radical
- Los procedimientos de peritonectomía constan de seis pasos quirúrgicos que deben realizarse secuencialmente en relación con la distribución y la extensión de la CP.
Cada procedimiento se define según las regiones y los órganos afectados:
- 1) omentectomía mayor,
peritonectomía parietal derecha +/- exéresis del colon derecho;
- 2) peritonectomía pélvica +/‒exéresis rectosigmoidea +/- histerectomía total,
salpingo-ooforectomía bilateral y anastomosis colorrectal baja;
- 3) omentectomía menor con exéresis del ligamento hepatoduodenal +/- gastrectomía +/- colecistectomía;
- 4) peritonectomía del cuadrante superior derecho +/- exéresis de la cápsula de Glisson;
- 5) peritonectomía del cuadrante superior izquierdo +/- esplenectomía,
y
- 6) otras resecciones intestinales y exéresis de masas abdominopélvicas
La extirpación de los implantes con distribución difusa y extensa en la superficie peritoneal obliga a la extirpacion de todo el peritoneo. Los implantes aislados y escasos del peritoneo parietal o visceral que no infiltran en profundidad son extirpados o electrovaporados.
Los implantes voluminosos,
el tumor confluente o el implante que invade en profundidad a un órgano o estructura anatómica obliga a la exéresis asociada de estas.
En las CP extensas o limitadas pero de gran volúmen puede ser necesario realizar exéresis multiviscerales y/o amplias resecciones intestinales.
La afectación tumoral de una parte importante del intestino delgado puede limitar o impedir la realización de la cirugía radical
2.-Quimioterapia intraperitoneal
- La quimioterapia administrada por vía intraperitoneal,
permite realizar un tratamiento muy intensivo de los tumores localizados en la cavidad abdominal en relación a la dosis de fármacos utilizada.
- Los quimioterápicos utilizados por vía intraperitoneal varían según el tumor primario que origina la CP.
Las moléculas más utilizadas son el 5-FU,
la mitomicina C,
la doxorubicina,
el cisplatino,
el paclitaxel,
la gemcitabina,
el etopósido,
la bleomicina,
el metotrexato,
el melfalán,
el interferón,
el oxaliplatino y el irinotecán.
Los fármacos que actúan a nivel intraperitoneal pueden ser administrados de forma aislada o en combinación.
3.-Hipertermia
- La asociación del calor a la quimioterapia intraperitoneal potencia el efecto terapéutico regional de algunos quimioterápicos y provoca un «shock tóxico» directo sobre las células tumorales.
- Esta aplicación combinada de tratamiento regional recibe el nombre de quimiohipertermia peritoneal (HIPEC,
del inglés hyperthermic intraperitoneal chemotherapy).

Fig. 25: HIPEC. Técnica cerrada

Fig. 2

Fig. 3

Fig. 4
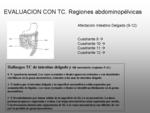
EVALUACION CON TC.
Regiones abdominopélvicas
Las regiones abdominopelvicas vienen definidas por dos planos sagitales a través de la línea media clavicular y dos planos transversos,
uno a través de las espinas iliacas anterosuperiores y otra a través del punto mas caudal del margen costal.

Fig. 5

Fig. 6
Desde enero de 2013 se han incluido 10 pacientes en protocolo de CP.
Se les ha realizado una TC helicoidal de 64 canales con administracion de contrastr IV en fase arterial y venosa.
La presencia o ausencia de afectación peritoneal se evalúa en 13 regiones anatómicas.
El tamaño tumoral varia de 0 a 3.
Los hallazgos de TC de intestino delgado y su mesenterio corresponden a las regiones 9 a 12.
Se revisa el ICP quirurgico y lo comparamos con los hallazgos visualizados en TC en el momento del diagnostico y de forma retrospectiva.
Caso 1: Paciente de 56 años de edad,
diagnosticado en agosto del 2012 de
neoplasia gástrica avanzada con posible carcinomatosis peritoneal que habiendo finalizado 3 ciclos de quimioterapia neoadyuvante y tras ser presentado en comité de tumores se decide Intervención quirúrgica electiva.
El paciente se encuentra asintomático en el momento actual.

Fig. 7
Caso 2: Varón de 51 años.
En diciembre de 2011 hemicolectomia derecha y resección de implante en meso por adenocarcinoma de colon perforado a retroperitoneo (pT3 N2a M1) con metástasis hepática en segmento VII.
En enero de 2012 reintervenido por fístula enterocutánea realizándose resección de anastomosis previa y asas de intestino delgado fija a flanco derecho con anastomosis ileocolica y metastasectomia hepática de tumoración en segmento VII y II con colecistectomia.
Tratado con quimioterapia adyuvante hasta septiembre del mismo año.
Presenta recidiva a nivel peritoneal y hepática.
Una vez completado el estudio y presentando en el comité de tumores digestivos se decide quimioterapia
neoadyuvante y posteriormente programar para citoreducción más HIPEc más radiofrecuencia de LOE hepática.

Fig. 8

Fig. 9

Fig. 10
Caso 3: Paciente de 48 años con antecedente de gastrectomía por ulcus gástrico hace 15 años.
Diagnosticado de neoplasia de muñón gástrico con carcinomatosis peritoneal en junio de 2012,
que tras finalizar quimioterapia neoadyuvante y ser presentado en el Comité de Tumores Digestivo,
se decide ingreso en cirugía para evaluar citoreducción e Hipec.

Fig. 11

Fig. 12

Fig. 13
Caso 4: Paciente de 48 años de edad intervenido por neoplasia de colon en abril del 2011 (T3N0M0).
En seguimiento en Consultas de Cirugía y Oncología.
Tras diagnosticarse carcinomatosis peritoneal en noviembre de 2012 y tras finalizar quimioterapia sistémica,
es revaluada por en Comité de Tumores Digestivos indicando laparotomía para citorreducción e HIPEC.
La paciente se encuentra asintomática en el momento actual.

Fig. 14

Fig. 15
Caso 5:Paciente que debuta con TEP.
En laparoscopia: implantes peritoneales de5 mm.
,
por toda la cavidad abdominal,
intestino delgado e intestino grueso.
Epiplón completamente infiltrado.
Carcinoma seroso de alto grado compatible con origen ovárico.
Quimioterapia neoadyuvante.
Se realiza laparotomía mas HIPEC.

Fig. 16

Fig. 17
Caso 6: Paciente de 47 años,
con el diagnóstico de Neo de ovario,
masa pélvica y carcinomatosis,
ingresa para tto.
quirúrgico post quimioterapia (Carboplatino,
Taxol y Abastin x 7 ciclos) + HIPEC.

Fig. 18

Fig. 19
Caso 7: Paciente de 66 años,
Hemicolectomía derecha por cáncer de colon T3N0M0 en Octubre de 2011.
Recidiva locoregional y peritoneal.

Fig. 20

Fig. 21
Caso 8: Paciente de 60 años con diagnóstico de recidiva de Ca de ovario que ingresa programada para tratamiento quirúrgico.

Fig. 22

Fig. 23
Caso 9: Paciente de 59 años,
con diagnósotico de Ca de ovario estadío IIIC (adenocarcinoma papilar seroso de ovario).
Qimio neoadyuvante.

Fig. 24