Las infecciones constituyen una de las complicaciones más importantes del transplante de progenitores hematopoyéticos (TPH),
incluso habiendo disminuido su morbimortalidad en los últimos años gracias a:
- Conocimiento de los factores de riesgo.
- La recuperación inmunitaria postTPH.
- Patrón de infección según la fase evolutiva del TPH.
- Desarrollo de antimicrobianos más efectivos.
Tras el TPH el paciente se encuentra en un estado de inmunodeficiencia celular y humoral que favorece que aparezcan complicaciones infecciosas en el paciente.
El tiempo que necesita el sistema inmunológico para recuperarse tras el TPH es muy variable y depende de:
- Tipo de transplante.
- Fuente de los progenitores
- Régimen de acondicionamiento
- Grado de histocompatibilidad donante-receptor.
- Presencia de la enferemdad injerto contra huésped (EICH).
Existen otros factores que aumentan el riesgo de infecciones:
- Grado y tiempo de la neutropenia.
- Alteración de barreras anatómicas
- Existencia de infecciones latentes
Las complicaciones pulmonares en los pacientes postransplante de TPH tienen lugar en el 40-60% y son causa de elevada morbimortalidad.
La TAC es excelente para la detección de alteraciones en el parénquima pulmonar,
pero estos hallazgos son generalmente poco específicos,
por lo que si estos hallazgos los asociamos al estado inmunológico del paciente y al periodo postTPH,
podremos acotar mejor las opciones diagnósticas.
Se distinguen tres fases evolutivas que comienzan a partir del día de la infusión de los progenitores (día 0),
en cada una de las cuales van a predominar determinadas infecciones.
PERIODO DE NEUTROPENIA (días 0 a +30)
En la fase inmediatamente después del TPH,
tiene lugar una profunda neutropenia que dura entorno a 2-3 semanas.
Los patógenos a los que nos enfrentaremos con más frecuencia en este periodo son:
- Hongos:
* Aspergillus: es el principal patógeno en este periodo.
* Candida albicans
- Bacterias gramnegativas y/o grampositivas.
*Pseudomona aeruginosa,
Escherichia coli,
Streptococcus pneumoniae,
Staphylococcus aureus y Haemophilus influenzae
- Virus
* Virus del herpes simple (VHS): En pacientes seropositivos para el VHS,
el empleo profilactico de aciclovir ha reducido notablemente las infecciones por este agente.
* Virus Respiratorio Sincitial (VRS).
Otras patologías no infecciosas que nos podemos encontrar son la hemorragia alveolar difusa,
edema pulmonar y la toxicidad por fármacos.
ASPERGILLUS
Las infecciones por hongos son muy frecuentes en este periodo,
de diagnóstico difícil y de morbimortalidad elevada.
El patógeno más frecuente es Aspergillus,
cuyas esporas están en el ambiente y son inhaladas (al adquirirse por inhalación,
el tratamiento del aire que rodea al paciente tiene una especial relevancia en la prevención de esta complicación.)
En TAC,
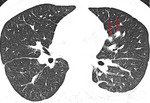
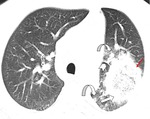
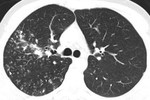
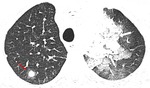
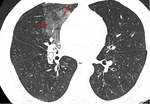
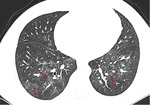
la aspergilosis angioinvasiva aparece como nódulos rodeados de un halo en vídrio deslustrado (figura 1) (figura 2).
Corresponde a un área central consolidada que representa la infección fúngica extendiéndose por el parénquima pulmonar rodeados de áreas de infarto hemorrágico causadas por la trombosis a medida que el hongo invade los vasos adyacentes.
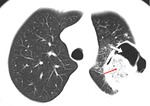
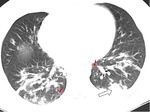
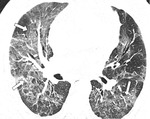
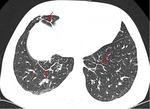
La cavitación del nódulo,
que representa el signo de la media luna,
tiene lugar durante el proceso de recuperación de la infección cuando se está resolviendo la neutropenia (figura 3) (figura 4).
También se pueden ver consolidaciones semgnetarias (figura 3) (figura 5).
Aproximadamente en un 30% de los casos de aspergilosis,
el hongo invade la vía aérea,
apreciándose en el TAC signos de patología peribronquial o peribronquiolar con nódulos centrolobulillares de 5 mm hasta áreas de consolidación mayores de 5 cm (figura 6).
CANDIDA ALBICANS
La candidiasis pulmonar puede ocurrir por vía hematógena o endobronquial:
- Cuando tiene lugar vía endobronquial,
dicha candidiasis suele estar limitada al parénquima pulmonar y se suele presentar como nódulos o áreas de consolidación alveolar de predominio en lóbulos inferiores.
- Por vía hematógena da lugar a múltiples nódulos de distribución bilateral,
asociados frecuentemente a infección en otras localizaciones extrapulmonares.
Los nódulos o áreas de consolidación pueden estar acompañadas de áreas en vidrio deslustrado.
Por lo tanto,
se suelen ver nódulos hemorrágicos de 2-4mm de diámetro con o sin centro necrótico que contiene los microorganismos,
acompañados o no de áreas en vidrio deslustrado alrededor.
VIRUS RESPIRATORIO SINCITIAL
Los hallazgos predominantes son nódulos de distribución centrilobulillar y áreas parcheadas de consolidación bilatearles asimétricas.
NEUMONÍAS BACTERIANAS
La TAC puede aportar información limitada en relación a las neumonías bacterianas postTPH.
Los hallazgos que se encuentran son superponibles a los encontrados en la población inmunocompetente,
tales como áreas focales de consolidación o pequeños nódulos de distribución centrolobulillar (figura 7).
Hemorragia alveolar difusa
Se observa aproximadamente en el 20% de los pacientes postTPH.
Tiene una alta tasa de mortalidad,
pero un diagnóstico precoz acompañado de un tratamiento esteroideo puede mejorar la tasa de supervivencia.
Las manifestaciones clínicas son inespecíficas y la hempostisis rara.
Los hallazgos en la TAC consisten en áreas bilaterales de vidrio deslustrado o áreas de consolidación.
El lavado broncoalveolar revela macrófagos cargados de hemosiderina.
Edema pulmonar
Se debe principalmente a la infusión de grandes volúmenes de líquidos a los que se ve sometido el paciente (fármacos,
productos sanguíneos,
nutrición parenteral) junto con la disfunción cardiaca y renal debido a los regímenes previos de quimioterapia.
Los síntomas clínicos son de presentación aguda y los hallazgos en la TAC son aumento del diámetro de los vasos pulmonares,
aumento de la trama intersticial,
áreas en vidrio deslustrado y derrame pleural.
Toxicidad farmacológica
Son muy comunes aunque su patrón en la TAC es inespecífico.
Pueden aparecer áreas bilaterales en vidrio deslustrado,
consolidaciones o áreas de engrosamiento de la trama reticular.
PERIODO INTERMEDIO (días +30 a +100)
Es el periodo que sigue al implante medular y que se caracteriza por un descenso tanto de la inmunidad celular como humoral.
Los dos patógenos más frecuentes en este periodo son el Citomegalovirus (CMV) y Pneumocystis jirovecii.
Otra patología no infecciosa que nos podemos encontrar es la neumonía intersticial idiopática.
Los patógenos a los que nos enfrentaremos con más frecuencia en este periodo son:
- Virus
* Citomegalovirus (CMV).
* Virus Respiratorio Sincitial (VRS)
- Hongos:
* Pneumocystis jirovecii
*Aspergillus: aunque es menos frecuente que en el periodo de neutropenia,
es la infección más temida de este periodo por su alta mortalidad.
* Candida albicans
CITOMEGALOVIRUS
El citomegalovirus (CMV) es uno de los agentes infecciosos más frecuentes en el TPH alogénico.
En la mayor parte de los casos,
la infección es consecuencia de la reactivación de un virus endógeno mantenido en estado latente.
Por ello,
es fundamental conocer el estado serológico del paciente antes del TPH,
ya que los seropositivos serán los de mayor riesgo de presentar esta complicación.
La neumonía intersticial por CMV es por frecuencia y gravedad la principal forma clinica de dicha enfermedad (figura 8).
En la TAC se observan múltiples nódulos pequeños bilaterales (en la antomía patológica corresponden con nódulos hemorrágicos con macrófagos con cuerpos de inclusión con CMV) junto con áreas de consolidación o zonas de vidrio deslustrado (figura 9).
PNEUMOCYSTIS JIROVECII
Cada vez se ven menos debido al tratamiento profiláctico que se instaura en estos pacientes,
por lo que se da sobre todo en los pacientes que no toleran o no reciben dicha profilaxis.
En la TAC se ven áreas de vidrio deslustrado difusas,
de predomio perihiliar o patrón de atenuación en mosaico (figura 10).
Neumonía intersticial idiopática
Se trata de un diagnóstico de exclusión y se define como una lesión tras el TPH en asusencia de infección.
Se debe a la toxicidad por fármacos previos al TPH.
Ocurre aproximadamente en el 12% de los pacientes sometidos a TPH.
En el TAC se observan infiltrados intersticiales inespecíficos.
PERIODO TARDÍO (a partir del día +100)
En este periodo predomina la patología respiratoria de causa no infecciosa,
como la bronquiolitis obliterante,
bronquiolitis obliterante con neumonía organizada (BONO) y EICH crónica.
BRONQUIOLITIS OBLITERANTE
Ocurre en más del 10% de los pacientes que reciben postTPH autólogo y se sospecha que la causa se deba al EICH crónico,
presentándose como episodios de disnea junto con patrón obstructivo irreversible en la espirometría.
En la TAC se ve dilatación bronquial,
patrón de atenuación en mosaico y evidencia de atrapamiento aéreo en espiración.
BONO (bronquiolitis obliterante con neumonía organizada)
Clínicamente se manifiesta como tos no productiva,
disnea y febrícula que responde bien al tratameinto esteroideo.
En la TAC se observan condensaciones parcheadas,
de localización subpleural y peribroncovascular,
acompañdo o no de vidrio deslustrado y de nódulos.
EICH CRÓNICO
Ocurre en casi la mitad de los pacientes que sobreviven más de 6 meses tras el transplante TPH.
Se debe a un ataque de las células del donante contra los tejidos del huésped,
por lo que suele acompañarse de signos y síntomas en otros órganos como la piel,
el hígado o el tracto gastrointestinal (figura 11).