En esta sección abordaremos la revisión del tema siguiendo este esquema Fig. 1:
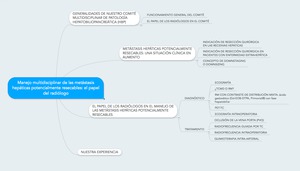
Fig. 1: Mapa mental de nuestra presentación electrónica.
GENERALIDADES DE NUESTRO COMITÉ MULTIDISCIPLINAR DE PATOLOGÍA HEPATOBILIOPANCREÁTICA (HBP)
- FUNCIONAMIENTO GENERAL DEL COMITÉ
- EL PAPEL DE LOS RADIÓLOGOS EN EL COMITÉ
METÁSTASIS HEPÁTICAS POTENCIALMENTE RESECABLES: UNA SITUACIÓN CLINICA EN AUMENTO
- INDICACIÓN DE RESECCIÓN QUIRÚRGICA EN LAS RECIDIVAS HEPATICAS
- INDICACIÓN DE RESECCIÓN QUIRÚRGICA EN PACIENTES CON ENFERMEDAD EXTRAHEPÁTICA
- CONCEPTO DE DOWNSTAGING O DOWNSIZING
EL PAPEL DE LOS RADIÓLOGOS EN EL MANEJO DE LAS METÁSTASIS HEPÁTICAS POTENCIALMENTE RESECABLES
- DIAGNÓSTICO
- ECOGRAFÍA
- ¿TCMD O RM?
- RM CON CONTRASTE DE DISTRIBUCIÓN MIXTA (ácido gadoxético (Gd-EOB-DTPA,
Primovist®) con fase hepatobiliar
- PET-TC
- ECOGRAFÍA INTRAOPERATORIA
- TRATAMIENTO
- OCLUSIÓN DE LA VENA PORTA (PVO)
- RADIOFRECUENCIA GUIADA POR TC
- RADIOFRECUENCIA INTRAOPERATORIA
- QUIMIOTERAPIA INTRA-ARTERIAL
NUESTRA EXPERIENCIA
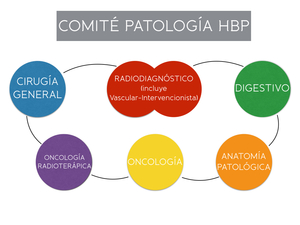
Fig. 2: Composición del comité de patología hepatobiliopancreática de nuestro hospital.
GENERALIDADES DE NUESTRO COMITÉ MULTIDISCIPLINAR DE PATOLOGÍA HEPATOBILIOPANCREÁTICA (HBP)
Los casos clínicos relacionados con el área hepatobiliopancreática representan un grupo de patologías frecuente,
heterogéneo y muchas veces de complicado manejo,
que requieren múltiples y diferentes técnicas para su diagnóstico y abordaje terapéutico,
así como especialistas cualificados de una forma específica para optimizar la atención más adecuada en estos pacientes.
Éste fue el motivo por el que se constituyó el comité HBP en el Complejo Hospitalario de Albacete (CHUA) en 2009,
debidamente acreditado desde la Unidad de Calidad Asistencial.
Forman parte del comité de forma habitual (Fig. 2) especialistas de Cirugía General (Unidad de Patología HBP),
Radiodiagnóstico,
Radiología Intervencionista,
Digestivo,
Oncología,
Oncología Radioterápica y Anatomía Patológica.
Eventualmente acuden otros especialistas para presentar casos relacionados,
principalmente desde Medicina Interna.
Al ser centro de referencia en Castilla-La Mancha,
no sólo se incluyen los pacientes de la Gerencia de Atención Integrada de Albacete,
sino también del resto de la provincia y el Hospital de Cuenca.
El manejo multidisciplinar de estos pacientes ha hecho que se establezcan protocolos,
que se estimule la formación continuada con los diferentes enfoques por especialidad en charlas periódicas monográficas,
que se aprenda de los casos más complejos y que se busque la solución más efectiva posible.
Nos ha permitido un ahorro de pruebas o procedimientos que sin la intercomunicación que nos permite el comité se repetirían o que sin la opinión del otro especialista no tendrían el mismo significado.
También ha permitido ciertas subespecializaciones dentro de cada servicio,
lo que permite una mejora y un avance en el diagnóstico y tratamiento de estos pacientes con optimización de las técnicas diagnósticas y de tratamiento que hasta el momento no se hacían o a las que no se les sacaba el máximo rendimiento.
Como ejemplo de ello,
podemos citgar la propia cirugía de resección de metástasis hepáticas,
así como las ecografías y radiofrecuencias intraoperatorias).
El balance realizado y la experiencia acumulada de los participantes,
nos hace considerar que es una de las mejores herramientas de las que disponemos para conseguir el máximo provecho de nuestros recursos,
puestos al servicio de la mejor atención que somos capaces de brindar a nuestros pacientes.
La puesta en marcha de este Comité ha supuesto esfuerzo y horas de trabajo extra para los miembros que lo componen,
mucha ilusión por realizar un trabajo de equipo bien hecho,
y satisfacción tras comprobar semana a semana que dicho esfuerzo se traduce en una atención que intenta aumentar su calidad día tras día.
Con la formación del equipo multidisciplinar dedicado a la patología hepatobiliopancreática hemos suplido deficiencias que existían en nuestro hospital en el manejo de estos pacientes.
Se han podido solucionar problemas que hasta entonces hacían necesaria la participación de hospitales de otras comunidades como Madrid,
Murcia o la Comunidad Valenciana.
FUNCIONAMIENTO GENERAL DEL COMITÉ
El comité se reúne una vez por semana.
Los casos remitidos incluyen pacientes nuevos,
recidivas de patologías,
actualizaciones sobre el plan diagnóstico y/o de tratamiento de pacientes ya conocidos y resultados relevantes de casos ya presentados previamente.
Estos casos se envían por los clínicos a la Secretaría de Cirugía General,
que centraliza la información y envía al resto de participantes la información pertinente que se tratará en el siguiente comité,
para que todos los participantes conozcan de antemano y puedan revisar los casos adecuadamente.
Tras ser presentados los casos,
se toman las decisiones pertinentes de forma conjunta,
consensuada y vinculante,
enviando el consenso final a todos los participantes una vez finalizada la reunión (Fig. 3).
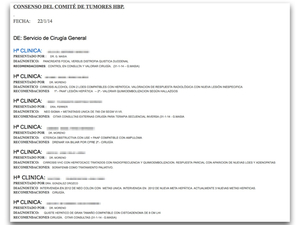
Fig. 3: Ejemplo de uno de los documentos de consenso que se genera tras cada reunión semanal.
EL PAPEL DE LOS RADIÓLOGOS EN EL COMITÉ
Los radiólogos dedicados al diagnóstico preparan las imágenes de los pacientes que se presentan,
comentan las mismas en casos de duda o si aportan interés especial para el manejo del paciente.
También orientan sobre el algoritmo diagnóstico más adecuado en los pacientes en estudio o seguimiento.
Los radiólogos intervencionistas actúan como consultores en su área,
valorando las indicaciones de los diferentes procedimientos que les son requeridos.
METÁSTASIS HEPÁTICAS POTENCIALMENTE RESECABLES: UNA SITUACIÓN CLINICA EN AUMENTO
En España hay más de 20.000 casos/años de cáncer colorrectal (CCR),
encontrando metástasis hepáticas (MH) a lo largo de la enfermedad en un 50-70% de los pacientes: 20-25% sincrónicas y 25-35% metacrónicas.
Entre el 10-15% de estas metástasis son potencialmente resecables.
El concepto de metástasis RESECABLE implica la posibilidad de extirpar las lesiones por completo,
con margen negativo (R0),
sea cual sea su número,
tamaño y localización,
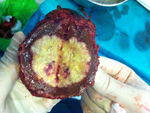
dejando un hígado remanente suficiente para permitir una función hepática normal. Fig. 4
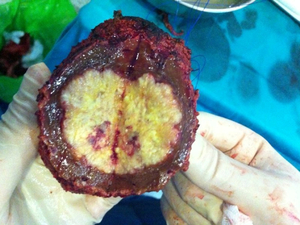
Fig. 4: Evaluación en quirófano por parte del cirujano de una metástasis hepática resecada con margen macroscópico libre.
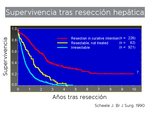
Los datos siguientes reflejan la supervivencia del CCR con MH:
- sin tratamiento: 6-16 meses de supervivencia media (a los 5 años,
nula)
- sólo con quimioterapia: 20% a los 3 años
- resección quirúrgica (R0) + quimioterapia: 42-58% proximadamente a los 5 años (muy variable según las series por la multitud de factores pronósticos implicados).
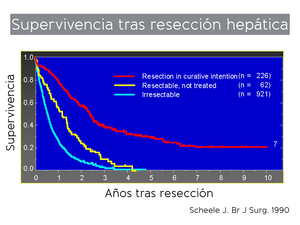
Fig. 5: Gráfica que muestra los datos de supervivencia en pacientes que han sido sometidos a resección de MHCCR.
References: Scheele J et al. Hepatic metastases from colorectal carcinoma: impact of surgical resection on the natural history. Br J Surg. 1990 Nov;77(11):1241-6.
Por tanto,
el tratamiento de elección de las MHCCR es la resección quirúrgica completa de las mismas Fig. 5
Estos resultados cercanos al 60% de supervivencia a 5 años en el último grupo referido anteriormente se ha producido gracias a diversos factores:
- los avances en las técnicas de imagen preoperatorias,
- el perfeccionamiento en las técnicas quirúrgicas y anestésicas,
- la introducción de nuevos agentes citotóxicos y biológicos para la quimioterapia pre y postoperatoria y
- la adecuada selección de los pacientes.
Estos cambios conllevan un aumento en el número de pacientes candidatos a cirugía de resección de MHCCR y un manejo más complejo de dichos pacientes.
Por tanto,
se acepta que el tratamiento de todos los pacientes con CCR así como la indicación quirúrgica de las MHCCR deben ser responsabilidad de un equipo multidisciplinar que incluya a oncólogos,
radiólogos y cirujanos hepáticos para coordinar la actuación más adecuada en cada caso.
En nuestro hospital existe un equipo multidisciplinar encargado de decidir el tratamiento de todos los pacientes con CCR y otro encargado de la patología hepatobiliar que es el que,
en consenso con el de CCR,
decide el tratamiento de los paciente con CCR y metástasis hepáticas.
INDICACIÓN DE RESECCIÓN QUIRÚRGICA EN LAS RECIDIVAS HEPATICAS
En pacientes tratados quirúrgicamente con intención curativa se presentará una recidiva de la enfermedad en alrededor del 60% de casos,
de los cuales en un 20% se tratará exclusivamente de una recidiva hepática y subsidiaria de una segunda resección cumpliendo los mismos criterios de indicación de la primera.
Se ha demostrado que la morbilidad y mortalidad quirúrgica son comparables a la primera resección y se consigue una supervivencia media de entre 32 y 46 meses.
Por tanto,
parece razonable considerar una reintervención en los pacientes con recidiva hepática de la enfermedad si cumplen los criterios seguidos en la indicación de la primera resección.
INDICACIÓN DE RESECCIÓN QUIRÚRGICA EN PACIENTES CON ENFERMEDAD EXTRAHEPÁTICA
Tradicionalmente,
la enfermedad extrahepática estaba considerada casi de manera universal como una contraindicación para la resección de las MHCCR.
Sin embargo,
se ha podido demostrar un índice de supervivencia a 5 años de 12-37% después de la resección del hígado en determinados pacientes con enfermedad extrahepática,
independientemente de su localización (pulmón,
ganglios linfáticos del tumor primario,
retroperitoneales o del pedículo hepático,
carcinomatosis y misceláneos peritoneales.
La presencia de metástasis peritoneales es motivo de controversia,
en alguna serie se considera más importante el número total de metástasis a resecar,
más que la localización,
incluyendo también las peritoneales.
Actualmente hay acuerdo en que metástasis peritoneales localizadas y en pequeño número,
no contraindicarían de forma absoluta la resección.
Las adenopatías metastásicas en el área 1 (hilio hepático o retroduodenales) empeoran el pronóstico pero no contraindican de forma absoluta la extirpación.
Sin embargo,
las metástasis ganglionares en el área 2 (alrededor de la arteria hepática o tronco celíaco) se asocian a tan mal pronóstico que sí deben considerarse una contraindicación para la resección.
Por tanto,
estos pacientes deben ser seleccionados cuidadosamente y debería considerarse la resección en ellos sólo después de confirmar una estabilidad de la enfermedad o tras obtener una buena respuesta a la quimioterapia sistémica y siempre y cuando se vaya a obtener una resección R0 de la enfermedad intra y extrahepática.
CONCEPTO DE DOWNSTAGING O DOWNSIZING
Hace referencia al proceso de convertir con quimioterapia neoadyuvante lesiones metastásicas hepáticas que inicialmente eran irresecables en resecables.
Con los nuevos regímenes de quimioterapia combinando 5-fluorouracilo,
ácido folínico y oxaliplatino o irinotecan,
se ha conseguido rescatar para la cirugía del 10 al 30 % de pacientes,
y se preveen cifras mayores con los nuevos anticuerpos monoclonales (cetuximab y bevacizumab).
Las supervivencias a largo plazo conseguidas en estos pacientes son casi superponibles a las de los pacientes resecados por primera intención.
La cirugía hepática debe ser realizada tan pronto como la enfermedad se convierta en resecable,
sin prolongar la quimioterapia.
La progresión del tumor durante la administración de la quimioterapia neoadyuvante,
debe ser considerada una contraindicación relativa a la resección.
Otras formas de aumentar la resección de las MH son la cirugía programada en dos tiempos,
la resección combinada con radiofrecuencia,
la radioterapia intraarterial con esferas de Ytrio y la embolización portal.
Fig. 6

Fig. 6: Existen diferentes formas de convertir metástasis hepáticas irresecables en resecables.
EL PAPEL DE LOS RADIÓLOGOS EN EL MANEJO DE LAS METÁSTASIS HEPÁTICAS POTENCIALMENTE RESECABLES
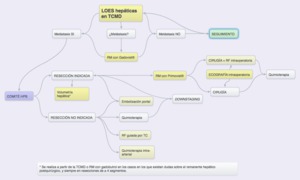
Fig. 7: Algoritmo de manejo de las MHCCR en nuestro centro. Se resaltan en amarillo los pasos en los que participa directamente el Servicio de Radiodiagnóstico, tanto en el área de diagnóstico como el de tratamiento.
DIAGNÓSTICO
La detección precoz y adecuada caracterización de las MH en el CCR es crítica a la hora de abordar el tratamiento del paciente para aumentar sus posibilidades de supervivencia.
Fig. 7
Lo que el radiólogo debe aportar al cirujano hepático es:
- Determinar número,
tamaño,
localización y resecabilidad de las metástasis hepáticas.
- Posible existencia de adenopatías metastásicas en hilio hepático.
- Valorar posible enfermedad extrahepática (abdominal,
pélvica,
pulmonar).
- Estadificar el tumor primario en caso de metástasis sincrónicas.
ECOGRAFÍA
Se realiza en casos seleccionados para complementar la caracterización de las lesiones hepáticas,
haciendo el diagnóstico diferencial entre lesiones quísticas y sólidas,
especialmente en las de pequeño tamaño.
En ocasiones,
también se recurre a ella de forma preoperatoria para confirmar la localización de cara a la ecografía intraoperatoria.
¿TCMD o RM?
El estudio de rutina para estadiar y seguir los pacientes con CCR se realiza con TCMD.
Por este motivo,
se trata generalmente de una adquisición única hepática.
Si se conoce previamente por otros estudios la existencia o sospecha de lesiones focales hepáticas,
se planificará un estudio trifásico hepático.
Si con el estudio TCMD no se puede confirmar el diagnóstico de metástasis,
se realizará una RM hepática con gadolinio de distribución extracelular no específico (estudio dinámico),
en nuestro caso utilizamos gadobutrol (Gadovist®).
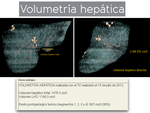
La realización de una volumetría hepática (Fig. 8) se reserva para pacientes seleccionados.
Se hace a partir de la TCMD o RM con gadobutrol en los casos en los que existan dudas sobre el remanente hepático postquirúrgico y siempre en resecciones de ≥ 4 segmentos.
Se considera volumen hepático remanente insuficiente si es < 25% en hígados sanos y < 35% en hígados patológicos (diabéticos o esteatosis por quimioterapia previa).
En nuestro hospital se hace en la estación de trabajo del equipo TCMD por la facilidad de uso que nos ofrece el software respecto al de la RM.
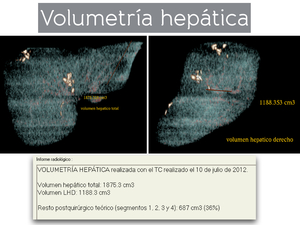
Fig. 8: Volumetría hepática realizada en la estación de trabajo de nuestro equipo TCMD General Electric, en un paciente intervenido de resección hepática por MHCCR previa (ver clips metálicos), en el que aparecieron 2 nuevas lesiones metastásicas y se planteó nueva cirugía para resección de las mismas en el comité HPB.
RM CON CONTRASTE DE DISTRIBUCIÓN MIXTA (ácido gadoxético (Gd-EOB-DTPA,
Primovist®),
realizando fase hepatobiliar
En caso de confirmarse el diagnóstico de metástasis,
tras plantear el caso en el comité se planificará una RM con Primovist® Fig. 9 si se decide resección quirúrgica,
realizada preferiblemente la misma semana de la intervención.
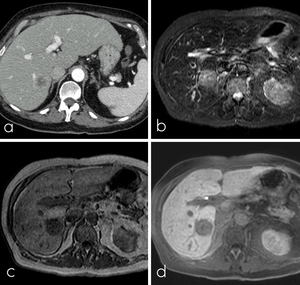
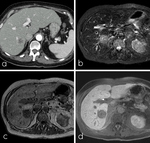
Fig. 9: Paciente con metástasis hepática única secundaria a CCR: a) TCMD con contraste iv; b) RM transversal STIR; c) RM transversal T1 y d) RM transversal T1 con supresión grasa tras administración de Primovist®, con adquisición tardía a los 30 minutos.
El objetivo de realizar la RM con Primovist® después de haber realizado otras pruebas previamente es confirmar con la mayor sensibilidad posible el número,
tamaño y localización de las metástasis hepáticas de forma previa a la cirugía para evitar hallazgos inesperados durante la misma.
En los primeros pacientes valorados en nuestro comité,
antes de establecerse los protocolos actuales,
no se hacía de rutina,
muchas veces por falta de coordinación entre el Servicio de Cirugía y el de Radiodiagnóstico.
De esta forma,
encontramos varias discordancias entre los hallazgos de TCMD y RM con gadolinio frente a los hallazgos en quirófano,
sobre todo en lesiones de pequeño tamaño.
Estas discordancias han disminuido drásticamente desde que realizamos de forma coordinada la RM con Primovist® por protocolo antes de cada resección quirúrgica.
La RM con ácido gadoxético (Gd-EOB-DTPA) realizando una adquisición tardía en fase hepatobiliar aumenta la sensibilidad para detectar metástasis hepáticas frente al estudio estándar con contraste de gadolinio extracelular detectando lesiones hasta menores de 1cm.
Resulta de utilidad añadir secuencias de difusión para aumentar más la exactitud diagnóstica.
PET-TC
No se realiza sistemáticamente ya que para la detección de metástasis hepáticas otras técnicas como la RM ha demostrado una mayor sensibilidad.
Se realiza en algún caso seleccionado para la detección de enfermedad extrahepática no identificada por TC o RM en los casos que se consideran resecables.
ECOGRAFÍA INTRAOPERATORIA Fig. 10
Se realiza siempre.
En nuestro hospital la realizan conjuntamente los cirujanos y los radiólogos.

Fig. 10: Equipo de ecografía que se utiliza en quirófano.
TRATAMIENTO
OCLUSIÓN DE LA VENA PORTA (PVO) PARA AUMENTAR EL VOLUMEN HEPÁTICO REMANENTE Fig. 11
El objetivo de la embolización portal es la redistribución del flujo portal hacia los segmentos del hígado restante tras la cirugía,
hipertrofiando el lóbulo contralateral y aumentando el remanente hepático entre un 10-15% en 3-9 semanas,
aunque en hígados con patologías crónicas puede ser menor.
Se puede hacer antes de la cirugía hepática o entre 2 cirugías hepáticas.
La PVO se puede realizar percutáneamente con control ecográfico y fluoroscópico,
con el paciente bajo sedación y consciente en la sala de radiología intervencionista y sin necesidad de laparotomía.
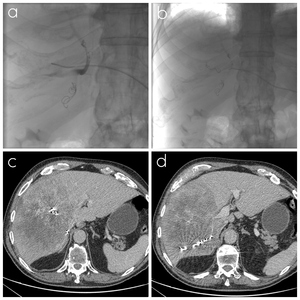
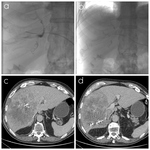
Fig. 11: Las figuras a) y b) son adquisiciones radiográficas durante el procedimiento de embolización portal. Las figuras c) y d) muestran el resultado final en una TCMD de control.
Las indicaciones para la embolización portal dependen de los factores que afectan al volumen residual hepático que se necesita para mantener una adecuada función hepática tras la resección.
La presencia de patología hepática subyacente,
haber recibido quimioterapia preoperatoria,
el IMC del paciente,
el tipo de resección prevista,
así como las comorbilidades del paciente son factores a tener en cuenta.
Por todo ello,
el límite del volumen residual para una resección segura varía de un paciente a otro.
Indicaciones de PVO:
- En pacientes con un hígado sano,
cuando el volumen residual calculado es ≤20% (el bisegmento lateral izquierdo -II y III- supone el 20% del volumen total en más del 75% de pacientes en ausencia de hipertrofia).
- En pacientes que han recibido quimioterapia preoperatoria cuando el volumen residual calculado es ≤30%.
- En los pacientes con fibrosis o cirrosis hepática se indicará la PVO cuando el volumen residual es ≤40%.
RADIOFRECUENCIA GUIADA POR TC
Se considera terapia paliativa,
no sustituye a la resección quirúrgica si ésta es técnicamente factible,
ya que sus resultados en términos de supervivencia a largo plazo son inferiores a los de la resección,
aunque recientemente se han obtenido supervivencias comparables a 3 años.
Sólo sustituirá la resección quirúrgica en caso de que las condiciones generales del enfermo desaconsejen ésta última.
Puede estar indicada en caso de metástasis peritoneales limitadas.
En algunos casos puede asociarse a resección de otras metástasis,
cuando la resecabilidad es técnicamente dificultosa o de radicalidad dudosa.
Esta asociación conlleva una supervivencia inferior a la de los pacientes en quienes se han resecado todas aunque superior al tratamiento exclusivo con RF y al tratamiento únicamente quimioterápico.
Esta práctica se encuentra en evaluación.
Existen diferentes técnicas que finalmente inducen necrosis coagulativa,
obteniendo resultados bastante similares.
En nuestro hospital utilizamos la ablación por radiofrecuencia (RF),
que induce esta necrosis coagulativa inducida por calor agitando las moléculas de agua a través de una corriente alterna producida por una antena monopolar en un radio de varios milímetros hasta 3-5 cm.
En función del volumen tratado,
las recurrencias en MHCCR se describen entre 12-31%,
con un porcentaje de 2.8% de complicaciones mayores y un 17% de complicaciones menores.
En pacientes con pequeño volumen tumoral,
se ha llegado a describir supervivencias del 50% a los 5 años,
aunque la mayor parte de los estudios reflejan porcentajes de un 35% aproximadamente.
Tras la realización de RF en las MHCCR,
puede encontrarse un fino anillo de realce marginal en fase arterial tardía hasta 4-5 meses tras el procedimiento.
Se considera que el procedimiento ha sido adecuado,
si en los controles posteriores,
va desapareciendo este anillo y no se observa realce en la fase portal.
Si existe aumento de tamaño de la lesión tras 6 semanas de la RF o distorsión progresiva del margen lesional,
debe considerarse la existencia de progresión local.
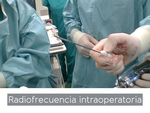
RADIOFRECUENCIA INTRAOPERATORIA Fig. 12
Cuando es posible,
preferimos realizar la RF en el quirófano,
al mismo tiempo que la resección quirúrgica en aquellas lesiones que no pueden ser resecadas,
de acuerdo con las decisiones tomadas en el comité.
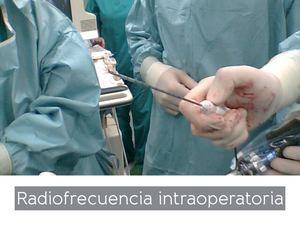
Fig. 12: Preparación de un procedimiento de radiofrecuencia guiada por ecografía en quirófano.
QUIMIOTERAPIA INTRA-ARTERIAL
En caso de tumores irresecables,
la quimioterapia intraarterial hepática con floxuridina para las metástasis del hígado ha producido mayores tasas de respuesta global pero no mejoría constante en la supervivencia cuando se compara con la quimioterapia sistémica.
En nuestro hospital tenemos escasa experiencia con este tratamiento.
NUESTRA EXPERIENCIA
Entre octubre de 2009 y septiembre de 2013 hemos recogido 42 pacientes con 50 procedimientos quirúrgicos realizados para resección de MHCCR.
7 pacientes necesitaron una segunda intervención por recidivas hepáticas.
1 paciente fue sometido a 3 intervenciones quirúrgicas para resección de metástasis hepáticas.
De nuestra serie,
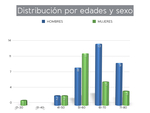
35 resecciones se realizaron en hombres y 15 en mujeres (Fig. 13).
La edad media de todos los pacientes fue 63,2 años y la mediana 64 años (Fig. 14).
La edad máxima fue 78 años y la mínima 27 años.
En los hombres,
la edad media fue 64,2 años y la mediana 62 años.
En las mujeres,
la edad media fue 61 años y la mediana 60 años.
El número de resecciones hepáticas ha ido aumentando progresivamente conforme la Unidad de Cirugía hepática ha ido adquiriendo más experiencia,
de 3 pacientes operados en 2010 a 20 pacientes en 2012 (Fig. 15).
Así mismo,
la experiencia de los radiólogos que intervienen en el manejo de los pacientes se ha ido incrementando de la misma forma,
por un lado en cuanto a la actualización de los protocolos y por otro,
a la realización de más procedimientos tanto diagnósticos (volumetrías,
RM con Primovist@) como de tratamiento (ecografías y RF intraoperatorias,
PVO).
Fig. 16
Muchos pacientes fueron operados al principio con una única prueba de imagen (TCMD),
encontrando como posibles causas de esta situación la falta de coordinación y comunicación entre el Servicio de Cirugía y el de Radiodiagnóstico y también la falta de experiencia de los facultativos implicados.
La aparición de discordancias entre los hallazgos de una prueba única y los obtenidos en quirófano nos obligaron a replantear los algoritmos de actuación,
acelerando nuestra curva de aprendizaje,
tanto en el manejo de esta patología como en la dinámica de trabajo de un equipo multidisciplinar.
Todos los casos fueron operados con un estudio de TCMD previo y una ecografía intraoperatoria.
En 9 casos (18%) se realizó RM con gadolinio iv para confirmar el diagnóstico de metástasis.
En 19 casos (38%) se realizó RM con Primovist@ como estudio preoperatorio para confirmar el número y localización de las metástasis.
Estos casos han ido aumentando progresivamente durante estos años y en 2013 un 70% tenían este estudio previo a la cirugía.
A 4 pacientes (9%) se les realizó una PVO para aumentar el remanente hepático,
siendo valorados de forma complementaria con una volumetría hepática pre y postratamiento para controlar el crecimiento hepático.
En 4 pacientes se realizó una RF intraoperatoria,
todas ellas en 2013.
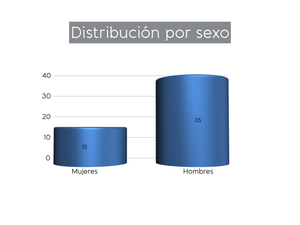
Fig. 13: Distribución por sexo.
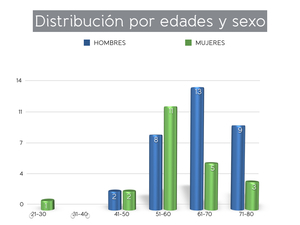
Fig. 14: Distribución por edades y sexo.
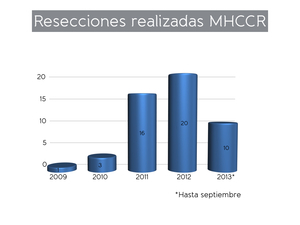
Fig. 15: Número de resecciones MHCCR realizadas entre 2009 y septiembre de 2013.
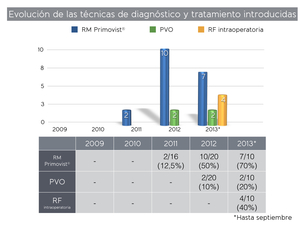
Fig. 16: Evolución de las técnicas de diagnóstico y tratamiento introducidas.
Por tanto,
en estos 4 años hemos adquirido experiencia,
hemos mejorado la comunicación entre los diferentes Servicios y hemos adoptado nuevos protocolos de actuación (Fig. 7).