La epilepsia de origen temporal es la epilepsia farmacorresistente más frecuente,
y suele afectar a las estructuras localizadas en la región medial del lóbulo temporal,
tales como el hipocampo y la amígdala.
En estos casos,
la RM tienen un papel fundamental ya que permite detectar posibles lesiones estructurales,
facilita la toma de decisiones y plantea posibles tratamientos.
Además,
en los casos susceptibles de un manejo quirúrgico ayuda a predecir el pronóstico de los pacientes
Para ello es imprescindible la realización de un estudio de RM con un protocolo específico que nos permita una correcta valoración del lóbulo temporal.
En nuestro centro,
que disponemos de equipos de 1.5T,
realizamos el siguiente protocolo:
- Secuencia volumétrica 3D T1 High Resolution (HR) en proyección axial (grosor de corte 1.6 mm,
ZIP x 2)
- Secuencia volumétrica 3D T1 HR en proyección coronal* (grosor de corte 1.8 mm,
ZIP x 2)
- Secuencia T2 en proyección axial y coronal* con cortes de 3mm y un gap de 0.3 mm.
- Secuencia FLAIR en proyección axial y coronal* con cortes de 4 /0.4 mm.
(*deben ser perpendiculares al hipocampo)
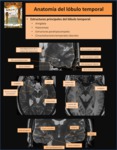
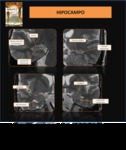
Es además fundamental un correcto conocimiento de la anatomía del lóbulo temporal y su correlación con las técnicas de imágen.
( Fig. 2 y Fig. 3 )
Posteriormente revisaremos brevemente las principales alteraciones estructurales que cursan con crisis temporales,
y las clasificaremos según su etiopatogenia en:
1) ALTERACIONES DEL DESARROLLO
2) PATOLOGÍA TUMORAL
3) ENFERMEDADES INFECCIOSAS
4) LESIONES VASCULARES
5) ENCEFALITIS LÍMBICAS
6) MISCELÁNEA
1.
ALTERACIONES DEL DESARROLLO:
1.1 ESCLEROSIS MESIAL TEMPORAL (EMT)
La esclerosis del hipocampo o EMT es la alteración estructural más frecuentemente encontrada en los estudios de imagen de los pacientes que acuden con crisis de origen temporal,
y la causa más importante de epilepsia refractaria. Histológicamente,
se caracteriza por pérdida neuronal,
reorganización sináptica en las fibras musgosas
y astrogliosis, con afectación del hipocampo,
siendo el cuerpo la zona más frecuentemente afectada seguido de la cola,
la cabeza y la amígdala. Aunque la causa de la ETM no está claramente establecida,
y probablemente no sea única,
se admite que algún tipo de agresión durante el desarrollo lesiona el hipocampo en individuos predispuestos que tras el inicio de las crisis desarrollan EMT.
Hasta en el 22% de los casos coexiste con una segunda lesión,
lo que se conoce con el nombre de "lesión “dual”,
siendo las mas frecuentes las displasias corticales ( Fig. 4 ).
Como consecuencia de la pérdida neuronal del asta de Amon del hipocampo con posterior desarrollo de gliosis,
los hallazgos de la RMl os podemos dividir en:
- Secundarios a la atrofia del hipocampo: ( Fig. 4)
- Dsiminución del volumen con pérdida de las interdigitaciones de la cabeza y/o de la arquitectura interna
- Dilatación del asta temporal ipsilateral
- Atrofia ipsilateral del fórnix y cuerpo mamilar
- Atrofia del lóbulo temporal
- Secundario a la Gliosis: ( Fig. 4)
- Hiperseñal en las secuencias potenciadas en T2 y FLAIR del hipocampo.
- Pérdida de la intensidad se señal normal de sustancia blanca del lóbulo temporal entre el hipocampo y el surco colateral.
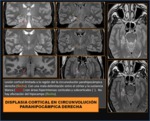
1.2 DISPLASIA CORTICAL FOCAL (DCF)
Las displasias corticales forman un espectro de alteraciones del desarrollo cortical que varían desde una leve afectación de la corteza hasta una más profunda alteración del cortex,
a veces asociada a otras lesiones como la esclerosis mesial ( Fig. 4 ) o lesiones tumorales de escaso potencial proliferativo como los DNET o los tumores neurogliales.
Es muy importante detectar y caracterizar las displasias corticales porque el tratamiento quirúrgico y el pronóstico varían.
Histológicamente,
los hallazgos más frecuentes en las DCF son la desorganización de la arquitectura del córtex («dislaminación»),
el aumento de neuronas de la capa molecular,
aumento de tamañno de algunas neuronas (citomegalia) o la presencia de neuronas displásicas y de células balonadas (37%).
La clasificación que propone Palmini se basa en estos datos histológicos y agrupa las DCF en tipo I,
que engloba las lesiones con
dislaminación o citomegalia y tipo II (tipo Taylor) ( Fig. 5) que incluye las que presentan también neuronas dismórficas con células balonadas.
El interés que tiene diferenciar estos dos grupos ( Fig. 6 ) se basa en publicaciones recientes que plantean la posibilidad de distinguirlos con RM,
y,
sobre todo,
en que tienen características clinicopatológicas y pronóstico postquirúrgicos diferentes.
Ambos grupos presentan algunos signos de imagen característicos.
Entre los signos típicos de una Displasia cortical cabría destacar:( Fig. 5 )
- Alteración del patrón normal de las circunvoluciones
- Engrosamiento cortical
- Pérdida de la diferenciación de la unión sustancia gris - sustancia blanca
- Alteración de la señal en la sustancia blanca,
aunque sin efecto expansivo
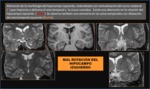
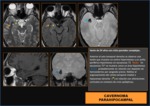
1.3 MALROTACIÓN HIPOCAMPAL ( Fig. 7 )
Las anomalías en la conformación del hipocampo han sido descritas en relación a múltiples entidades,
principalmente alteraciones congénitas,
en la epilepsia del lóbulo temporal y en la Enfermedad de Alzheimer,
entre otras.
La malrotación del hipocampo es secundaria a un defecto en la inversión de la lámina cortical medial que origina el hipocampo.
Esta alteración se ha visto en pacientes con epilepsia,
malformaciones y en anomalías del desarrollo cortical.
La malrotación hipocampal,
hace referencia a un hipocampo situado en una localización anormalmente medial,
que no ha rotado hacia la profundidad,
dentro de la pared medial del lóbulo temporal.
Suele presentar una morfología ovalada en el plano coronal,
en la que el diámetro craneocudal es similar ó mayor que el transverso.
El asta temporal aparece dilatada y la cisura coroidea prominente.
La estructura interna de la circunvolución hipocampal se desdibuja,
manteniéndose el tamaño y la señal interna normales.
Se ha descrito que aunque en pacientes epilépticos la tasa de malrotación es mayor,
no se ha podido describir una causalidad entre la malrotación y la epilepsia del lóbulo temporal.
No obstantese se sospecha que la malrotación hipocampal puede establecer un sustrato que facilite la aparición de crisis y pérdida neuronal,
que conlleven a la aparición de esclerosis hipocampal y la posterior aparición de epilepsia del lóbulo temporal .
2. PATOLOGÍA TUMORAL:
Las neoplasias encontradas en pacientes que cursan clínicamente con crisis temporales son generalmente tumores de bajo grado y lento crecimiento,
por ejemplo gangliogliomas,
gangliocitomas,
DNET o astrocitomas de bajo grado.
En el 90% de los casos afectan al córtex temporal o se sitúan próximas al mismo.
No suelen asociar edema ni efecto de masa.
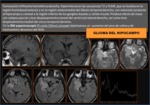
Los astrocitomas de bajo grado de tipo astrocitoma fibrilar (grado II de la OMS) aparecen en RM como lesiones hiperintensas de morfología infiltrativa que afectan al córtex y a la sustancia blanca subcortical,
y sin captación patológica de contraste (Fig. 8).
Los Tumores neuro-gliales (gangliogliomas/ gangliocitomas) son tumores neuroepiteliales bien diferenciados (grado I de la OMS) compuestos por células neoplásicas ganglionares (gangliocitoma) o por combinación de célulares ganglionares con células neoplásicas gliales (gangliogliomas).
Constituyen menos del 2% de todos los tumores cerebrales y tienen predilección por los niños y adultos jovenes.
En más del 70% afectan al lóbulo temporal y los pacientes suelen cursar clínicamente con crisis de larga evolución.
En RM aparecen como lesiones relativamente bien circunscritas,
sólidas o quísticas,
con nódulo mural,
que a veces asocian calcificaciones,
siendo el patrón de captación de contraste de las mismas variable (Fig. 9).
Los tumores neuroepiteliales disembrioplásticos (DNET) son tumores benignos que aparecen en adultos jóvenes como lesiones corticales multiquísticas o multinodulares,
hiperintensas en secuencias T2 y que raramente muestran captación de contraste.
3. ENFERMEDADES INFECCIOSAS:
Las infecciones con afectación cortical como la tuberculosis,
neurocisticercosis o las encefalitis virales pueden ser causa de epilepsia tanto en fase aguda,
por la respuesta inflamatoria local, como en las fases crónicas por la atrofia-gliosis secundaria.
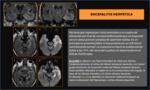
La encefalitis herpética pertenece al grupo de encefalitis infecciosas,
siendo la entidad más prevalente,
sobre todo la producida por el herpes simple tipo 1.
Todos los virus de la familia herpes comparten una estructura molecular común: un core o núcleo de DNA de doble cadena lineal,
una cápside,
una envuelta amorfa ( tegumento) y una envuelta de gliocoproteínas virales.
Son las diferencias en las glicoproteínas de la superficie lo que les confiere las diferencias a los diferentes virus de la familia.
La infección del SNC por los virus de la familia herpes pude ser por VIA HEMATÓGENA o bien por TRANSMISIÓN NEURONAL a partir de un foco de infección extracerebral.
La forma de transmisión neuronal es el mecanismo de infección en los casos producidos por VHS-1,
que es el agente patógeno más prevalente de las encefalitis de origen viral. En este caso el virus invade y se acantona en el ganglio de Gasser e invade el SNC a través de los axones.
Los pacientes cursan con fiebre,
crisis y déficit neurológico progresivo con una morbilidad y mortalidad hasta 50-70% sin tratamiento (ACICLOVIR).
El LCR puede ser negativo para la reacción en cadena de la polimerasa (PCR) – amplificación DNA viral en las primeras 48-72 h y después de 10 días.
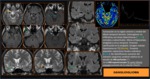
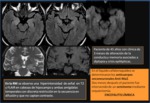
Hallazgos en la RM:
La sensibilidad de la RM en la detección de alteraciones en pacientes con encefalitis herpética es del 90%.
- Afectación bilateral y asimétrica con áreas de hiperintensidad de señal en relación con edema,
hemorragia y necrosis.
- Es posible identificar pequeños focos de hemorragia subaguda(añadir secuencias eco de gradiente en las fases subagudas de la enfermedad) ( Fig. 10)
- La captación de contraste aparece en fases más tardías en forma de un realce giral ( Fig. 10)
- Los ganglios de la base están generalmente respetados.
La secuencia de difusión (DWI) es de gran utilidad,
ya que puede revelar alteraciones no visibles en las secuencias de RM convencional,
sobre todo en la fase aguda,
ya que las áreas de hiperintensidad de señal en secuencias T2 y FLAIR pueden no ser evidentes hasta transcurridas 48 horas desde el comienzo de la enfermedad.
La causa de esta restricción en difusión es la naturaleza citotóxica que cursa con necrosis del parénquima cerebral ( Fig. 11).
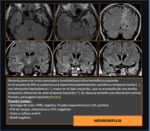
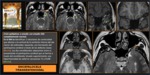
Dentro de las patologías de origen infeccioso,
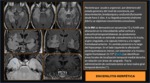
la neurosífilis debe considerarse dentro del diagnóstico diferencial de la encefalitis VHS.
La neurosífilis se puede producir en cualquier momento desde la inoculación inicial hasta el último estadio de sífilis terciaria.
Hallazgos en la RM: ( Fig. 12)
- Hiperintensidad bilateral y asimétrica temporal medial,
secundario al edema y gliosis así como debido al incremento de la permeabilidad vascular.
- Atrofia temporal y dilatacion de astas temporales
4.
LESIONES VASCULARES :
Las malformaciones vasculares constituyen el 5% del sustrato epileptógeno en pacientes con epilepsia.
Las MAV (malformaciones arterio-venosas) y los cavernomas (Fig. 13) son las malformaciones vasculares mas frecuentes.
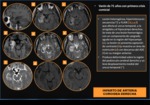
El infarto puede ser tambien una causa de epilpesia sobre todo en adultos.
No es infercuente que pacientes con infartos agudos presenten síntomas que puedan confundirse clinicamente con crisis agudas.
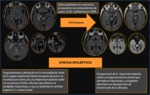
En estos casos el CT o la RM pueden sugerir las existencia de una lesión isquémica (Fig. 14).
Sin embargo es conveniente conocer y no confundir con una isquemia,
los cambios en el parénquima cerebral que pueden aparecer en la RM secundarios al status epiléptico. (Fig. 15)
Se han descrito alteraciones sobre todo en la sustancia gris cortical pero también en ocasiones en sustancia gris profunda como los ganglios basales y tálamo.
Los estudios de RM muestran alteraciones en secuencias FLAIR y en secuencias difusión,
que generalmente son reversibles.
En general, los cambios que refleja la RM están relacionados con la respuesta metabólica,
el aumento de la actividad neuronal y el incremento del aporte vascular que tiene lugar durante la crisis. Se produce un edema vasogénico por la rotura de la barrera hematoencefálica y el aumento del flujo vascular en el foco de actividad epileptógena,
que en la RM se manifiesta con hiperintensidad en T2 y FLAIR,
áreas de hipervascularización cerebral en el estudio de perfusión y un realce leptomeníngeo o giriforme con la administración de contraste iv.
También se desarrolla edema citotóxico, que en DWI muestra restricción.
Por tanto se sabe que existe daño celular,
que en estos casos es reversible.
Ambos tipos de edema y sobre todo el citotóxico,
se correlacionan con la frecuencia y la duración de las crisis.
Estas lesiones no presentan efecto masa,
pueden ser uni o bilaterales y su principal característica es la transitoriedad,
con un intervalo hasta su resolución muy variable,
que oscila entre 1 y 12 meses.
Es por tanto el diagnóstico diferencial fundamentalmente debe realizarse con el infarto isquémico.
6.
ENCEFALITIS LÍMBICAS:
Descrita por primera vez en 1960 por Brierley y cols.,
quienes describieron 3 casos de pacientes con encefalitis subaguda que afectaba al sistema límbico.
Se caracterizan por una presentación subaguda con alteraciones cognitivas,
convulsiones,
confusión,
trastornos psiquiátricos (depresión,
irritabilidad,
alucinaciones) y el desarrollo de déficit de memoria a corto plazo En 1968 Corsellis y cols.
acuñaron el término de “encefalitis límbica”y establecieron su relación con determinados tipos de neoplasias sistémicas
Pueden tener un origen infeccioso o autoinmune (paraneoplásico o no paraneoplásico)
a.
Encefalitis infecciosas: (vista en apartado 3.)
b.
Encefalitis autoinmunes: (Fig. 16)
Causa más frecuente de epilepsia del lóbulo temporal en adultos.
Es un trastorno neurológico subagudo mediado por células T y anticuerpos,
estos anticuerpos pueden se contra antígenos de membrana o intracelulares.
Los antígenos intracelulares incluyen Hu,
CV2,
amphiphysin,
Ri,
Yo y Ma2 y se conocen con el nombre de antígenos onconeuronales.
Las neoplasias asociadas con estos antígenos son el carcinoma microcítico de pulmón,
tumores testiculares ( Fig. 17 ),
teratoma ovárico y carcinoma de mama,
pero la presencia de estos antígenos no implica necesariamente una encefalitis paraneoplásica.
Los antígenos de membrana incluyen los canales de potasio voltaje dependientes.
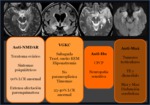
Los hallazgos en la RM aunque varía en algunos casos,
suele observarse una hiperintensidad en las secuencias potenciadas en T2 y FLAIR en cabezas de hipocampo y ambas amígdalas temporales con discreta restricción en la secuencia en difusión y que no captan contraste ( Fig. 18 ).
6.
OTRAS:
Existen otras patologías menos frecuentes que podemos encontrar en pacientes con crisis de origen temporal.
Entre otras se encuentran las variantes anatómicas del lóbulo temporal o malformaciones congénitas,
como los encefaloceles...
( Fig. 19).
Existen además cuadros de epilepsia temporal como consecuencia de secuelas traumáticas tras TCE y secundarias a tratamientos previos como radioterapia o agentes quimioterápicos.