El ictus cursa con un déficit neurológico focal o global y puede ser de causa isquémica o hemorrágica.
En el área de parénquima cerebral isquémico se pueden distinguir dos zonas:
- Área infartada: zona irrecuperable secundaria a una isquemia severa ocasionada por un flujo menor de 10 ml/min/100g mantenido durante 2-3 horas.
- Área de penumbra: zona recuperable que rodea el área infartada que ha sufrido una disminución del flujo de 15-20 ml/min/100g.
Si la disminución del flujo se mantiene puede convertirse en área infartada.
La utilización de trombolíticos en fases precoces del ictus (3-4,5 horas) ha disminuido la morbimortalidad,
al repermeabilizar el área isquémica recuperable disminuyendo el área infartada final.
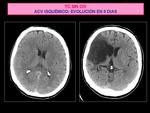
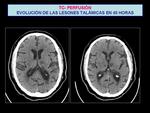
La Fig. 1 muestra la evolución de una accidente cerebrovascular isquémico no subceptible de tratamiento fibrinolítico,
que no presenta hallazgos significativos en las primeras horas de presentación de la clínica con hipodensidad extensa a los 8 días.
En nuestro centro disponemos de un TC General Electrics de 64 coronas con el que realizamos los estudios de código ictus.
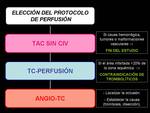
En los pacientes sin criterios de exclusión para recibir tratamiento con trombolíticos se realizan como protocolo de código ictus tres estudios Fig. 2 :
- La TC sin contraste intravenoso (CIV) que permite descartar la presencia de una causa distinta a la isquémica.
- La TC-perfusión que establece si existe y en que porcentaje parénquima recuperable con el tratamiento trombolítico.
- La angio-TC de troncos supraaórticos (TSA) y polígono de Willis para detectar la causa vascular que lo ha originado.
METODOLOGÍA EN LA ESTACIÓN DE TRABAJO PASO A PASO
1º SELECCIÓN DEL PROTOCOLO
Si el paciente es susceptible de tratamiento trombolítico se selecciona desde el inicio el protocolo de TC perfusión en la estación de la TC que incluye secuencialmente una TC basal sin civ,
el estudio de perfusión con civ y una angio-TC de TSA Fig. 2 .
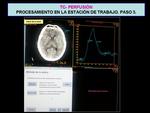
2º TC BASAL SIN CIV
Se realiza un estudio cerebral sin civ sin angulación.
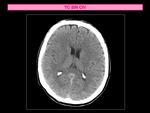
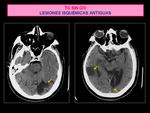
- Si el paciente no presenta hallazgos significativos Fig. 3 , se observan signos precoces de ACV isquémico o lesiones isquémicas antiguas no excluyentes de tratamiento trombolítico Fig. 4 se continua el estudio con la TC de perfusión .
Se incide en la detección de hallazgos hiperagudos de ACV isquémico en el territorio de la arteria cerebral media (ACM) como: borramiento de los surcos, hipodensidad de los ganglios basales(GGBB) o del aprénquima cerebral,
pérdida de la diferenciación sustancia gris (SG)/sustancia blanca (SB) en la cisura de Silvio y ACM hiperdensa.
- Si el paciente presenta otra patología causante de la clínica como hemorragias,
neoplasias o malformaciones vasculares se da por finalizado el estudio.
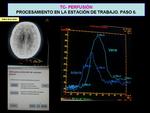
3º TC DE PERFUSIÓN
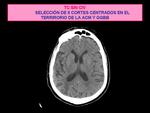
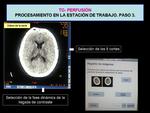
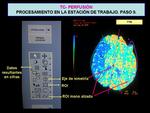
- Se seleccionan 8 cortes centrados en el área a estudio,
normalmente en el territorio de la ACM / GGBB Fig. 5 .
Se dirige el sentido de los cortes en dirección caudocraneal para que se realicen secuencialmente según la llegada del contraste yodado.
Se administran 50 cc de contraste yodado a una velocidad de 4 cc/sg. Se realizan sobre los 8 cortes seleccionados cortes rápidos seriados (cine) en 99 fases de modo que obtenemos un total de 792 imágenes de TC perfusión.
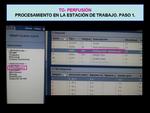
- En la estación de trabajo se selecciona el estudio de perfusión del paciente que contiene 792 imágenes y se cargan en el visualizador a través de la aplicación de la estación CT Perfusión 4 Fig. 6 .
Podemos optar por realizar el análisis con la aplicación "Ataque cerebral" manual o automático Fig. 7 .
La pantalla de la estación queda dividida en cuatro cuadrantes donde podremos ir visualizando varios mapas y gráficos a la vez.
- "Ataque cerebral" manual:
1.
Tiempo: Comprobamos que el paciente no se ha movido en las imágenes "datos de la serie" que se sitúa en la zona superior izquierda donde podemos ver el estudio dinámico con la llegada de contraste en cada corte Fig. 8 .
Si hay algún corte en el que el paciente se ha movido seleccionamos "aplicar registro" hasta que el estudio quede lo menos artefactado por movimientos posible.
Siguiente.
2.
Umbrales de procesamiento: establecidos de base.
Eliminan de la imagen el hueso Fig. 9 .
Siguiente.
3.
Entrada de la arteria: podemos localizar de forma automática una arteria.
Si la curva resultante no es óptima podemos colocar manualmente un ROI sobre la zona de la arteria que seleccionemos,
de modo que el programa busca la mejor curva arterial dentro del área del ROI.
Las curvas vasculares se situaran en la pantalla en la zona superior derecha Fig. 10 .
Siguiente.
4.
Vena para corrección de volumen parcial: podemos localizar de forma automática una vena.
Si la curva resultante no es óptima podemos colocar manualmente un ROI sobre la zona de la vena que seleccionemos,
de modo que el programa busca la mejor curva venosa dentro del área del ROI.
Si las curvas vasculares se salen de la gráfica,
para disminuir su tamaño y visualizarlas en su totalidad,
situamos el ratón sobre la gráfica y presionamos la barra espaciadora Fig. 11 .
Siguiente.
5.
Última imagen prerealce y primera imagen prerealce: corresponde a la última imagen sin civ previa a la llegada de contraste en fase arterial y a la última imagen con contraste tras la fase venosa respectivamente.
La aplicación suele seleccionarloas adecuadamente de forma automática pero tenemos la posibilidad de modificarlas Fig. 12 .
Siguiente.
6.
Ajustes finales: presenta un resumen de los parámetros seleccionados previamente Fig. 12 .
Calcular.
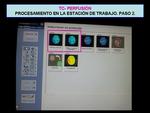
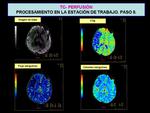
Con los datos finales obtenidos nos permite seleccionar en cada cuadrante de la pantalla varios parámetros que podemos ver representados con mapas de colores para un análisis inicial del área isquémica,
los princiales de ellos Fig. 13 :
- Tiempo de transito medio (TTM): diferencia de tiempo entre la entrada de sangre arterial y la salida venosa.
Es el parámetro más precoz y útil en los estadíos precozes.
- - Volumen sanguíneo cerebral (VSC): volumen de sangre por unidad de masa cerebral.
Parámetros normales: 4-6 ml/100g.
- - Flujo sanguíneo cerebral (FSC): volumen de flujo sanguíneo por unidad de tiempo.
Parámetros normales: 50-60 ml/min/100g.
El FSC=VSC/TTM.
- También podemos ver a la vez como localizadores los datos de serie y la imagen de base Fig. 13 .
7.
Interpretación inicial de los mapas obtenidos Fig. 17 :
Situamos en el cuadrante superior derecho las imágenes de adquisición "datos de serie",
y en el resto los mapas de TTM,
VSC y FSC.
- TTM: en nuestro programa el área azul representa la zona isquémica,
pero no podemos diferenciar el área infartada de la penumbra .
- VSC y FSC: el área infartada tendrá un flujo bajo (azul) y un volumen bajo (azul) mientras que el área de penumbra tendrá un flujo bajo (azul) y un volumen conservado.
Con la barra de herramientas localizada a la derecha podemos delinear con un ROI a mano alzada el área de interés,
crear un eje simétrico en la línea media y copiar el ROI en el hemisferio contralateral para comparar los parámetros de ambas zonas Fig. 14 .
En la barra de herramientas el icono "datos funcionales" nos muestra con datos numéricos los hallazgos resultantes de la comparación de ambas áreas en los ROIs Fig. 14 .
- "Ataque cerebral automático":
Realiza todos los pasos anteriores de forma automática sin poder modificar los parámetros Fig. 7 .
Se puede optar por esta opción en un primer momento y si el resultado final muestra fallos o no es óptimo utilizar el modo manual.
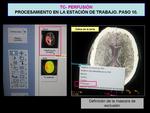
- Selección de protocolo nuevo: "Clasificación de tejidos" Fig. 15 :
1.
Definición de la máscara de exclusión: con un ROI a mano alzada dibujamos el área que queremos excluir del estudio (hemisferio contralateral,
ventrículos...) y presionando sobre él con el botón derecho del ratón lo propagamos al resto de las imágenes Fig. 15 .
Siguiente.
2.
Segmentación de la materia blanca y gris: define automáticamente la SG y la SB y nos da la opción de modificarla manualmente si no es correcta Fig. 16 .
Siguiente.
3.
Definición de los umbrales del flujo y volumen de sangre: los define de forma automática en la materia gris y blanca y nos permite modificarla manualmente Fig. 16 .
Siguiente.
4.
Interpretación de los mapas obtenidos: además de los mapas anteriores,
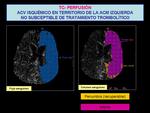
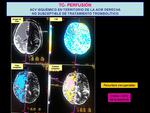
nos proporciona un mapa de volumen en el que Fig. 17 :
- el área con volumen bajo y flujo bajo que representa la zona infartada queda representada en rosa.
- el área con volumen normal y flujo bajo que representa la zona de penumbra queda representada en amarillo.
Si el área infartada supera el 20% del área isquémica está contraindicado el tratamiento trombolítico Fig. 18 y Fig. 19 .
Entre los estudios de TC-perfusión realizados en nuestro centro,
como caso infrecuente y excepcional,
se identificó una pequeña zona de isquemia talámica bilateral que en los mapas de color mostraron un 100% de penumbra Fig. 20 .
Estos hallazgos de pequeño tamaño y en localizaciones distintas al territorio de la ACM deben interpretarse con cautela,
ya que no es el objetivo del estudio ni está testado aún lo sufciente,
pudiendo llevarnos a falsas conclusiones.
El paciente finalmente no fue candidato de tratamiento trombolítico.
En el control a las 48 horas con TC sin civ aparecieron en estas localizaciones pequeñas zonas hipodensas en relación con infarto subagudo de la arteria de Percheron (variante de la normalidad que consiste en la irrigación de ambos tálamos paramediales por una única rama del segmento P1 de una de las arterias comunicantes posteriores) Fig. 21 .
4º ANGIO-TC DE TSA Y POLÍGONO DE WILLIS
Por último realizamos un angio-TC que incluye TSA y polígono de Willis desde el cayado aórtico,
introduciendo 45 cc de contraste yodado a 4,5cc/sg,
que nos permite estudiar la circulación de los ejes carotídeos,
vertebrobasilar e intracraneal,
establecer la posible causa del ictus (trombo,
disección…), su localización y el grado de enfermedad ateroesclerótica.
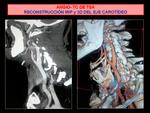
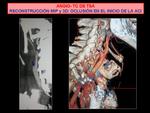
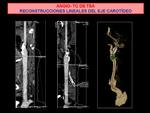
Como mapeo visual de ayuda para el clínico o radiólogos intervencionista se pueden realizar reconstrucciones MIP,
3D Fig. 22 Fig. 23 o despliegue de los vasos de interés Fig. 24 .