Tradicionalmente el estudio de extensión de diversos tumores primarios se ha practicado por TC y la RM se ha reservado para completar el estudio en hígados esteatósicos Fig.2,
o cuando es necesario caracterizar lesiones de pequeño tamaño; diferenciar quiste o hemangioma de metástasis,
Fig.3.
El TC tiene la ventaja de su mayor disponibilidad y de poder valorar simultáneamente la afectación hepática y extrahepática de la enfermedad.
La RM por contra es más útil en la caracterización de lesiones infracentimétricas y detecta un mayor número de lesiones.
Cada vez se hace más imprescindible en pacientes tributarios de tratamiento quirúrgico o cuando,
como en los adenocarcinomas de páncreas,
el hallazgo de metástasis puede desestimar la cirugía.
Fig.4.
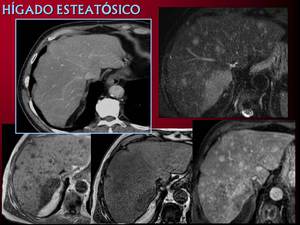
Fig. 2: Hígado esteatósico, sin evidencia de lesiones por Tc y con múltiples metástasis por RM.
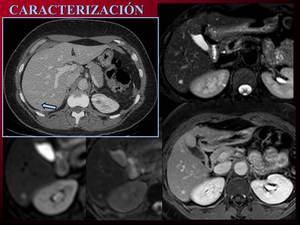
Fig. 3: Caracterización de lesiones subcentimétricas, indeterminadas por TC en estudio de extensión de paciente con tumor carcinoide ileal. Lesión sólida, hiperintensa en T2 que no restringe la difusión y capta contraste de forma progresiva.Compatible con hemangioma.
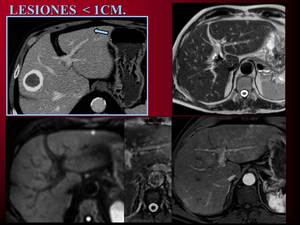
Fig. 4: Caracterización de lesiones subcentimétricas, indeterminadas por TC en estudio de extensión de paciente con neoplasia de páncreas. Lesión sólida, moderadamente hiperintensa en T2 que restringe la difusión y capta perifericamente postcontraste.Compatible con metástasis.
METÁSTASIS SIN TRATAMIENTO
ESTUDIOS SIN CONTRASTE
En los TCs sin contraste las metástasis suelen ser iso o hipodensas respecto al resto de parénquima,
salvo en casos de sangrado o calcificación intralesional en que pueden ser hiperdensas.
Podemos observar calcificaciones en metástasis de tumores mucinosos del tracto gastrointestinal o metástasis de ovario,
mama,
pulmón,
renales y de tiroides.
Por RM,
en las secuencias precontraste,
la mayoría de metástasis no tratadas son hipointensas o isointensas en secuencias potenciadas en T1. Fig.5. Se ha descrito el signo del doughnut,
borde hipointenso que rodea un centro ovoideo o irregular aún de menor señal.
En hígados esteatósicos podemos observar preservación del parénquima hepático perilesional,
en secuencias T1 fuera de fase,
hallazgo que se ha relacionado con disminución del flujo portal,
ya sea por compresión o por un mayor aporte arterial de la lesión.
Metástasis hiperintensas en T1 se observan principalmente en casos de melanoma,
por depósitos de melanina o methemoglobina extracelular.
Pueden aparecer hiperintensas lesiones con hemorragia o necrosis coagulativa (n.
de colon) o metástasis con elevado contenido proteico (adenocarcinoma ovárico,
tumor quístico mucinoso pancreático o mieloma múltiple).
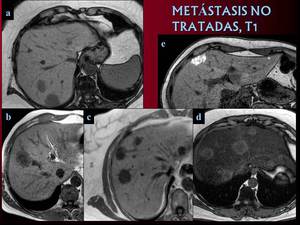
Fig. 5: Metástasis en secuencias potenciadas en T1. B.Signo del doughnut.
C. Metástasis de tumor mucinoso colorectal, muy baja señal en T1. D.Preservación del parénquima perilesional en T1 fuera de fase.
E. Metastasis hiperintensas en paciente diagnosticado de melanoma.
En secuencias potenciadas en T2 la mayoría de metástasis son hiperintensas.
Las secuencias potenciadas en T2 con supresión grasa y STIR nos facilitan la identificación de lesiones.
En un estudio de Danet,
el 72% de las lesiones eran moderadamente hiperintensas y un 20% presentaban zonas marcadamente hiperintensas debido a necrosis y degeneración quística.
Es típico el patrón en diana con centro más hiperintenso por necrosis coagulativa,
zona media hipointensa por reacción desmoplástica y periferia hiperintensa correspondiente a borde de crecimiento,
con mayor proporción de células tumorales.
Las metástasis de melanoma pueden aparecer hipointensas en T2 y STIR por depósitos de melanina y methemoglobina.
Fig.6.
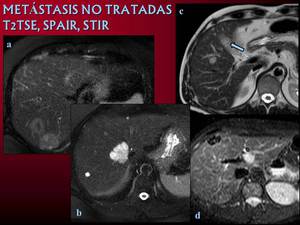
Fig. 6: Metástasis en secuencias potenciadas en T2. Fibrosis central en a. Metástasis marcadamente hiperintensas de tumor mucinoso colorectal en b.Imágenes en diana por necrosis central en c. Metástasis de melanoma hipointensas por depósito de melanina.
La mejora de las secuencias potenciadas en difusión ha aumentado la sensibilidad de la RM en la detección de metástasis hepáticas.
Fig.7.
El marcado contraste con el parénquima en secuencias con valores b 50-150 sec/mm2 nos permite advertir lesiones milimétricas que de otro modo pasarían desapercibidas.
Los valores b altos 500-800 sec/mm2 ayudan a caracterizar lesiones en el supuesto de que las lesiones malignas,
más hipercelulares y heterogeneas,
y la presencia de macromoléculas en el espacio extracelular producen una mayor restricción de la difusión.
Debemos siempre correlacionar las secuencias de difusión con los mapas de ADC (coeficiente de difusión aparente) para detectar la difusión real y eliminar el efecto de hiperintensidad en T2 y correlacionar los hallazgos con el resto de secuencias y con estudios previos.
Existen falsos positivos en caso de tumores mucinosos,
con necrosis central o degeneración quística.
Fig.. Fig.8.
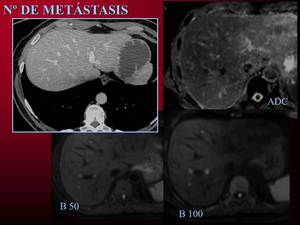
Fig. 7: Estudio de tumor carcinoide ileal. TC previo a la intervención sin claras lesiones focales. Múltiples lesiones subcentimétricas por RM que restringen la difusión y son compatibles con metástasis.
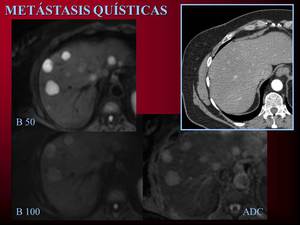
Fig. 8: Control evolutivo de paciente con antecedentes de carcinoma colorectal. Lesiones quísticas que no restringen la difusión. No existentes en el TC previo. Metástasis de tumor mucinoso colorectal.
La difusión es útil en pacientes con mala función renal,
alergia al contraste o riesgo de fibrosis sistémica nefrogénica.
Se ha utilizado para predecir la respuesta tumoral (lesiones con ADC alto peor respuesta) y valorar la respuesta al tratamiento (aumento del ADC en las lesiones que responden al tratamiento,
incluso antes de detectar cambios en su tamaño).
ESTUDIO POSTCONTRASTE
Tanto el yodo del TC como el gadolinio no organoespecífico en RM son contrastes que nos indican la perfusión y difusión en el espacio extracelular; por lo tanto el patrón de captación será similar con ambas técnicas.
Traducen el grado de captación de las lesiones respecto al resto de parénquima.
Las metástasis suelen tener el mismo comportamiento que el tumor de origen,
suelen ser hipovasculares en tumores de colon,
pulmón,
adenocarcinoma de páncreas y en tumores de vejiga y próstata.
Se observan lesiones hipervasculares en tumores primarios de tiroides,
tumores neuroendocrinos (tm.
carcinoide,
tm.
islotes pancreáticos,
feocromocitoma),
melanoma,
ca.
renal,
coriocarcinoma y sarcomas.
En casos de sospecha de metástasis en esto tumores el estudio por TC debe incluir una fase arterial.
Los patrones de captación de las metástasis de diferentes tumores primarios,
tanto hiper como hipervasculares se superponen.
El más frecuente es la captación periférica y contínua y el llenado progresivo de contraste.
En fase arterial podemos observar captación periférica y contínua (por efecto de parasitación de la lesión y reacción desmoplástica/ inflamatoria del parénquima adyacente),
metástasis homogeneamente hipercaptantes (suelen se menores de 1'5 cms.),
metástasis heterogeneas por fibrosis y necrosis central (>3cms.) o con mínima captación periférica (lesiones hipovasculares).
Fig.9.
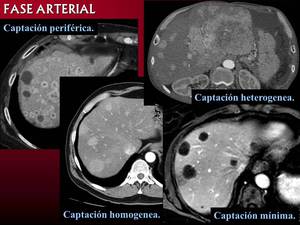
Fig. 9: Patrones de captación en fase arterial. Captación periférica y contínua en metástasis de n. de páncreas, captación homogenea en metástasis de tumor carcinoide ileal. Captación heterogenea en las metástasis de mayor tamaño de un gastrinoma. Mínima captación periférica en metástasis de tm. mucinoso colorectal.
En fase portal y retardadas el patrón más frecuente es la captación progresiva incompleta.
En menor grado,
se observan lesiones que se hacen isointensas con el resto de parénquima o persistencia de una mínima captación perférica.
Fig.10.
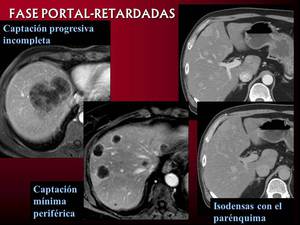
Fig. 10: Metástasis en fase portal-retardadas. Captación progresiva postadministración de contraste como patrón más frecuente.
Persistencia de mínima captación periférica en imagen central.
Metástasis que prácticamente se homogeinizan con el parénquima en imágenes derechas.
El fenómeno de washout periférico se ha descrito como hallazgo típico de metástasis,
consiste en lavado de contraste en la periferia de la lesión en fases retardadas,
es más frecuente en las metástasis hipervasculares,
especialmente en tm.
neuroendocrinos.
Supone una mejor vascularización arterial y venosa en periferia,
donde se sitúa el tumor viable,
respecto al centro de fibrosis o necrosis.
Fig.11.
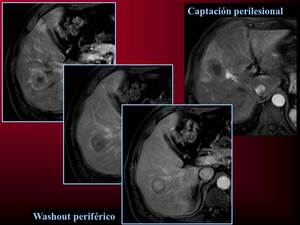
Fig. 11: Washout periférico en lesión metastásica de cáncer colorectal.
Captación perilesional en forma de cuña en otra lesión del mismo paciente.
Pueden observarse alteraciones de captación perilesional transitoria,
más evidentes en fase arterial y correlacionadas con reacción desmoplástica,
reacción inflamatoria y proliferación vascular.
Pueden presentar morfología de cuña o circumferencial y son más frecuntes en las lesiones hipovasculares; colon y páncreas.
Fase hepatocitaria.
Se han reportado muy buenos resultados con los quelatos de gadolinio de eliminación hepática y en la literatura compiten con la difusión en la detección de un mayor número de metástasis hepáticas pero,
debido al precio y al aumento de tiempo de exploración,
en nuestra institución no se utilizan de forma rutinaria.
En fase excretora el sistema reticuloendotelial de las células hepáticas normales elimina contraste mientras que las metástasis destacan por su hipointensidad respecto al resto de parénquima.
Fig.12.
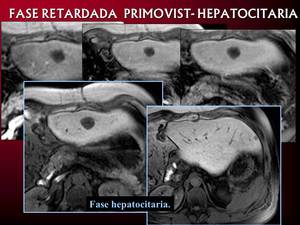
Fig. 12: Metástasis con contraste de eliminación biliar.
Estudio dinámico normal en las tres imágenes superiores.
Fase hepatocitaria en las dos inferiores, lesiones hipointensas respecto al resto de parénquima.
CAMBIOS POSTRATAMIENTO
AFECTACIÓN DIFUSA
La toxicidad hepática postquimioterapia comprende desde meras alteraciones analíticas por hepatitis química,
reactivación de hepatitis B e hígado graso,
a fibrosis,
hipertensión portal y cirrosis.
Pueden ocurrir en cualquier paciente tratado con quimioterapia citotóxica convencional y veces es difícil determinar el agente causante debido a la combinación de fármacos.
Es frecuente en el tratamiento neoadjuvante de pacientes con ca.
colorectal o en tratamientos largos con Irinotecan (presente en el Folfiri),
fluoropirimidinas (5-Fu,
capacitabina) o oxiloplatino (Folfox,
Xelox).
Puede afectar a la capacidad de regeneración y llegar a limitar las resecciones hepáticas,
dado el riesgo de insuficiencia posttratamiento.
Fig.13.
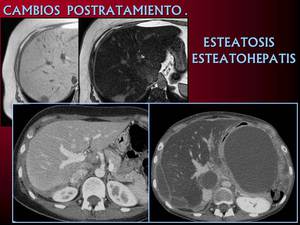
Fig. 13: Esteatosis difusa en paciente con tratamiento neoadjuvante por metástasis de carcinoma colorectal, marcada pérdida de señal en secuencias potenciadas en T1 fuera de fase.
TC de estadificación en paciente diagnosticada de neoplasia de ovario diseminada. Marcados signos de esteatosis en el Tc de control postquioterapia con Taxol y Carboplatino.
Las nuevas terapias moleculares,
pueden producir toxicidad hepática aunque es menos frecuente.
Se ha descrito en los inhibidores de los receptores de factores de crecimiento epidérmico de la tirosinasa EGFR,
Erlotinib (Tarceva,
n.
de pulmón),
en inmunomoduladores como el Ipilimubab (melanoma),
en KIT inbibidores como el Imatinib,
en los inhibidores del factor de crecimiento del endotelio vascular (VEGF) y de su receptor VEGFR,
el Bevazucimab y Pazopanib.
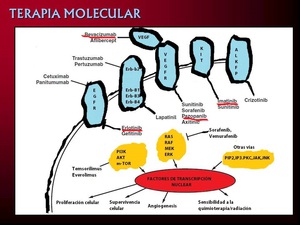
Fig. 14: Terapia molecular. Lugares de actuación de los distinto fármacos en la membrana y a nivel intracelular. Subrayados los agentes que se han descrito como más citotóxicos.
Normalmente producen alteraciones analíticas que suelen resolverse al dejar el tratamiento.
Por imagen se observa disminución de la atenuación,
engrosamiento de la pared vesicular,
ascitis y disminución de la atenuación periportal.
Se han descrito casos raros de necrosis hepática con Imatinib.
Los cambios de esteatosis hepática suelen ser difusos pero pueden observarse casos de afectación focal,
heterogenea o incluso multinodular que por TC sugieren infiltración tumoral o metástasis pero en RM muestran clara pérdida de señal en secuencias fuera de fase.
Fig.
15.
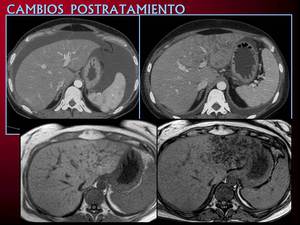
Fig. 15: TC de estadificación en paciente con neoplasia de ovario y carcinomatosis en debut. En el TC de control postquimioterapia se observa una alteración de densidad difusa en lóbulo izquierdo que sugiere infiltración tumoral. Dada la disociación con la marcada respuesta en el resto de lesiones se practica una RM que descubre una zona de infiltración grasa focal.
Pseudocirrosis. Tanto en pacientes portadores de metástasis como en hígados previamente sanos se han descrito cambios postquimioterapia similares a la cirrosis.
Se observa lobulación de contornos por retracción de la cápsula hepática,
pérdida de volumen,
parénquima regenerativo entre zonas cicatriciales y puede asociarse a signos de hipertensión portal.
Su evolución es rápida,
en 1-3 m.
postratamiento.
Es más frecuente en las metástasis del cáncer de mama y no está ligada a su evolución,
se ha observado tanto en lesiones que remiten como en las que progresan.
Fig 16.
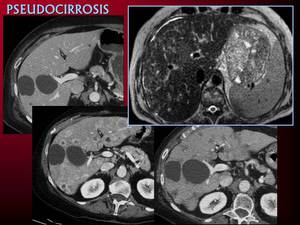
Fig. 16: Pseudocirrosis postratamiento. Imagen superior de la derecha. RM con cambios postratamiento en paciente tratada con terapia convencional para n. de mama.
Las otras tres imágenes muestran la evolución de un hígado normal a pseudocirrosis en una paciente portadora de n. mama lobulillar y recidiva tratada con Taxol y Bevazucimab.
Se han descrito casos de esclerosis biliar postquimioterapia en pacientes tratados con infusión arterial de Fluxoridina que condicionan estenosis segmentarias similares a la colangitis esclerosante con mayor afectación de hepático común y bifurcación primaria.
No es un tratamiento muy extendido por lo que es difícil observar sus complicaciones en la práctica habitual.
Enfermedad hepática veno-oclusiva en pacientes con quimioterapia mieloablativa previo al alotransplante de médula ósea.
Obstrucción de pequeñas venas y sinusoides hepáticos 3 semanas del transplante.
Por TC hepatoesplenomegalia,
ascitis,
engrosamiento de pared vesicular,
edema periportal y disminución de diámetro de la suprahepática derecha,
menos de 4 mms.
Podemos ver una afectación similar en pacientes de cáncer colorectal tratados con oxiloplatino.
Hiperplasia nodular regenerativa postquimioterapia.
Es debida al aumento de la resistencia al flujo en el sinusoide hepático (HTP),
disminución del aporte portal o del drenaje venoso por las suprahepáticas.
Por RM se obbservan nódulos de 0'1 a 4 cms.
hipo,
hiper o isointensos en T1,
hipointensos en T2,
isointensos e difusión.
Tras administración de contraste tanto por RM como por TC,
se observan múltiples nódulos de tamaño similar,
hipercaptantes en fase arterial e isointensos con el resto de parénquima en fase portal y retardadas.
Fig.
17.
Pueden aparecer hiper o isointensos en fases retardadas con contrastes hepatoespecíficos.
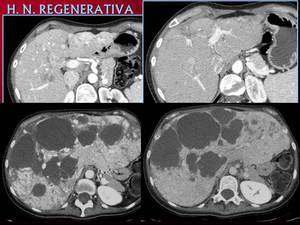
Fig. 17: Hiperplasia nodular regenerativa. Nódulos de regeneración postratamiento que pueden captar en fase arterial y se homogeinizan con el resto de parénquima en fases retardadas.
CAMBIOS EN LESIONES METASTÁSICAS
Las metástasis tratadas presentan disminución de la atenuación por TC debido a la disminución de la celularidad por necrosis y cambios mucinosos.
Son más hiperintensas en secuencias potenciadas en T2 y en casos de necrosis coagulativa muestran un aspecto más quístico.
Pueden presentar cambios fibróticos,
que a veces se asocian a retracción de la cápsula hepática y calcificar.
Tras administración de contraste suelen mostrar captación periférica y continua,
más evidente en fase arterial.
Fig.19.
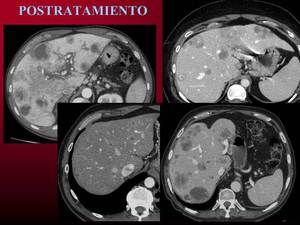
Fig. 18: Cambios postratamiento. Edema periportal y múltiples lesiones irregulares y con necrosis central. Calcificaciones postratamiento. Irregularidad de márgenes,retracción de cápsula hepática.
Metástasis que captan como hemangiomas.
Lesiones focales que en exploraciones previas presentan características típicas de metástasis pueden similar hemangiomas postratamiento.
Aparecen hiperintensas en T2 ,
con captación globular y discontínua y replección progresiva de contraste.
Dichos cambios se cree que son debidos al efecto antiangiogénico de la quimioterapia; captación globular debido a irregularidades en la vascularización y mayor captación retardada debido a alteraciones de drenaje.
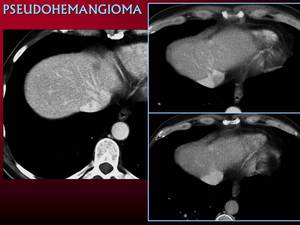
Fig. 19: Metástasis hipodensa en el TC de estadificación, imagen de la izquierda. Postadministración de contraste muestra una captación similar a un hemangioma.
VALORACIÓN DE RESPUESTA
Los tratamientos quimioterápicos convencionales se basan en el efecto citotóxico sobre la lesión.
Medimos el tamaño como forma de valorar la respuesta y los criterios más utilizados son los del RECIST1.1 (Response Evaluation Criteria In Solid Tumors).
Se valoran lesiones mayores de 10 mms,
un máximo de 2 lesiones por órgano y 5 por paciente,
midiendo su diámetro mayor.
Se considera respuesta completa cuando desaparecen todas las lesiones y las adenopatías patológicas.
Respuesta parcial cuando hay una respuesta mayor o igual al 30% de la suma del diámetro mayor de las lesiones diana.
Enfermedad estable cuando no hay cambios significativos.
Progresión de la enfermedad cuando aumenta un 20% la suma de los diámetros y debe superar al menos los 5 mms.
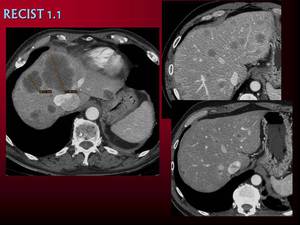
Fig. 20: RECIST 1.1. Medida del diámetro mayor de dos lesiones diana. Respuesta parcial en paciente con metástasis de n. de pulmón.
Los nuevos tratamientos moleculares suelen tener un efecto citostático por lo que la medida del tamaño puede subestimar la respuesta al tratamiento.
Cada vez más se buscan marcadores funcionales que valoran la respuesta al tratamiento dependiendo del tipo de tumor y del tratamiento utilizado.
Así los criterios de Choi sirven para valorar la respuesta de los GIST al Imatinib.
En ellos la respuesta parcial se consigue al disminuir el diámetro mayor en proporción igual o mayor al 10 % y la atenuación mayor o igual al 15%,
no aparecen nuevas lesiones ni aumentan las no medibles. Progresión de la enfermedad cuando el diámetro mayor aumenta un 10%,
aparecen lesiones nodulares intralesionales,
aumentan las ya existentes o aparecen nuevas lesiones.
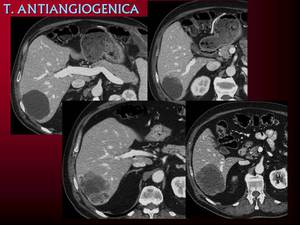
Fig. 21: Paciente afecto de metástasis de GIST. Primera imagen TC con respuesta al tratamiento. Progresiva recidiva con aumento del componente sólido y formación de nódulos dentro del quiste. Paciente con varias recidivas y ya tratado con Imatinib, Dovitinib y última remisión con Regofinib.
El Bevacizumab,
uno de los anticuerpos monoclonales más utilizados,
puede producir cambios morfológicos que se han relacionado con una buena respuesta patológica pero no se correlacionan con disminución del tamaño.
Se considera respuesta óptima las lesiones presentan un aspecto pseudoquístico,
son homogeneas,
de muy baja densidad con márgenes lisos y bien delimitados y sin captación periférica.
En la respuesta parcial la atenuación es mixta,
márgenes variables y puede haber discreta captación.
En la ausencia de respuesta la densidad es heterogenea,
la interfase lesión/hígado mal definida y persiste captación periférica.
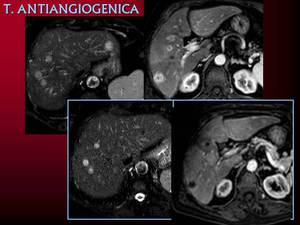
Fig. 22: Metástasis de tumor de células renales. Disminución de la vascularización y aspecto pseuquístico postratamiento con Sunitinib.
Metástasis con respuesta atípica al tratamiento,
pseudoprogresión. A veces lo que observamos no corresponde a una progresión real de la enfermedad sino a lesiones ya existentes pero isodensas con el parénquima que se hacen más evidentes con la terapia antiangiogénica.
Podemos observar disminución de densidad con aumento de tamaño de las lesiones pero que en realidad es por hacerse más evidente un cápsula periférica ya existente.
Aumento de tamaño con aumento de densidad de las lesiones debido a que la alteración de la vascularización produce hemorragia intralesional,
hiperdensa en los TCs sin contraste o con nivel líquido líquido. Hemorragias recurrentes que producen cambios temporales en el tamaño de las lesiones.
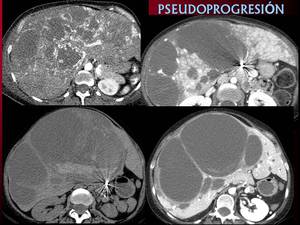
Fig. 23: En la primera imagen TC de diagnóstico de paciente con metástasis de coriocarcinoma. La imagen superior de la derecha corresponde al primer control con terapia antiangiogénica. Las dos inferiores pertenece a un tercer control en el que se observan signos de sangrado intralesional y aumento de tamaño de las lesiones, sin embargo su captación ha disminuido. La historia clínica de la paciente refiere la existencia de un control externo que informa de respuesta parcial con marcada disminución de tamaño de las lesiones.
Criterios de respuesta a la terapia inmunomoduladora se considera respuesta parcial una disminución igual o mayor al 50% de la carga tumoral y progresión de la enfermedad,
aumento mayor o igual al 50% de la carga tumoral.
El fármaco tipo es el Ipilimumab en melanomas.























