INTRODUCCIÓN:
Las masas retroperitoneales primarias (que surgen en el retroperitoneo pero no de los órganos retroperitoneales principales) son un grupo poco frecuente pero diverso de tumores benignos y malignos y lesiones no tumorales.
De éstas,
el 70-80% son malignas,
constituyendo únicamente el 0.1%- 0.2% de todos los tumores malignos del cuerpo.
Dar la localización precisa,
determinar la extensión de la invasión y caracterizar el tipo patológico son algunos de los desafíos a los que nos enfrentamos.
Pueden dividirse en masas sólidas o quísticas y a su vez en masas neoplásicas o no neoplásicas.
Esta presentación tratará principalmente las masas sólidas.
REVISIÓN ANATÓMICA:
El retroperitoneo es el espacio comprendido entre el peritoneo parietal por delante y la fascia transversalis por detrás que se extiende desde el diafragma hasta la pelvis.
Está generalmente dividido por fascias en los espacios pararrrenal anterior y posterior,
perirrenal y el de los grandes vasos.
Fig. 1
Espacio pararrenal anterior:
Limitado anteriormente por el peritoneo parietal posterior,
posteriormente por la fascia renal anterior o fascia de Gerota y lateralmente por la fascia lateroconal.
Se subdivide en el espacio pancreáticoduodenal,
que contiene el páncreas y el duodeno y el espacio pericolónico,
que contiene el colon ascendente y descendente.
Espacio pararrenal posterior:
Limitado por la fascia renal posterior por delante o fascia de Zuckerkandl,
la fascia transversales por detrás y por el músculo psoas medialmente.
Se continúa lateralmente por fuera de la fascia lateroconal como la grasa properitoneal de la pared abdominal.
Superiormente se continúa como una capa fina de grasa extraperitoneal subdiafragmática.
Por debajo del nivel de los riñones,
los espacios pararrenal anterior y posterior se unen para formar el espacio retroperitoneal infrarrenal,
que comunica inferiormente con el espacio prevesical y los compartimenos extraperitoneales de la pelvis.
Espacio perirrenal:
Limitado por la fascia de Gerota y la fascia de Zuckerkandl que juntas constituyen la fascia renal.
Contiene los riñones,
vasos renales,
glándulas suprarrenles,
pelvis renales,
uréteres proximales,
linfáticos y grasa perirrenal.
Espacio de grandes vasos:
Es la región grasa que rodea la aorta,
la vena cava inferior y que apoya en los cuerpos vertebrales y los músculos psoas.
La anatomía compartimental tradicional no explica completamente la diseminación de colecciones líquidas o tumores del retroperitoneo.
Ahora se postula que las fascias perirrenles son estructuras multilaminadas con potenciales planos interfasciales expandibles como el retromesentérico,
retrorrenal,
lateroconal y interfascial combinado.
El conocimiento de esta anatomía y sus interconexiones puede ayudar a entender las vías de extensión y diseminación de los procesos retroperitoneales
En TC y RM,
los planos fasciales retroperitoneales se detectan cuando hay grasa retroperitoneal abundante.
Una fascia que mide más de 3 mm se considera engrosada y es un signo sensible pero no específico de procesos patológicos retroperitoneales.
LOCALIZACIÓN RETROPERITONEAL:
El primer paso es determinar si el tumor está localizado en el espacio retroperitoneal e identificar si es así el órgano de origen.
Para ello hay una serie de signos descritos:
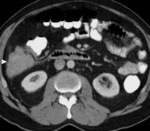
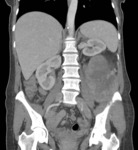
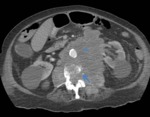
- Desplazamiento anterior de los vasos principales retroperitoneales y los órganos retroperitoneales (riñones,
suprarrenales,
colon ascendente y descendente,
páncreas y porciones del duodeno.
Fig. 2 Fig. 3
- Identificación del órgano de origen.
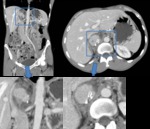
- Positive Beak Sign (signo del pico positivo).
Deformidad de los márgenes del órgano adyacente en forma de pico indica que se trata del órgano de origen.
Fig. 4
- Embedded Organ Sign (signo del órgano embebeido). Cuando se trata del órgano de origen,
se observa un conctacto íntimo entre la masa y el órgano de origen,
normalmente con una reacción desmoplásica y posibles ulceraciones (+). Al contrario,
un órgano moldeable,
comprimido por una masa,
se deforma en forma crescente (-). Fig. 5
- Phantom Organ Sign (signo del órgano fantasma).
Cuando un órgano no se ve,
se trata probablemente del origen de la masa Fig. 6
- Prominent Feeding Artery Sign.
Se puede llegar a identificar una arteria de irrigación al tumor de mayor calibre.
- La ausencia de signos determinantes que sugieran el órgano de origen indica el diagnóstico probable de masa retroperitoneal primaria.
Los bordes redondeados en vez de en pico (negative beak sign),
con una deformidad crescente de un órgano adyacente al tumor (negative embedded sign) sugiere por tanto tumor retroperitoneal primario.
MASAS RETROPERITONEALES PRIMARIAS.
Las masas retroperitoneales primarias,
pueden dividirse en masas sólidas o quísticas y a su vez en masas neoplásicas o no neoplásicas.
MASAS SÓLIDAS
1.
NEOPLÁSICAS
Las neoplasias sólidas primarias retroperitoneales pueden dividirse en 4 grupos importantes: neoplasias mesodérmicas,
tumores neurogénicos,
tumores de células germinales,
del cordón y estromales y neoplasias linfoides.
Fig. 7
1.1. ORIGEN MESODÉRMICO
Neoplasias poco frecuentes,
siendo menos del 1% (0.1-0.2%) de las neoplasias malignas de los adultos.
El 15% de ellos,
se originan en retroperitoneo.
La mayoría de neoplasias retroperitoneales son de origen mesodérmico,
constituyendo los liposarcomas,
leiomiosarcomas e histiocitomas fibroso maligno más del 80% de ellos.
Típicamente se presentan en la sexta o séptima década de la vida y son normalmente de gran tamaño en su presentación
Las técnicas de imagen presentan un papel importante en la determinación de la extensión y el diagnóstico diferencial.
Se necesita una muestra histológica para establecer el diagnóstico definitivo y su estadiaje
El tratamiento de elección es la resección quirúrgica completa del tumor inicial y de las posibles recidivas,
siendo este el factor pronóstico más importante que determina la supervivencia.
1.1.1.
LIPOSARCOMA
Constituyen el 40% de los sarcomas retroperitoneales,
siendo el tipo más común
Se originan de las células mesenquimales primitivas y no de los adipocitos.
Resulta difícil el diagnostic diferencial entre liposarcoma recurrente y la propia grasa retroperitoneal presentando el primeo una mayor hiperatenuación.
En alguna occasion pueden tender una apariencia distinta a la del tumor primario,
sin contener grasa visible.
La organización mundial de la salud (OMS) los clasifica en 5 subtipos:
- Bien diferenciado: Más común.
Presenta una apariencia en atenuación y señal similar a la grasa macroscópica.
Ausencia o escasa captación de contraste intravenoso,
con presencia de componentes de fibrosis o esclerosis.
Bajo potencial metastásico y alta recurrencia.
DD con lipoma Fig. 8
- Mixoide: 2º subtipo más frecuente.
Se suele manifestar en población más joven.
Presenta normalmente un aspecto pseudoquístico por una distribución homogénea entre grasa y tejidos blandos.
Realce progresivo tras la administración de contraste intravenoso.
- Desdiferenciado: Contiene un component graso bien diferenciado y un componante no graso.
En un 30% de los casos puede aparecer calcificaciones u osificaciones.
Fig. 9 Fig. 10
- Células redondas y pleomórico: Subtipos menos comunes.
Lesiones heterogéneas y agresivas con poco o ningún contenido de grasa macroscópica.
Fig. 11
1.1.2.
LEIOMIOSARCOMA
Segundo sarcoma retroperitoneal primario más común,
representando un 30%,
tratándose de la neoplasia venosa intraluminal y de vena cava inferior más frecuente.
Se manifiesta en la quinta y sexta década de la vida,
siendo más frecuente en la mujer(66%)
Extravascular (62%),
intravascular (5%,
intra y extravascular (33%).
Masas de tejidos blandos bien delimitados.
Cuando son de gran tamaño,
pueden presentar áreas de necrosis y hemorragia.
Señal baja o intermedia en las secuencias potenciadas en T1 e intermedia o alta en las potenciadas en T2.
Realce de contraste heterogéneo en fases precoces que persiste en fases tardías. Fig. 12
La clínica inicial depende del segmento afectado :
- Segmento superior (Vena cava inferior intrahepática) àSíndrome de Budd-Chiari.
- Segmento medio (Desde la VCI intrahepática hasta las venas renales) à dolo en hipocondrio derecho e insuficiencia renal
- Segmento inferior (por debajo de las venas renales) à dolor y edema de las extremidades inferiores.
1.1.3.
HISTIOCITOMA FIBROSO MALIGNO
El tercer sarcoma retroperitoneal más común (15-19%),
representando el sarcoma de partes blandas más común en el cuerpo.
Se manifiesta en la quinta y sexta década de la vida,
siendo más frecuente en el hombre (66%).
Hallazgos no específicos de imagen.
Fig. 13
Se trata de grandes masas de partes blandas infiltrantes con captación heterogénea del contraste presentando áres de necrosis y hemorragia en su interior.
Calcificaciones en el 7-20% de los casos.
RM: señal baja o intermedia en secuencias potenciadas en T1 y heterogéneamente alta en secuencias potenciadas en T2.
1.1.4.
SARCOMAS MENOS COMUNES.
1.1.4.1.
RABDOMIOSARCOMA
Tiene una distribución bimodal: a los 7 años y en la adolescencia.
El 7% de ellos se da en el retroperitoneo.
Son masas con calcificaciones necrosis y calcificaciones,
con un realce heterogéneo tras la administración de contraste.
Metástasis en un 10-20%.
1.1.4.2.
ANGIOSARCOMA:
Tumor maligno del endotelio y células mesenquimales.
La localización más frecuente es la aurícula derecha,
y mucho menos frecuente la vena cava inferior (retroperitoneo).
Se trata de masas hipercaptantes que ensanchan el vaso del que se originan.
1.1.4.3.
SARCOMA DE CÉLULAS SINOVIALES
Normalmente localizado alrededor de las articulaciones (85-95%) siendo mucho menos frecuente en el retroperitoneo.
Pronóstico incierto.
Los hallazgos de imagen no son especefícos pero debe considerarse en el diagnóstico cuando un paciente joven (15-40 años) se presenta con una masa retroperitoneal.
1.1.4.4.
CONDROSARCOMA.
Tumor maligno que produce matriz cartilaginosa.
Los condrosarcomas extraesqueléticos representan el 2% de todos los sarcomas de partes blandas.
El TC muestra una masa grande de partes blandas con un anillo condroide o calcificaciones de tipo arciforme.
También pueden verse calcificaciones puntiformes amorfas en el tipo mixoide.
Presentan un realce heterogéneo y prominente Fig. 14
1.1.5.
OTROS TUMORES MESENQUIMALES MENOS FRECUENTES.
1.1.5.1. PECOMAS
Los tumores de células epitelioides perivasculares (Perivascular Epithelioid Cell tumors (PEComas)) son tumores mesenquimales benignos con potencial maligno variante. Las células expresan marcadores melanocíticos (melanin-A,
factor de transcripción de la microftalmia) y marcadores de músculo liso (HMB-45,
actina).
Hay muchos tumores incluídos en este grupo entre los que se presentan: angiomiolipomas,
linfangioleiomiomatosis,
sarcoma de células perivasculares y tumores miomelanocíticos de células claras entre otros.
1.1.5.2. TUMOR DESMOIDE
También conocido como fibromatosis profunda,
fibromatosis agresiva o fibrosarcoma bien diferenciado.
Son poco frecuentes,
menos del 1% de todos los tumores retroperitoneales.
Puede ser esporádico o asociado a síndromes familiares como el síndrome de Gardner o poliposis coli.
Son estrógeno dependientes,
siendo más frecuente en las mujeres desde la pubertad hasta los 40 años.
En imagen,
dependen de la composición del tejido (células fusiformes,
colágeno y matriz mixoide) y de la vascularización.
En general,
se observa una masa mal o bien diferenciada con alta atenuación en TC y en RM,
lesiones celulares en fase precoz se observan con hiperseñal en secuencias potenciadas en T2 que con la pérdida de celularidad y depósito de colágeno se presentan con hiposeñal T2.
Realce moderado-marcado tras la administración de contraste. Fig. 15
1.2. ORIGEN NEUROGÉNICO
Representan el 10-20% de todos los tumors retroperitoneales primarios.
Se presentan en un grupo de edad menor y frecuentemente son benignos con major pronóstico. Normalmente localizados a lo largo de la cadena simpática,
en la región paraespinal; en la médula suprarrenal o en los órganos de Zukerkandlo cuerpos paraaórticos.
(paraaortic bodies).
Se clasifican según su origen en: vaina nerviosa,
células gangliónicas y paragangliónicas
1.2.1.
TUMORES DE LA VAINA NERVIOSA:
1.2.1.1.
SCHWANOMA/NEURILEMOMA
Se presentan en mujeres de 20-50 años.
Constituyen el 6% de las neoplasias retroperitoneales primarias.
Se presentan como masas capsuladas y bien delimitadas,
que presentan una atenuación e intensidad de señal heterogénea.
Compuestas por componente de Antoni A celular (hiposeñal en T1 y T2) y Antoni B mixoide.
Presenta una posición excéntrica en relación con el nervio de origen,
por lo que la cirugía conservadora es posible.
Puede observarse degeneración quística/hemorrágica,
calcificaciones e hialinización.
1.2.1.2.
NEUROFIBROMA
Se presentan en varones de 20-40años,
normalmente,
hasta en un 90%,
como tumores aislados.
Ante la presencia de neurofibromas múltiples o neurofibromas plexiformes,
nos encontramos ante un caso de Neurofibromatosis tipo 1 (NF1).
Se trata de masas homogéneas bien delimitadas,
no encapsuladas,
compuestos por células de la vaina nerviosa,
componente mixoide y haces de colágeno.
Presenta una posición central y en continuidad con el nervio de origen por lo que la resección quirúrgica conlleva la escisión del nervio.
Fig. 16 Pueden degenerar a tumores malignos de la vaina nerviosa (MNST).
1.2.1.3.
TUMORES MALIGNOS DE LA VAINA NERVIOSA (MNST)
Incluyen: Schwanoma maligno,
sarcoma neurogénico y neurofibrosarcoma. Representan el 5-10% de los sarcomas de partes blandas.
Se presentan en pacientes de 20 a 50 años.
El 50% se originan de novo y el resto se derivan de neurofibromas o tras radiación.
Alrededor del 2% al 5% de los pacientes con NF1 desarrollan MNST.
Se trata de masas grandes y heterogéneas con necrosis o calcificación central con márgenes pobremente diferenciados.
El hallazgo más importante a tener en cuenta es el crecimiento rápido de una masa asociado a dolor espontáneo y no remitente.
El tratamiento de elección es la resección quirúrgica completa.
1.2.3.
ORIGEN EN CÉLULAS GANGLIÓNICAS:
1.2.3.1.
GANGLIONEUROMA
Tumor benigno poco frecuente que se presenta en la segunda a cuarta década de la vida.
Tiene origen en los ganglios simpáticos.
Normalmente asintomático.
El 57% son funcionales,
con secreción de catecolaminas,
péptidos intestinales vasoactivos u hormonas androgénicas.
Se trata de masas de baja atenuación bien delimitadas,
con un posible aspecto en espiral,
que pueden rodear un vaso sanguíneo sin estenosarlo.
Calcificaciones puntiformes se ven en un 20-30%.
1.2.3.2.
GANGLIONEUROBLASTOMA
Tumor pediátrico de grado intermedio.
(2-4 años)
1.2.3.3.
NEUROBLASTOMA
Tumor pediátrico maligno,
más frecuente en varones en la primera década de la vida.
El 66% están localizados en la glándula suprarrenal,
y el resto a lo largo de la cada simpática paravertebral.
Se presentan normalmente como masas infiltrantes,
irregulares,
lobuladas y heterogéneas,
englobando vasos sanguíneos y con calcificaciones groseras.
Realce variable tras la administración de contraste.
1.2.4.
CÉLULAS PARAGANGLIÓNICAS:
1.2.4.1.
PARAGANGLIOMA:
Feocromocitoma extraadrenal.
Localizado en los órganos de Zuckerkand,
en la región paraaórtica próximo al origen de la arteria mesentérica superior. Hasta el 40% son malignos,
con un comportamiento agresivo local y/o metástasis a ganglios,
hueso,
pulmón o hígado.
Pueden ser funcionales hasta en un 60% de los pacientes,
produciendo síntomas causados por la secreción de catecolaminas.
Se muestran como masas de partes blandas bien delimitadas con necrosis (40%),
calcificaciones puntiformes (15%) o hemorragia intratumoral.
En la RM presentan señal intermedia en las secuencias potenciadas en T1 y moderadamente alta en las potenciadas en T2.
Tumores hipervasculares con realce precoz e intenso.
1.3.
TUMORES DE CÉLULAS GERMINALES,
DEL CORDÓN Y ESTROMALES.
1.3.1.
TUMORES DE LAS CÉLULAS GERMINALES RETROPERITONEALES PRIMARIOS (GCTs).
Sólo el 1%-2.5% se origina en una localización extragonadalsiendo el mediastino más frecuente que el retroperitoneo.
Se piensa que se forman a partir de los remanentes de las células germinales (línea media de T6 a L2).
Se puede tratar de tumores seminomatosos o no seminomatosos (Fig diapositiva)
La mayoría se trata de metástasis de un primario gonadal por lo que debe de excluirse una neoplasia testicular coexistente.
1.3.2.
TERATOMA RETROPERITONEAL PRIMARIO.
Tumores poco frecuentes,
constituyendo un 6%-11% de los tumores retroperitoneales primarios.
Se originan de las células germinales pluripotenciales.
Son más frecuentes en las mujeres con una distribución bimodal,
con una presentación en menores de 6 meses y en los adultos jóvenes.
Es el tercer tumor retroperitoneal más frecuente en niños después del neuroblastoma y el tumor de Wilms.
Se subclasifican en:
1.3.2.1.
TERATOMA MADURO (QUISTE DERMOIDE):
Se presenta como una masa predominantemente quística con calcificación en forma de diente (56%) y grasa (93%).
Puede observarse un nivel grasa líquido y artefacto químico entre la grasa y el fluido.
En un 81% de casos se puede ver la protuberancia de Rokitansky (component sólido villiforme)
1.3.2.2.
TERATOMA INMADURO.
Poco frecuente (<1%).
Se presenta en menores de 20 años siendo las proximidades del polo superior del riñón izquierdo,
su localización más frecuente.
Son masas predominantemente sólidas con áreas grasas dispersas y calcificaciones groseras y mal delimitadas dispersas.
1.3.2.3.
TERATOMA MALIGNO
Masa irregular e infiltrante a los órganos y vasculatura adyacente.
Presentan elevación de la α-fetoproteina (AFP) en un 50% de casos.
1.4. ORIGEN LINFOIDE
1.4.1.
LINFOMA:
Se trata del tumor maligno retroperitoneal más frecuente (33%).
Hay dos tipos:
- Linfoma de Hodking (LH): con una distribución bimodal,
con un pico en la segunda y sexta década de la vida.
Puede darse enfermedad limitada al mediastino y bazo.
- Linfoma no Hodking (LnH): Edad de presentación en la cuarta a séptima década de la vida.
Puede existir enfermedad extranodal en el hígado,
bazo o intestinos,
sobre todo en estadíos avanzados de la enfermedad.
Los ganglios paraaóriticos están afectados en un 25% y 55% en cada grupo respectivamente.
El 14% de los LnH se presentan como una masa retroperitoneal.
En TC se trata de masas homogéneas bien delimitadas,
con realce leve y homogéneo que crecen entre las estructuras retroperitoneales sin comprimirlas o estenosarlas.
La aorta y vena cava inferior pueden estar desplazadas anteriormente,
produciendo el signo denominado “aorta flotante”.
Necrosis y calcificaciones son poco frecuentes,
al menos antes del tratamiento.
En RM,
presentan una señal isointensa en las secuencias potenciadas en T1 e iso o hiperintensas en las potenciadas en T2.
Se observa un realce homogéneo o parcheado tras la administración de contraste intravenoso Fig. 17
El tratamiento consiste en quimio y radioterapia.
La diferenciación entre tumor viable y fibrosis no es fácil,
una hiposeñal en T2 con mínimo realce es sugestivo de fibrosis.
En el PET,
se diferencian por una captación alta de 18FDG por parte del tumor.
1.4.2.
LINFADENOPATÍAS:
1.4.2.1.
ADENOPATÍAS METASTÁSICAS:
Las neplasias malignas tienden a extenderse inicialmente a las adenopatías locoregionales.
Los carcinomas que normalmente metastatizan a retroperitoneo son el carcinoma renal,
testicular,
de cérvix uterino y prostáticos.
Los criterios de para diferenciar entre adenopatías metastásicas o reactivas se basan en tamaño,
morfología,
etc. Fig. 18 Fig. 19 Fig. 20
El más utilizado es el tamaño,
específicamente en el diámetro corto,
siendo las medidas límites en adenopatías retrocrurales de 6 mm,
en retroperitoneales de 10 mm y en pelvis de 15 mm.
Debemos sospechar de un proceso patológico subyacente ante la presencia de múltiples adenopatías en el límite alto de la normalidad.
1.4.2.2.
ENFERMEDAD DE CASTLEMAN LOCALIZADA.
También conocida como hyperplasia linfoide angiofolicular o hyperplasia linfoide gigante.
Se trata de una condición linfoproliferativa idiopática no clonal poco frecuente.
Su localización más frecuente es en el tórax,
apareciendo en el retroperitoneo en tan solo un 10%–15% de los casos.
Se presentan como masa de partes blandas única,
homogénea y bien delimitada con moderado o marcado realce tras la administración de contraste,
pudiendo presentar un anillo periférico con mayor realce.
Pueden aparecer fibrosis central o calcificaciones en un 30% de los casos.
Fig. 21
2.
NO NEOPLÁSICAS
2.1. LIPOMATOSIS PSEUDOTUMORAL
Más frecuente en varones,
con edad media de 48 años.
Crecimiento metaplásico benigno de material grasa.
Puede presentarse de forma asintomática,
con dolor hipogástrico o síntomas gastrointestinales.
Comúnmente aparece en la región pélvica (región perirrectal y perivesicular).
Se produce un exceso de grasa con efecto masa sobre estructuras vecinas sin captación de contraste ni masa de partes blandas.
2.2. HEMATOPOYESIS EXTRAMEDULAR
Depósitos anormales de tejido hematopoyético fuera de la médula ósea (hígado,
bazo y en ganglios linfáticos.
Se puede obsevar en hemoglobinopatías,
mielofibrosis,
linfoma,
leucemia y carcinoma. En TC se objetiva en región paravertebral masas lobuladas o redondeadas con isoatenuación,
con o sin grasa macroscópica.
2.3. FIBROSIS RETROPERITONEAL
Más frecuente en varones,
con edad media 40- 60 años.
Se trata de una enfermedad de tejido colágeno y vascular de causa desconoocida pudiendo asemejarse a un tumor retroperitoneal. Típicamente de origen idiopático (>70% de los casos),
possible origen autoimmune.
Puede ser secundario a drogas,
procesos malignos,
inflamatorios,
hemorragias,
tras radioterapia o quimioterapia.
Puede estar asociado con otras enfermedades fibrosantes mediadas por IgG4,
como la colangitis esclerosante,
tiroidis de Riedel,
pseudotumor orbitario y pancreatitis autoinmune entre otras.
En TC se muestran como masas de tejidos blandos formando placas irregulares que rodean la aorta abdominal infrarrenal y las arterias ilíacas comunes,
produciendo una retracción ureteral con consecuente ureterohidronefrosis. Fig. 22
El tratamiento consiste en corticoides,
inmunoterapia,
fármacos modificadores de la enfermedad reumática,
tamoxifeno o cirugía.
2.4. PSEUDOTUMOR INFLAMATORIO
También conocido como tumor miofibroblástico inflamatorio,
granuloma de células plasmáticas,
pseudotumor xantomatoso,
proliferación miofibroblástica pseudosarcomatosa,
proliferación miofibroblástica inflamatorioa o miofibroblastoma.
Se trata de un proceso benigno poco frecuente que se puede confundir con procesos malgnos localizado frecuentemente en pulmones y órbitas pero que puede estar presente en casi cualquier órgano.
Es una lesión borderline de significado incierto,
de probable origen reactivo o neoplásico.
Edad de presentación: infancia y adultos jóvenes.
Normalmente asintomático o asociado a síndrome constitucional consistente en fiebre ,
pérdida de peso,
masa abdominal)
Puede presentarse como masa única o multiples.
Se trata de infiltrados de células polimórifcas inflamatorias (cambios inflamatorios agudos y crónicos) con variable cantidad de fibrosis,
necrosis,
reacción granulomatosa y células fusiformes miofibroblásticas.
No existen hallazgos radiológicos específicos.
Vascularización prominente,
principalmente en fases tardías (fibrosis) Fig. 23