Por su particular origen embriológico y su localización estratégica en la base del cráneo,
existen ciertas enfermedades que afectan característicamente al clivus.
Una vez repasadas la anatomía normal de la base del cráneo,
clasificamos estas lesiones en tres grupos:
a) Patología neoplásica centrada en el clivus: cordoma,
plasmocitoma,
linfoma,
condrosarcoma,
meningioma y metástasis.
b) Lesiones seudotumorales: displasia fibrosa,
enfermedad de Paget,
histiocitosis de células de Langerhans y radionecrosis.
c) Afectación del clivus por lesiones vecinas: macroadenoma hipofisario y tumores nasofaríngeos.
Conocer y comparar las características clínicas y radiológicas de cada una de estas entidades debe permitir,
si no concluir un diagnóstico definitivo,
al menos,
discriminar entre lesiones benignas y malignas.
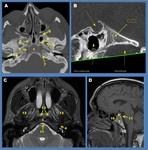
ANATOMÍA Fig. 1
El clivus es la porción de la base del cráneo situada entre el agujero magno y la cara dorsal de la silla turca.
Es el resultado de la fusión de la sincondrosis entre los huesos basioccipital y exooccipital,
cuyo periodo de osificación puede finalizar incluso a los 25 años.1.
El margen anterior del clivus corresponde con la pared posterior del seno esfenoidal,
la cara posterior delimita las cisternas prepontina y premedular.
En la porción inferior alcanza la cara posterior de la nasofarínge.
Los márgenes laterales se corresponden con la cisura petrooccipital,
que discurre desde el seno cavernoso hasta el agujero yugular.
Características en TC: Los mejores planos para analizar el clivus en TC son el sagital y el axial.
Contiene un centro de hueso esponjoso con medula ósea delimitado por cortical compacta.
Con la edad,
se produce una metamorfosis grasa de la médula ósea central,
que disminuye sus valores de atenuación.
Características en RM: En el plano sagital,
el clivus tiene forma triangular con la base en dirección a la silla turca y el vértice apuntando hacia el margen anterior del agujero magno.
La cortical ósea se visualiza como una línea negra tanto con potenciación T1 como T2.
La señal del hueso esponjoso depende del grado de madurez de la medular; normalmente el tejido hematopoyético,
que predomina en individuos jóvenes,
es hipointenso en T1,
mientras que cuando se produce metamorfosis grasa se torna más hiperintenso.
La mayor parte de las lesiones del clivus tienen un comportamiento hipointenso con potenciación T1 e hiperintenso con potenciación T2.
PATOLOGÍA NEOPLÁSICA DEL CLIVUS
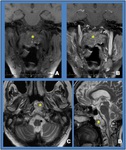
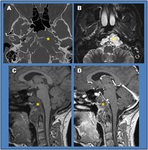
Cordoma (Fig. 2 y Fig. 3).
Los cordomas son tumores infrecuentes de lento crecimiento que surgen a partir de remanentes de la notocorda,
por lo que pueden aparecer a lo largo de todo el neuroeje,
desde la base del cráneo hasta el sacro.
Aunque el cordoma no tiene un signo radiológico característico,
debe considerarse cada vez que se identifique una lesión destructiva del clivus en un adulto joven.
2.
Aproximadamente el 35% de los cordomas asientan en la base del cráneo y,
de estos,
la gran mayoría en el clivus.
Los cordomas del ápex petroso existen,
pero son extremadamente infrecuentes.
La edad de aparición suele oscilar entre los 20 y 40 años se afecta por igual a ambos sexos3.
Aunque histologicamente son tumores benignos,
tienen un comportamiento agresivo y una tasa de recurrencia cercana al 100% incluso tras la realización de cirugía radical,
por lo que el pronóstico es malo.
Son muy raras su malignización histológica y la aparición de metástasis que,
en caso de suceder,
aparecen de forma algo más frecuente en los cordomas sacrocoxígeos.
Radiologicamente,
el cordoma es una masa de partes blandas con destrucción ósea.
Con frecuencia los cordomas son tumores extensos,
que invaden el espacio epidural y causan compresión del sistema vértebrobasilar y del tronco del encéfalo.
En la TC se diferencian con claridad zonas de calcificación que se corresponden con fragmentos del hueso destruido.
En la RM los cordomas son isointensos o ligeramente hiperintensos con potenciación T1 e hiperintensos con potenciación T2; además,
puede haber áreas de baja seña correspondiendo con las calcificaciones internas y zonas de degeneración quística.
Tras la administración de contraste paramagnético intravenoso puede observarse un marcado realce.
Tanto la TC como la RM son técnicas adecuadas para detectar este tumor; no obstante,
se considera a la RM superior en la evaluación de la extensión tumoral,
especialmente en lo que respecta al atrapamiento o desplazamiento de estructuras vasculares y al grado de afectación intracraneal4.
El condroma condroide es un subtipo de cordoma que asocial un mejor pronóstico.
No existe un consenso en la literatura sobre si existen características radiológicas que permitan su diferenciación del cordoma clásico4,5.
Mieloma múltiple / Plasmocitoma (Fig. 4)
El término plasmocitoma hace referencia a un tumor maligno de células plasmáticas que asienta sobre partes blandas o sobre el esqueleto.
La forma esquelética con frecuencia evoluciona hacia mieloma múltiple en el transcurso de 5 a 10 años.
El diagnóstico de mieloma múltiple se basa en diversos test sanguíneos (electroforesis,
frotis de sangre periférica),
biopsia de médula ósea y exploraciones radiográficas.
Diversos estudios han demostrado una mayor sensibilidad de la TC multicorte respecto a las radiografías convencionales para la evaluación de la extensión del componente lítico óseo.
En la TC,
el plasmocitoma se comporta como una lesión lítica de bordes esclerosos.
En RM,
pueden apreciarse zonas de pérdida de señal con potenciación T1.
Las secuencias STIR y TSE T2 resultan las más sensibles para su detección,
donde se observa un aumento de la señal.
Con la administración de contraste iv,
la lesión no tratada muestra un realce difuso.
Los plamocitomas pueden contener también zonas de vacío de señal en relación con la presencia de estructuras vasculares,
así como difusión restringida,
con bajos valores en el coeficiente de difusión aparente,
por su alta celularidad.
La radioterapia es la primera opción terapeútica cuando el tumor es radiosensible.
La cirugía se reserva para casos resistentes 7,8.
Linfoma
El linfoma óseo es una neoplasia infrecuente que supone menos del 5% del total de tumores óseos.
No suele darse en menores de 10 años y su pico de prevalencia se situa en torno a la sexta y séptima décadas de la vida.
Aunque los lugares más comúnmente afectados son el fémur,
pelvis,
húmero y tibia,
la afectación de vértebras y clivus no es extraña.
El linfoma óseo cursa con dolor insidioso e intermitente que puede persistir durante meses.
Puede haber edema local,
masa de partes blandas y afectación sistémica como fiebre y pérdida de peso.
La TC aporta una buena definición del componente lítico o blástico óseo,
de la integridad cortical y de la presencia de reacción perióstica y de masa de partes blandas.
La RM se demuestra superior en la evaluación de la afectación de la médula ósea y del componente de partes blandas.
En RM,
las secuencias con potenciación T1 son las más adecuadas para detectar cambios en la médula ósea,
observando pérdida de señal en las zonas afectadas,
que muestran un aumento de señal con potenciación T2.
El edema peritumoral y los cambios reactivos en la médula ósea pueden comportarse también con una hiperintensidad en T2,
exceptuando la fibrosis,
que presenta una señal baja.
Tras la administración de contraste iv se suele observar realce del componente tumoral 9.
Condrosarcoma
El condrosarcoma es un tumor de lento crecimiento de estirpe cartilaginosa.
Las ¾ partes de los condrosarcomas aparecen en la base del cráneo,
que es su principal localización,
por ello supone aproximadamente el 6% de los tumores de la base del cráneo.
Puede surgir en el cartílago,
hueso endocondral o células mesenquimales primitivas en el cerebro,
meninges,
hueso membranoso o partes blandas.
El condrosarcoma secundario suele aparecer sobre hueso patológico (displasia fibrosa,
enfermedad de Paget,
osteocondroma).
Las manifestaciones clínicas dependen de la localización,
pero característicamente cursa con múltiples neuropatías por afectación de pares craneales 10.
La TC es útil para visualizar la matriz calficicada característica del condrosarcoma.
Las calcificaciones varían en apariencia,
pero pueden ser puntiformes y amorfas.
Otros hallazgos en la TC son la erosión y destrucción ósea y la identificación de un componente de partes blandas que realza tras la administración de contraste.
La RM normalmente es menos específica y se emplea más para evaluar la extensión de la enfermedad.
El tumor es hipointenso respecto al cerebro con potenciación T1 e hiperintenso con potenciación T2.
Los focos internos de baja señal se corresponden con las calcificaciones.
Con contraste paramagnético se aprecia un realce heterogéneo,
por la misma razón2.
Meningioma
La presentación habitual del meningioma es la de un tumor benigno intracraneal que surge a partir de células aracnoideas de la superficie interna de la duramadre.
Aproximadamente el 33% afectan a la base del cráneo,
especialmente al ala del esfenoides.
La afectación del clivus puede darse en los meningiomas en placa y en los meningiomas intraóseos,
que son variantes infrecuentes de este tipo de tumor.
Los hallazos en TC consisten en una masa hiperdensa con marcado realce con contraste yodado, que puede asociar una hiperostosis reactiva del hueso como signo de posible invasión ósea.
Esta hiperostosis puede inducir a la confusión con otras entidades tales como la displasia fibrosa; sin embargo,
la menor edad del paciente y la ausencia de masa de partes blandas permiten su diferenciación del meningioma11.
En RM,
los meningiomas suelen ser isointensos o ligeramente hipointensos respecto a la sustancia gris en secuencias con potenciación T1.
Con potenciación T2,
aproximadamente el 10% son hipointensos,
el 50% isointensos y el 40% hiperintensos respecto a la sustancia gris.
Se observa un marcado realce homogéneo con la administración de contraste12.
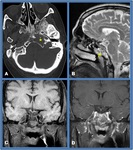
Metástasis (Fig. 5)
Aunque las metastasis hematógenas localizadas en la base del cráneo son atípicas,
superan en número a las neoplasias primarias.
Los tumores primarios más frecuentes en dar estas metástasis asientan en la próstata,
pulmón,
mama y riñón.
La lesión suele constar de un componente de masa de partes blandas.
La mayor parte de estas metástasis se corresponden con áreas de destrucción ósea en el TC,
excepto las metástasis del cáncer de próstata,
que suelen ser osteoblásticas.
En las imágenes de RM con potenciación T1 se observa un descenso de señal como resultado del reemplazamiento de la médula ósea.
Con potenciación T2,
las metástasis suelen ser hiperintensas respecto a la médula normal.
En las secuencias T1 con contraste,
tanto la afectación ósea como de partes blandas muestran captación del mismo.
En pacientes sin historia previa de procesos neoplásicos,
no es posible diferenciar solo por los estudios de imagen entre neoplasia primaria o metástasis,
en estos casos,
la presencia de lesiones en otras zonas del cráneo es de gran ayuda para realizar el diagnóstico2.
LESIONES SEUDOTUMORALES
Displasia Fibrosa (Fig. 6)
La displasia fibrosa en una anomalía en la formación ósea de etiología desconocida en la cual, conforme se desarrolla el hueso,
el tejido fibroso se expande y lo debilita.
La displasia fibrosa es una entidad benigna,
pero puede producir que el hueso se deforme y sea más susceptible a las fracturas.
En la base del cráneo,
puede condicionar también la existencia de atrapamientos nerviosos.
En el 27% de las displasias fibrosas monostóticas y en más del 50% de las poliostóticas se encuentra afectación de la base del cráneo.
En la TC,
la lesión tiene una densidad característica en “vidrio deslustrado”,
el hueso se amplía y los agujeros y cisuras craneales pueden verse reducidos o desplazados; si bien no suele desestructurarse en exceso el contorno óseo normal.
En RM,
la displasia fibrosa en fase inactiva tiene baja señal con potenciación T2 y no realza o muestra un realce mínimo con contraste iv.
Las lesiones activas contienen formaciones quísticas hiperintensas con potenciación T2,
zonas espontáneamente hiperintensas con potenciación T1 y un fuerte realce tras la administración de gadolinio13.
Enfermedad de Paget
La enfermedad de Paget puede afectar también a la base del cráneo,
especialmente al clivus y la porción adyacente del hueso esfenoidal.
La principal alteración en el Paget consiste en un remodelado óseo excesivo y anormal que resulta en un patrón engrosado y trabecular del hueso,
descrito como en mosaico o en puzzle.
Se distinguen tres fases en la enfermedad: 1) Fase lítica (incipiente,
activa),
en la que predomina la actividad osteoclástica,
2) Fase mixta (activa),
durante la cual hay reparación superpuesta con la reabsorción ósea.
3) Fase blástica (inactiva),
con predominio osteoblástico.
Los hallazgos en la TC incluyen una pérdida de la trabeculación ósea normal en las áreas líticas y un engrosamiento de la cortical y de las trabéculas,
que siguen un patrón desordenado en las fases de menor actividad.
En la fase blástica puede verse una mayor esclerosis.
La médula ósea suele presentar valores de atenuación correspondientes con grasa.
En RM,
la médula ósea en la enfermedad de Paget tiene un comportamiento variable que depende de la fase de la enfermedad y de la composición histológica de la médula.
Se distinguen tres patrones:
1) En la mayoría de los casos,
la señal de la médula ósea amarilla se mantiene con independencia de la secuencia de pulso empleada.
2) En algunos casos,
en la fase lítica o en el estadio precoz de la fase activa,
la médula tiene un comportamiento heterogéneo con potenciación T1 y T2.
En las imágenes potenciadas en T1,
la médula tiene una disminución de señal,
asemejándose al músculo,
aunque con la presencia de focos internos más hiperintensos correspondiendo con médula conservada.
En secuencias potenciadas en T2,
la médula es heterogénea con áreas de alta intensidad de señal.
El volumen del canal medular puede verse reducido por el engrosamiento de la cortical.
3) En la fase blástica (inactiva),
la medula tiene una baja intensidad de señal en todas las secuencias que representa la esclerosis 14.
Histiocitosis de células de Langerhans
La histiocitosis de células de Langerhans es un proceso de etiología desconocida que afecta con frecuencia a la base del cráneo,
inlcuyendo el clivus.
En la TC,
aparece como una lesión destructiva bien circunscrita,
habitualmente sin márgenes esclerosos,
que puede producir erosión ósea.
En la RM,
las lesiones aparecen como masas de partes blandas rodeadas de médula ósea y edema de partes blandas.
Una marcada captación de contraste puede apreciarse tanto en los estudios de TC como de RM 15.
Radionecrosis (Fig. 7)
La necrosis en la porción central la base del cráneo se observa con frecuencia después de la radioterapia para el carcinoma nasofaríngeo,
sobre todo en el esfenoides y el clivus.
En la TC,
clásicamente se observa disrupción de la cortical ósea con pérdida de trabeculaciones,
así como un aumento heterogéneo de la señal con potenciación T2 y un realce parcheado en las secuencias T1 post-contraste16.
La osteorradionecrosis,
con o sin osteomielitis asociada,
puede ser extremadamente difícil de diferenciar de una recidiva tumoral.
Aunque exista una destrucción ósea franca,
sin una masa de tejido blando,
la lesión es más sugestiva de osteorradionecrosis.
Los músculos adyacentes puede aparecer edematosos y mostrar realce intenso,
que puede ser difícil de diferenciar de una recurrencia tumoral si la afectación ósea no resulta visible en la TC.
Cuando una voluminosa masa de partes blandas se observa en relación con la destrucción ósea,
la biopsia se debe realizar para excluir una recidiva del tumor17.
LESIONES PARACLIVALES
Carcinoma invasivo nasofaríngeo (Fig. 8)
El carcinoma invasivo nasofaríngeo es la tumoración primaria que con mayor frecuencia se extiende a la base del cráneo.
Normalmente se trata de una tumoración con origen en el epitelio escamoso nasofaríngeo.
En la TC es una masa hipodensa.
En RM es isointensa con respecto al músculo con potenciación T1 e hiperintensa con potenciación T2.
En ambas técnicas se aprecia realce tras la administración de contraste iv.
Cuando hay invasión del clivus,
se observa erosión en la TC y reemplazamiento de la médula ósea en RM,
donde se manifiesta como una pérdida de señal en secuencias con potenciación T1.
En ausencia de una lesión nasofaríngea identificable,
los hallazgos en los estudios de imagen resultan inespecíficos y deben considerarse otros diagnósticos.
Metástasis,
linfoma y neoplasias primarias óseas son otras entidades que pueden causar simultáneamente erosión del clivus y una masa de partes blandas en la nasofaringe2.
Angiofibroma nasofaríngeo juvenil
El angiofibroma nasofaríngeo juvenil es un tumor infrecuente con un alto componente vascular que aparece con mayor frecuencia en varones adolescentes.
La presentación clínica se relaciona con la extensión tumoral.
Obstrucción nasal,
epixtasis y deformidad facial son los síntomas iniciales más característicos.
Puesto que es frecuente encontrar una extensa diseminación local del tumor en el momento del diagnóstico,
la afectación del clivus y seno cavernoso deben ser valoradas en los estudios radiológicos.
En la TC se identifica como una masa de partes blandas en la nasofarínge y espacios adyacentes.
En RM suele tener una señal intermedia con potenciación T1,
mientras que es muy variable con potenciación T2.
En ambas secuencias,
pueden apreciarse focos internos de vacío de señal representando vasos intratumorales.
Tanto en TC como en RM se demuestra un intenso realce con contraste iv.
La arteriografía convencional se emplea con frecuencia para obtener una información detallada del aporte vascular del tumor y facilitar su embolización prequirúrgica2.
Macroadenoma hipofisario invasivo (Fig. 9)
En adultos,
la mayor parte de los tumores hipofisarios son adenomas.
Se trata de una lesión histológicamente benigna circunscrita a la silla turca o cisterna supraselar.
Pueden expandirse lateralmente al seno cavernoso o en dirección inferior al seno esfenoidal y a la base del cráneo.
Cuando existe esta invasión,
puede ser difícil la diferenciación entre el adenoma y otras lesiones como el carcinoma del seno esfenoidal,
el cordoma o una extensión hacia el cráneo del carcinoma nasofaríngeo.
La TC muestra una expansión de la silla turca y realce de la masa de partes blandas,
con destrucción ósea.
En RM,
las imágenes con potenciación T1 muestran una masa isointensa o ligeramente hipointensa que realza tras la administración de contraste paramagnético 2.
Aunque es una entidad extremadamente rara,
debemos recordar que durante el desarrollo embrionario existe una migración del lóbulo anterior de la hipófisis por el canal de Rathke.
Por ello,
es posible que existan restos hipofisarios que desencadenen un adenoma intraóseo18.
Otros tumores paraclivales
Anteriormente se han descrito las entidades neoplásicas más frecuentes que surgen en las proximidades del clivus y pueden condicionar su infiltración.
Sin embargo,
cualquier proceso maligno es susceptible de invadir el clivus por contigüidad.
La Fig. 10 muestra un ejemplo de un tumor infrecuente en la nasofarínge,
el carcinoma adenoide quístico,
que produce una gran invasión de la base del cráneo.
OTRAS LESIONES
En esta presentación,
se describen las entidades más frecuentes que pueden afectar al clivus; sin embargo,
hay un amplio espectro de enfermedades de diverso origen (neoplásico,
infeccioso,
metabólico,
idiopático) que,
con mucha menor frecuencia,
pueden causar una lesión en el clivus.
En la Fig. 11 se muestra,
a modo de curiosidad,
un caso de ecchordosis physalifora,
una lesión benigna que resulta de remanentes ectópicos de la notocorda.
CLAVES PARA EL DIAGNÓSTICO DIFERENCIAL 19
Una lesión en el clivus puede encontrarse como un hallazgo incidental en un estudio de imagen.
Cuando produce sintomatología clínica,
suele cursar con cefalea o neuropatías craneales,
especialmente lesiones del VI par.
La RM es la mejor técnica para detectar y caracterizar una lesión en el clivus.
La secuencia con potenciación T1 en el plano sagital es posiblemente la más importante,
las lesiones muestran una pérdida de la señal de la médula grasa que ocupa el clivus normal.
La TC es complementaria a la RM,
si bien con frecuencia la supera en lesiones óseas.
Resulta especialmente útil para lesiones tales como la enfermedad de Paget,
displasia fibrosa o tumores óseos primarios.
Ante una lesión que invade tanto el clivus como la nasofaringe,
debe plantearse el diagnóstico diferencial entre el carcinoma nasofaríngeo (incluyendo el angiofibroma nasofaríngeo juvenil si se trata de un paciente joven) y el linfoma.
Si la lesion surge de la hipófisis,
debe considerarse en primer lugar un adenoma hipofisario.
Una hiperintensidad evidente con potenciación T2 orienta hacia cordoma o condrosarcoma.