Al ser la EC una entidad que característicamente presenta periodos de remisión y recaída,
los pacientes que la padecen se benefician significativamente del conocimiento detallado de la localización,
extensión,
actividad y severidad de las lesiones inflamatorias,
así como la detección de posibles complicaciones asociadas,
debido a que esta información colabora en el manejo terapéutico óptimo,
factor fundamental en el pronóstico de la enfermedad.
Existe una creciente evidencia de la utilidad de la RM como técnica de referencia para la valoración de la actividad en la EC,
especialmente en el intestino delgado.
La RM permite detectar con una alta precisión la actividad en la EC,
valorando las lesiones intra y extraluminales de manera adecuada,
además de las complicaciones asociadas,
tanto agudas como crónicas,
aunque en las estenosis puede existir un solapamiento de inflamación con fibrosis.
También hay que resaltar que esta técnica no irradia (consideración fundamental en pacientes que van a ser revalorados desde temprana edad en múltiples ocasiones) y presenta una baja incidencia de efectos adversos relacionados al medio de contraste.
Conocer la información que nos aporta la anatomía patológica y correlacionarla con las imágenes de la RM permite una mejor interpretación de estos hallazgos,
resultando en un impacto positivo en el manejo clínico del paciente
PATRÓN DE AFECTACIÓN LUMINAL
1) Estadio no ulcerativo:

Table 1: Correlación entre los hallazgos RM y de anatomía patológica en pacientes con EC que presentan patrón de afectación luminal en estadio no ulcerativo.
Los hallazgos en la RM mas comúnmente encontrados en los pacientes con actividad luminal son:
- Engrosamiento parietal (>3 mm).
- Hipercaptación de la mucosa.
- Vasa recta prominente.

Fig. 1: Segmento ileal con signos de EC activa: engrosamiento mural, captación de la mucosa (cabezas de flechas naranja) y vasa recta prominente (cabezas de flechas rojas).
La pared intestinal inflamada demuestra una significativa captación de contraste posterior a su administración,
y esta intensidad de captación se correlaciona con la severidad del proceso inflamatorio.

Fig. 2: Imagen potenciada en T1 con saturación grasa adquirida posterior a la administración de contraste intravenoso (Fig. a) que demuestra intensa captación mural del íleon distal. El paciente es intervenido quirúrgicamente por mala respuesta al tratamiento. La pieza quirúrgica (Fig. b) demuestra engrosamiento mural, así como lesiones mucosas inflamatorias. El estudio histológico (Fig. c) demuestra un importante número de neutrófilos y ulceraciones mucosas. Un marcador específico para endotelio (CD31) (Fig. d) revela un incremento en la vascularización que explica la hipercaptación visualizada en la Fig a.
2) Estadio ulcerativo:

Table 2: Correlación entre los hallazgos RM y de anatomía patológica en pacientes con EC que presentan patrón de afectación luminal en estadio ulcerativo.
Las úlceras son consideradas lesiones severas (así como las fístulas y abscesos) en los pacientes con EC,
y la detección de este tipo lesiones tiene importantes implicaciones clínicas tanto en:
- Tratamiento: los pacientes son candidatos a recibir tratamiento con drogas anti TNF (previamente se debe descartar la presencia de abscesos por el riesgo de sepsis).
- Pronóstico: la persistencia de lesiones severas posterior al tratamiento adecuado indica peor pronóstico,
con mayor probabilidad de hospitalización y resecciones intestinales.
Con respecto a las úlceras:
- Son más comunes en el borde mesentérico del intestino delgado.
- Pueden progresar en profundidad alcanzando la muscular propia o incluso traspasarla provocando fístulas y abscesos.
- La combinación de úlceras longitudinales y transversales confluyentes,
rodeada por áreas polipoideas en la mucosa (pseudopólipos inflamatorios),
produce la presencia del "patrón en empedrado" Fig. 5.

Fig. 3: Úlceras en paciente con EC. Lesiones mucosas profundas e irregulares en un segmento ileal engrosado e hipercaptante (cabezas de flechas), las cuales se correlacionan con los hallazgos visualizados en la pieza quirúrgica (Fig. b), en donde se aprecian úlceras longitudinales (flechas).

Fig. 4: Úlcera en intestino delgado. Imagen potenciada en T1 con saturación grasa adquirida posterior a la administración de contraste intravenoso (Fig. a) que demuestra engrosamiento parietal con hipercaptación de la mucosa. Observe la pequeña lesión de aspecto lineal hipercaptante en mucosa que alcanzan capas profundas de la pared (flechas en Fig a). En el estudio histológico (Fig. b) de la pieza quirúrgica del segmento visualizado en la Fig. a se observa la presencia de úlceras en la base de las criptas (flechas en Fig. b) con infiltrado neutrofílico adyacente (estrellas en Fig. b).

Fig. 5: Imagen axial potenciada en T2 con saturación grasa (Fig. a) e imagen coronal potenciada en T1 con saturación grasa adquirida posterior a la administración de contraste intravenoso (Fig. b) que demuestran actividad severa de la EC en segmento terminal neoileal. Obsérvese en la Fig. b la hipercaptación posterior a la administración de contraste intravenoso. La presencia de edema también es un signo indicativo de actividad de la enfermedad que se observa en la Fig. a. La pieza quirúrgica (Figs. c y d) demuestra engrosamiento mural, así como úlceras en la mucosa (estrellas) alternado por áreas polipoideas (flechas) que conforman en patrón en empedrado que se observa en pacientes con EC.
Los pólipos post-inflamatorios Fig. 6 son nódulos sésiles elevados rojizos rodeados de mucosa regenerativa que se encuentran en zonas donde han ocurrido episodios severos o repetidos de actividad inflamatoria.

Fig. 6: La reconstrucción multiplanar sagital de secuencia 3D potenciada en T1 con saturación grasa posterior a la administración de contraste intravenoso (Fig. a) demuestra la presencia de múltiples pólipos post-inflamatorios en la luz del colon descendente (flechas) de paciente con EC activa. Se le realiza hemicolectomía izquierda por anemia severa persistente. El estudio macroscópico (Fig. b) demuestra un importante número de lesiones polipoideas en la superficie de la luz colónica, así como eritema de la mucosa. La Fig. c corresponde al estudio histológico. Los pólipos post-inflamatorios en la EC son típicamente pequeños y múltiples, aunque también pueden presentar un aspecto filiforme (flecha).
PATRÓN DE AFECTACIÓN FISTULIZANTE
La EC fistulizante consiste en la presencia de lesiones penetrantes,
que incluyen fístulas y/o abscesos.
La fístula es una comunicación patológica entre la luz intestinal y otra estructura.
1) Fístulas:

Table 3: Correlación entre los hallazgos RM y de anatomía patológica en pacientes con EC que presentan patrón de afectación fistulizante con presencia de fístulas.
- Las localizaciones más comunes de las fístulas en pacientes con EC son: perianal (54%),
entero-entérica (24%),
rectovaginal (9%) y otras (13%).
- Los pacientes que presentan fístulas son candidatos a tratamiento con terapia anti-TNF,
descartando previamente la presencia de abscesos.
- Las fístulas entero-entéricas en muchas ocasiones no son sospechadas clínicamente debido a que pueden enmascararse por los síntomas inflamatorios.
Estas fístulas y las rectovaginales son las que presentan una menor respuesta al tratamiento médico,
teniendo que requerir cirugía.
- Las fístulas se pueden complicar con la presencia de abscesos y/o plastrones inflamatorios asociados.
Algunas veces no es posible identificar la fístula y sólo se identifica el plastrón inflamatorio,
que puede adquirir la apariencia de una estrella,
conocido como el "signo de la estrella" Fig. 9 .
Este signo está altamente asociado con la presencia de fístulas,
por lo cual hay que sospecharlas aunque no se detecten a través de los estudios de imagen.
- En ocasiones puede ser complicado diferenciar una fístula de adherencias postquirúrgicas o residuales a eventos inflamatorios previos Fig. 10 .
Es importante recordar que la afectación inflamatoria de la serosa puede provocar adherencias entre las asas intestinales,
con el peritoneo parietal o con la vejiga.

Fig. 7: Imágenes potenciadas en T1 eco de gradiente (VIBE) posterior a la administración de contraste intravenoso en planos axial (Fig. a y b) y coronal (Fig c). Fístula entero-entérica compleja (flechas en Fig. a y b) que compromete el ciego (C) y el íleon distal (I). Observe la dilatación de las asas de intestino delgado secundaria a la presencia de una masa/flegmón inflamatorio que provoca oclusión de la luz. Se realiza resección quirúrgica que incluye múltiples asas de intestino delgado comprometidas. La pieza quirúrgica presenta una excelente correlación con los hallazgo de imagen (Fig. b). Véase como la fístula tambien envuelve el duodeno (D) (flecha en Fig. c), el cual se localiza en el retroperitoneo. Esta información fue fundamental para una adecuada planificación quirúrgica, evitando lesiones duodenales durante la cirugía.

Fig. 8: Fístula ileo-ileal. Imágenes potenciadas en T1 posterior a la administración de gadolinio en plano coronal (Fig. a y b) y axial (Fig. d), que demuestran el tracto fistuloso como una lesión de aspecto lineal hipercaptante que comunica la luz de ambos segmento intestinales (flecha en Fig. a). Observe en la Fig.b la correlación con la pieza quirúrgica, en la cual se observa eritema en la mucosa adyacente a la fístula (flecha). En la Fig. d se identifican un tracto fistuloso a mesenterio asociado a un plastrón inflamatorio (cabeza de flecha). En la Fig. c se demuestra la pieza quirúrgica con los hallazgos visualizados en la Fig. d (cabeza de flecha).

Fig. 9: Reconstrucciones multiplanares de secuencia 3D potenciadas en T1 con saturación grasa posterior a la administración de contraste intravenoso (Fig. a, b y d) las cuales demuestran fistula entero-entérica (cabeza de flecha en Fig. a) con gran masa inflamatoria asociada en fosa ilíaca derecha (flechas en Fig. a). En la Fig. B se correlaciona la pieza quirúrgica con la imagen de RM. Observe la fístula en la pieza quirúrgica (cabeza de flecha en Fig. b y c). En la reconstrucción multiplanar sagital de secuencia 3D potenciada en T1 con saturación grasa posterior a la administración de contraste intravenoso se puede observar con mayor claridad el signo de la estrella.

Fig. 10: Adherencia entre dos segmentos intestinales en paciente con EC. Imagen 3D potenciada en T1 con saturación grasa en plano coronal posterior a la administración intravenoso de contraste (Fig. a) en donde se demuestra una banda lineal que capta contraste (cabeza de flecha en Fig. a) la cual une una pared intestinal con signos de actividad (estrella roja) que se encuentra engrosada e hipercaptante con asa de aspecto normal (estrella amarilla) que se encuentra adyacente. Observe la ausencia de cambios inflamatorios perientéricos lo cual sugiere adherencia intestinal. En la Fig. B se aprecia la pieza macroscópica.
2) Abscesos:

Table 4: Correlación entre los hallazgos RM y de anatomía patológica en pacientes con EC que presentan patrón de afectación fistulizante con presencia de abscesos.
- Los abscesos aparecen como una colección líquida extraintestinal,
con o sin gas en su interior,
rodeada de una pared engrosada e hipercaptante.
- Los abscesos usualmente se asocian con la presencia de fístulas,
adherencias y masas/plastrones inflamatorios.
- En caso de que los abscesos no se resuelvan mediante tratamiento médico o drenaje percutáneo,
requerirán cirugía para su resolución.
En los casos donde se plantee el tratamiento quirúrgico,
una detallada descripción de la relación del absceso con las estructuras adyacentes mediante RM es de gran utilidad para una correcta planificación quirúrgica.

Fig. 11: Paciente con EC fistulizante asociada a la presencia de absceso pélvico y masa inflamatoria (flechas verdes en Figs. a y b). Signos de actividad inflamatoria en segmento ileal localizado en pelvis (flechas rojas en Figs. b y c). Observe como un segmento ileal adyacente se encuentra envuelto por la masa inflamatoria (flecha naranja en Figs b y c). En la Fig.c podemos observar la pieza quirúrgica y su correlación con los hallazgos en las imágenes de RM.

Fig. 12: Paciente con EC conocida que consulta por presentar neumaturia, dolor pélvico y fiebre. Reconstrucciones multiplanares axiales de secuencias potenciadas en T1 con saturación grasa posterior a la administración de contraste intravenoso (Figs. a y b) que demuestran masa inflamatoria (flechas en Fig. a) que rodea el sigma, asociado a la presencia de un absceso (estrella roja en Fig. a). También se identifica tracto fistuloso entre el absceso y la cúpula vesical (cabeza de flecha en Fig. b). La pieza quirúrgica (Fig. c) se correlaciona con la hallazgos visualizados en las imágenes de RM: Masa inflamatoria con absceso (estrella roja en Fig. c) adyacente a la pared del sigma (estrella azul en Fig. c).
PATRÓN DE AFECTACIÓN ESTENOSANTE:
La información fundamental a valorar en el estudio radiológico de las estenosis consiste en:
- La estenosis es predominantemente fibrótica,
inflamatoria o mixta.
- Localización y extensión.
- Morfología de la estenosis (curva o recta).

Table 5: Correlación entre los hallazgos RM y de anatomía patológica en pacientes con EC que presentan patrón de afectación estenosante.
- Estenosis inflamatoria vs fibroestenosis:
- Los eventos inflamatorios repetidos que afectan las asas intestinales en la EC pueden asociarse con la aparición de cambios fibróticos en la pared intestinal.
- Es importante diferenciar actividad inflamatoria de fibrosis en las asas intestinales engrosadas,
debido a que tiene implicaciones significativas en el tratamiento del paciente.
- En muchas ocasiones la inflamación y la fibrosis coexiste,
lo cual hace un verdadero reto para el radiólogo diferenciar entre las estenosis inflamatorias (estenosis agudas) y las fibroestenosis (estenosis crónicas).
Sin embargo,
se debe intentar en lo posible identificar esta diferencia dada su implicación en el manejo del paciente con síntomas oclusivos: en las estenosis con un componente inflamatorio con o sin fibrosis se debe intensificar el tratamiento médico debido a la mayor probabilidad de respuesta; en cambio,
cuando predomina el componente de fibroestenosis existe una baja probabilidad de respuesta al tratamiento médico,
y muy posiblemente el paciente sea candidato a tratamiento quirúrgico o dilatación endoscópica (debido a la progresiva implantación de la enteroscopia y la mejora en la técnica,
las dilataciones endoscópicas se han convertido en la primera opción terapéutica,
incluso en el intestino delgado).
- Es importante remarcar que las fibroestenosis se pueden encontrar incluso en la presencia lesiones inflamatorias severas.

Fig. 13: Paciente con EC que presenta estenosis que afecta extenso segmento ileocolónico. Segmento proximal y distal (estrella verde en Fig. a) que demuestra signos radiológicos de actividad, con área de fibroestenosis localizada entre estos segmentos (estrella roja en Fig. a). En la pieza quirúrgica se aprecia la correlación con lo hallazgos de imagen: dilatación del segmento proximal pre-estenótico (estrella verde en Fig. b) con eritema y superficie nodular de la mucosa intestinal; en el segmento medio se aprecia la fibroestenosis, con una severa disminución de la luz asociada a engrosamiento de la submucosa debido a la fibrosis (estrella roja en Fig. b).

Fig. 14: Estenosis con predominio de componente inflamatorio en íleon terminal. El estudio histológico (Fig. a) demuestra múltiples vasos dilatados en la pared intestinal (tinción CD 31 en Fig. a) que explica el pico de captación precoz posterior a la administración de contraste intravenoso (Fig. b). Se aprecia una marcada infiltración de neutrófilos, así como hiperplasia linfoide en las capas profundas (estrella amarilla). La positividad para el colágeno es débil (tinción tricrómica). Observe que no hay diferencia entre la captación a los 120 segundos y a los 7 minutos. (Figs. b y c).

Fig. 15: Depósito de fibras gruesas de colágeno (véase la tinción tricrómica) con escasa fibrosis (reticulina) laxa asociado a la presencia de escasos y finos vasos (CD 31) localizados en las capas profundas de la fibroestenosis, explicando el pico tardío y lento de captación en estas capas que se visualiza en el estudio dinámico de RM (Fig. b : Imagen potenciada en T1 con saturación grasa adquirida 70 segundos posterior a la administración del contraste intravenoso; Fig. c: Imagen potenciada en T1 con saturación grasa adquirida 7 minutos posterior a la administración de contraste intravenoso). La coexistencia de la fibrosis con la inflamación no es inusual. Véase el edema en las secuencias potenciadas en T2 con saturación grasa (cabeza de flecha en Fig. d).

Fig. 16: Presencia de lesiones inflamatorias severas en paciente con EC que presenta estenosis crónica. Imágenes axiales potenciadas en T1 con saturación grasa adquiridas posterior a la administración de contraste intravenoso que demuestran hipercaptación temprana de la mucosa (Fig. a) con posterior captación transmural en fases tardías (Fig. b). Véase el edema mural en la imagen potenciada en T2 con saturación grasa (Fig. c). En la Fig. d se visualiza fístula ileo-rectal con contenido líquido en su interior (flechas). La pieza quirúrgica (Fig. d) confirma la presencia de una mucosa ileal eritematosa (estrella amarilla), así como la presencia de la fístula. El examen microscópico (Fig. e) demuestra una importante infiltración neutrofílica (H/E), marcada positividad para el colágeno (tricrómico) y algunos finos vasos arteriales en la submucosa (CD31).
2.
Localización y extensión.
- Es fundamental para el manejo del paciente con EC,
especialmente aquellos que sean candidatos a cirugía, precisar el número de estenosis que presenta ya que a menudo pueden coexistir múltiples de éstas,
lo que se conoce como "mapping" de las estenosis.
- La extensión de las estenosis es relevante para valorar la posibilidad de dilatación endoscópica o estricturoplastias como tratamiento en estos pacientes,
debido a que es una opción terapéutica útil principalmente en fibroestenosis cortas.
3.
Morfología de las estenosis:
- Una fibroestenosis de disposición curva dificulta la dilatación endoscópica.
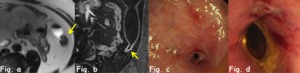
Fig. 17: Estenosis en colon izquierdo en paciente con EC. La endoscopia fue incompleta por imposibilidad de sobrepasar la estenosis, y no identificó signos inflamatorios significativos en el extremo distal de la misma. La RM confirmó la existencia de la estenosis (flecha en Fig. b) y aportó información adicional: estenosis corta de disposición rectilínea. La imagen potenciada en T2 no muestra edema (fecha en Fig. a) y tras la administración de contraste intravenoso presenta un mínimo realce en la imagen potenciada en T1. El conjunto de hallazgos endoscópicos y RM permiten caracterizar la estenosis como de predominio fibrótico, proporcionando información fundamental que permitió tomar la decisión de someter al paciente a dilatación endoscópica de la estenosis, con resultado exitoso del procedimiento (Figs. b y c).
A continuación se presenta un algoritmo potencial de manejo terapéutico en el tratamiento de las estenosis en pacientes con EC.
La información aportada por los estudios endoscópicos e imagenológicos es fundamental para alcanzar un plan terapéutico óptimo en estos pacientes.

Fig. 18: Algoritmo potencial de manejo terapéutico en el tratamiento de las estenosis en pacientes con EC.
EC DE LARGA EVOLUCIÓN

Table 6: Correlación entre los hallazgos RM y de anatomía patológica en pacientes con EC de larga evolución.
1) Proliferación fibrograsa:
- En pacientes con EC de larga evolución se aprecia la presencia de proliferación fibrograsa en el mesenterio generalmente adyacente al segmento intestinal afecto por la enfermedad.
- Es un hallazgo muy específico de la EC pero todavía no se conoce exactamente su causa.
- Algunos estudios sugieren que el tejido graso puede contribuir a la producción de agentes pro-inflamatorios,
presentando un papel potencial como mediador en la actividad inflamatoria.

Fig. 19: Estenosis ileal en paciente con EC de larga data. Proyección de maxima intensidad (Fig. a) y secuencia potenciada en T1 con saturación grasa (Fig. b) que demuestran proliferación fibro-grasa (estrellas amarillas en Figs. a y b) que rodea segmento ileal, así como engrosamiento parietal con hipercaptación posterior a la administración de contraste intravenoso (flechas). Debido a la mala respuesta al tratamiento médico se decide intervenir quirúrgicamente. Véase en la pieza quirúrgica (Fig. c) la proliferación fibro-grasa que rodea al íleo (estrellas amarillas).
2) Depósitos murales de grasa:
- El "signo del halo" Fig. 20 es consecuencia de la estratificación de la pared intestinal como consecuencia de la presencia de una capa conformada por tejido graso.
- A pesar de que el signo del halo se encuentra mas comúnmente en pacientes con EC de larga evolución,
también se puede ver en pacientes con malabsorción (principalmente en celíacos),
enfermedad del injerto contra huésped y obesidad.

Fig. 20: Signo del halo. Véase el depósito de grasa (flechas) en las imágenes potenciadas en T1 posterior a la administración de contraste intravenoso (Fig. a) y las secuencias potenciadas en T2 (Fig. b). La capa interna que presenta captación de contraste en las secuencias potenciadas en T1 representa la mucosa intestinal, mientras que la capa intermedia resulta del engrosamiento consecuencia de la infiltración grasa en la submucosa. La capa externa captante es la muscular propia y la serosa. En el estudio histológico (Fig. c) se evidencia el depósito de tejido graso (estrellas amarillas) entre la muscular de la mucosa y la muscular propia.




























