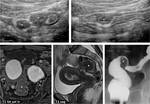
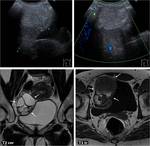
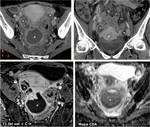
Fig. 1: Portada
1. INTRODUCCIÃN
La forma mÃĄs habitual de presentaciÃģn aguda de una enfermedad del aparato genital femenino es con dolor de instauraciÃģn reciente,
en general centrado en la pelvis y a veces lateralizado a derecha o izquierda.
Puede ser mÃĄs o menos intenso y ocasionalmente asociado a datos de peritonismo.
Pueden sumarse fiebre en mayor o menor grado y sangrado o exudado vaginal.
Deben valorarse atentamente todos los datos clÃnicos y analÃticos asociados.
Abarca desde situaciones que solo requieren de observaciÃģn (como en casos de rotura folicular) hasta otras en las que debe realizarse cirugÃa urgente (como en torsiones de alto grado o rotura de embarazo ectÃģpico con compromiso hemodinÃĄmico).
El objetivo es el tratamiento mÃĄs adecuado a cada situaciÃģn,
lo mÃĄs conservador posible.
Frecuentemente afecta a mujeres premenopÃĄusicas.
Quien se enfrente al diagnÃģstico de la enfermedad causante debe conocer el estado menstrual de la paciente y,
salvo que exista una situaciÃģn de gravedad extrema que impida retrasar el proceso diagnÃģstico,
si es o no gestante.
Siempre ha de considerarse la posibilidad de que la enfermedad causante de la sintomatologÃa de la paciente pueda ser gastrointestinal,
urolÃģgica o musculoesquelÃĐtica.
El abordaje inicial para el diagnÃģstico por imagen suele ser la ecografÃa,
si es posible por vÃa endovaginal o combinada.
La TCpuede ser muy Útil por su disponibilidad y posibilidad prÃĄcticamente generalizada de obtener datos reformateables en cualquier plano,
algo deseable ante una anatomÃa con importante variabilidad individual.
La RM,
por su parte,
aunque menos disponible,
es la herramienta que permite una mayor resoluciÃģn en contraste,
y tambiÃĐn con capacidad multiplanar,
ademÃĄs de evitar la exposiciÃģn a radiaciÃģn en pacientes en general jÃģvenes.
El radiÃģlogo debe utilizar sus herramientas diagnÃģsticas disponibles en funciÃģn de cada situaciÃģn concreta.
2. CAUSAS OVÃRICAS
2.1. QUISTE O FOLÃCULO OVÃRICO ROTO Y/O HEMORRÃGICO
2.1.1. Quiste folicular
Cuando un folÃculo ovÃĄrico crece por la estimulaciÃģn de la FSH en la primera mitad del ciclo puede producir molestias o dolor por compresiÃģn capsular,
en la ovulaciÃģn (fenÃģmeno de Mittleschmerz) o por su rotura o sangrado.
Por convenciÃģn solo se denomina quiste folicular al que supera los 3 cmde diÃĄmetro.
Suele ser el fruto de un folÃculo que no ha llegado a expeler un oocito,
y se mantiene sensible a la estimulaciÃģn estrogÃĐnica.
Se manifiesta como un quiste bien delimitado,
de pared fina,
sin septos ni nÃģdulos,
con contenido anecogÃĐnico y con densidad < 15 UH,
rodeado de tejido ovÃĄrico que contiene folÃculos y al que comprime.
Ante su hallazgo ecogrÃĄfico se recomienda nueva ecografÃa entre los dÃas 5 y 10 del ciclo siguiente.
Algunos persisten durante varios ciclos.
2.1.2. Quiste luteÃnico
Cuando un folÃculo expele el oocito la LH de la segunda mitad del ciclo puede convertir el folÃculo dominante en el cuerpo lÚteo,
que se mantendrÃĄ si se produce la implantaciÃģn,
con neoangiogÃĐnesis en la capa granulosa (que lo hace mÃĄs proclive al sangrado) y producciÃģn de progesterona.
La Ã-hCG lo mantiene durante el primer trimestre del embarazo,
aunque despuÃĐs no siempre se produce su regresiÃģn.
Se manifiesta,
pues,
como una imagen quÃstica con pared mÃĄs gruesa,
ecogÃĐnica y vascularizada.
2.1.3. Rotura y/o hemorragia
Es la causa mÃĄs frecuente de dolor pÃĐlvico agudo en mujeres premenopÃĄusicas no embarazadas afebriles,
y una de las mÃĄs frecuentes en gestantes.
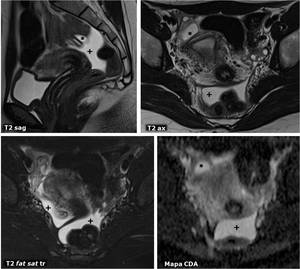
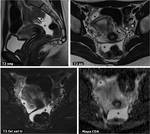
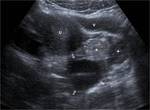
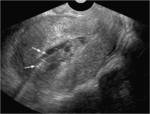
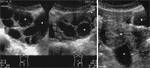
Fig. 2: FolÃculo o quiste folicular roto. Dolor agudo pÃĐlvico derecho periovulatorio en mujer joven. Se aprecia un folÃculo dominante en el ovario derecho (*), rodeado por lÃquido peritoneal que tambiÃĐn se exitende al receso de Douglas (+). El lÃquido tiene una intensidad de seÃąal similar a la del agua en todas las secuencias. No hay, pues, componente hemorrÃĄgico. En el mapa del coeficiente de difusiÃģn aparente (CDA) no se aprecia retricciÃģn de la difusiÃģn del agua ni en el lÃquido peritoneal ni en el folÃculo. El dolor se autolimitÃģ en unos dÃas.
Se presenta en forma de dolor agudo,
a veces importante e incluso con peritonismo,
en general unilateral,
ocasionalmente autolimitado.
Es frecuente que coexistan ambas situaciones (hemorragia y rotura).
Un quiste folicular con hemorragia intraquÃstica se manifiesta en la fase hiperaguda como un quiste de pared fina con contenido ecogÃĐnico formando una retÃcula.
Este patrÃģn,
que es diagnÃģstico,
se aprecia con mÃĄs facilidad con abordaje transvaginal.
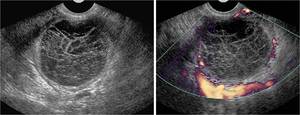
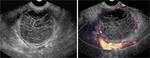
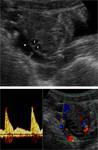
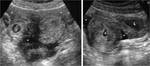
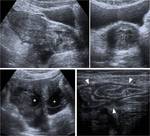
Fig. 3: Quiste folicular hemorrÃĄgico. En la ecografÃa transvaginal se aprecia una masa quÃstica ovÃĄrica de pared fina y escasamente vascularizada, conteniendo finos ecos que forman una retÃcula en la luz del quiste. Este patrÃģn es caracterÃstico de una hemorragia aguda intraquÃstica.
References: Cicchiello LA, Hamper UM, Scoutt LM. Ultrasound evaluation of gynecologic causes of pelvic pain. Obstet Gynecol Clin North Am. 2011;38:85-114.
MÃĄs adelante se produce progresivamente la retracciÃģn del coÃĄgulo,
que puede quedar en situaciÃģn gravitacional o adherido,
simulando una nodulaciÃģn mural,
aunque avascular (si bien no ha de confiarse ciegamente en la capacidad del doppler,
ni incluso con ajustes Ãģptimos,
para demostrar vascularizaciÃģn en nodulaciones en lesiones neoplÃĄsicas).
La RM puede demostrar el contenido hemorrÃĄgico subagudo con hiperintensidad de seÃąal tanto en T1 como en T2.
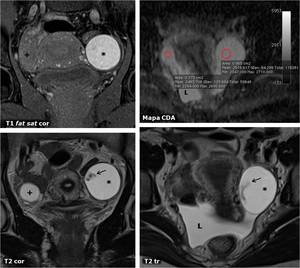
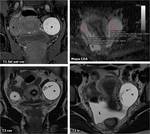
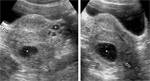
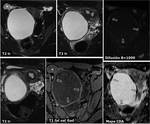
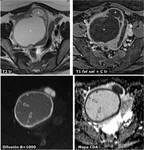
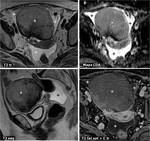
Fig. 4: Quiste folicular hemorrÃĄgico subagudo. Aproximadamente una semana despuÃĐs de un episodio de dolor agudo que se resolviÃģ parcialmente, se realizÃģ RM. En el ovario izquierdo hay una masa quÃstica de pared fina (*), cuyo contenido es hiperintenso tanto en T1 como en T2, con presencia de alguna nodulaciÃģn perifÃĐrica que no realzaba ni mostraba restricciÃģn de la difusiÃģn del agua (flechas). Este comportamiento es caracterÃstico de una hemorragia subaguda intraquÃstica, con presencia de coÃĄgulo retraÃdo y adherido a la pared. NÃģtese la diferencia de comportamiento con un folÃculo dominante contralateral (+), cuyo contenido muestra una seÃąal similar a la del agua. AdemÃĄs hay una cantidad discreta de lÃquido (L) en receso peritoneal de Douglas, probablemente por sumarse pequeÃąa rotura quÃstica junto con el sangrado.
Si se ha producido la rotura del quiste puede apreciarse su deformidad (por pÃĐrdida de tensiÃģn al vaciarse parcialmente) y lÃquido libre intraperitoneal adyacente.
El diagnÃģstico puede llegar a ser de exclusiÃģn cuando se descartan otras causas de dolor y solo se identifica algo de lÃquido tras vaciamiento completo del quiste,
o ni siquiera si el peritoneo lo ha reabsorbido.
En caso de hemorragia y rotura tanto el contenido del quiste como el lÃquido peritoneal pueden mostrar,
ademÃĄs de finos ecos,
densidades entre 25-100 UH.
El quiste luteÃnico complicado muestra paredes mÃĄs gruesas,
ecogÃĐnicas y vascularizadas,
en la segunda fase del ciclo o el primer trimestre del embarazo.
Los datos de hemorragia y rotura son similares.
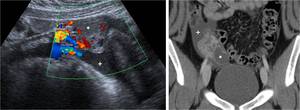
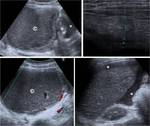
Fig. 5: Quiste luteÃnico roto y hemorrÃĄgico. Dolor agudo posovulatorio pÃĐlvico derecho, con signos de irritaciÃģn peritoneal. LesiÃģn quÃstica ovÃĄrica derecha (*) hendida, de pared algo mÃĄs gruesa y vascularizada, con contenido ecogÃĐnico y rodeada de lÃquido peritoneal (+) que tambiÃĐn contiene ecos y muestra una densidad de 40 UH, hemÃĄtico. El episodio se autolimitÃģ en unos dÃas.
2.2. ENDOMETRIOSIS
La endometriosis afecta hasta a un 10% de mujeres en edad fÃĐrtil.
La teorÃa etiopatogÃĐnica mÃĄs aceptada es la de la menstruaciÃģn retrÃģgrada.
En el 80% de los casos el tejido endometrial ectÃģpico estÃĄ en los ovarios,
donde puede desarrollarse como masas llamadas endometriomas,
que se manifiestan como masas complejas,
desde el llamado âquiste chocolateâ,
relleno por finos ecos,
hasta lesiones mixtas con ÃĄreas sÃģlidas,
mÃĄrgenes irregulares,
tabiques y adherencias,
que pueden similar enfermedad pÃĐlvica inflamatoria (EPI) o neoplasia.
La tÃĐcnica mÃĄs fidedigna para su diagnÃģstico es la RM,
con demostraciÃģn de focos hiperintensos en T1 que no se suprimen con saturaciÃģn espectral de la grasa y muestran hipointensidad en T2 (shading).
En general causa dolor pÃĐlvico crÃģnico cÃclico,
asociÃĄndose a infertilidad.
Sin embargo,
pueden presentarse en raras ocasiones de forma aguda en casos de rotura o sobreinfecciÃģn.
En estas pacientes es mÃĄs habitual la implicaciÃģn de la Escherichia coli como germen causante que en otros casos de EPI.
Solo el empleo de la RM podrÃĄ definir la existencia subyacente de una endometriosis en estos casos que,
por lo demÃĄs,
se comportan como indistinguibles de un absceso tubo-ovÃĄrico de otra causa.
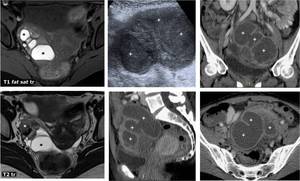
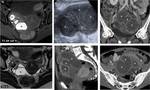
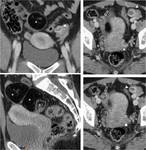
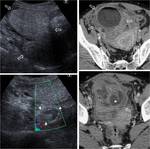
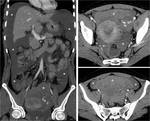
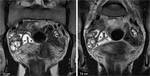
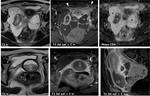
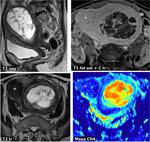
Fig. 6: Endometriosis y EPI. Mujer de 38 aÃąos. A la izquierda, estudio basal de RM. Se aprecia una masa ovÃĄrica derecha compleja, con loculaciones lÃquidas (*) hiperintensas en T1 con supresiÃģn grasa, algunas de las cuales son marcadamente hipointensas en T2, en relaciÃģn con sangrado de cronologÃas diversas. Este hallazgo es diagnÃģstico de endometriosis ovÃĄrica. Meses despuÃĐs la paciente acude con exacerbaciÃģn subaguda del dolor pÃĐlvico y fiebre. Tanto en ecografÃa como en TC se identifican estructuras tubulares tortuosas y plegadas (+), con contenido ecogÃĐnico y realce perifÃĐrico con el contraste, en relaciÃģn con piosÃĄlpinx bilateral y abscesos tubo-ovÃĄricos. Tras cirugÃa se comprobÃģ extenso absceso tubo-ovÃĄrico bilateral con focos de endometriosis ovÃĄrica y tubÃĄrica.
TambiÃĐn pueden darse la presentaciÃģn aguda de una endometriosis en forma de oclusiÃģn o suboclusiÃģn intestinal aguda o recidivante,
motivada por implantes subserosos intestinales que llegan a infiltrarse hasta capas relativamente profundas del sigma o del Ãleon pÃĐlvico y por adherencias asociadas a implantes peritoneales.
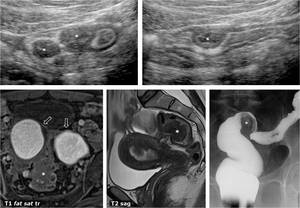
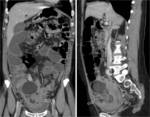
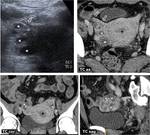
Fig. 7: PresentaciÃģn de endometriosis profunda con oclusiÃģn intestinal. Arriba, paciente joven con episodios repetidos de suboclusiÃģn intestinal. Se identifican varios nÃģdulos (*) en la pared de tramos de Ãleon pÃĐlvico, que anatomopatolÃģgicamente se demostrÃģ que correspondÃan a implantes endometriÃģsicos infiltrando hasta la capa muscular propia. Debajo a la izquierda, grandes masas ovÃĄricas bilaterales hiperintensas en T1 con supresiÃģn grasa (flechas), en relaciÃģn con endometriomas ovÃĄricos, y depÃģsito nodular posterior profundo (*), predominantemente hipointenso, pero con pequeÃąos focos de hiperintensidad en T1, improntando en la pared anterior del recto superior. En el centro, imagen potenciada en T2 en incidencia sagital que muestra la relaciÃģn entre este implante endometriÃģsico profundo, que presenta incluso un pedÃculo vascular, y el recto superior improntado. Esta mujer de 35 aÃąos presentaba tambiÃĐn crisis de soboclusiÃģn intestinal. Inferiormente y a la derecha, imagen de enema opaco en otra mujer con un implante endometriÃģsico profundo (*) en la pared del sigma distal.
Existe tambiÃĐn la posibilidad de uropatÃa obstructiva por implantes endometriÃģsicos profundos periureterales.
2.3. TORSIÃN ANEXIAL
Supone el 3% de las urgencias ginecolÃģgicas.
En todos los casos puede tratarse de una torsiÃģn completa o incompleta,
con mayor o menor grado de compromiso vascular en funciÃģn de la tensiÃģn sobre los vasos del pedÃculo torsionado.
En casos graves la viabilidad del ovario y/o la trompa puede estar comprometida si no se instaura un tratamiento rÃĄpido.
El compromiso vascular inicial suele ser venoso y linfÃĄtico,
siguiÃĐndose de detenciÃģn del flujo arterial.
La detecciÃģn de flujo arterial con doppler no descarta el diagnÃģstico,
por la dualidad del aporte arterial (desde arterias ovÃĄricas,
de la aorta,
y ramas de la hipogÃĄstrica) y la posibilidad de torsiÃģn incompleta.
Encontrar flujo arterial de alta resistencia es muy sugerente de torsiÃģn en un contexto clÃnico adecuado.
Hallazgos generales: anejo aumentado de tamaÃąo,
con estroma ovÃĄrico heterogÃĐneo (con ÃĄreas ecogÃĐnicas por hemorragia y otras hipoecogÃĐnicas por edema o necrosis),
en posiciÃģn anÃģmala,
con retracciÃģn uterina.
Es muy especÃfico el hallazgo del pedÃculo vascular torsionado ("signo del remolino",
quizÃĄ mÃĄs fÃĄcilmente identificable en la TC).
Si ademÃĄs no se detecta flujo en su interior,
es dato sugerente de torsiÃģn de alto grado,
como lo es la identificaciÃģn de aumento de densidad en la grasa perifÃĐrica.
Junto al pedÃculo torsionado puede verse la trompa interpuesta engrosada y dilatada.
Puede haber lÃquido libre.
En RM se ha descrito ademÃĄs una restricciÃģn moderada de la difusiÃģn del agua.
Cuando esta restricciÃģn es marcada debe sospecharse lesiÃģn neoplÃĄsica subyacente o absceso complicando el proceso.
2.3.1. TorsiÃģn ovÃĄrica espontÃĄnea
La torsiÃģn anexial sin existencia de una masa ovÃĄrica predisponente es mÃĄs frecuente en niÃąas y adolescentes,
con mayor hipermotilidad anexial.
TambiÃĐn puede verse en gestantes entre las 8-16 semanas.
Los hallazgos son los de un ovario aumentado de tamaÃąo,
coincidiendo con el lado de la clÃnica aguda,
con folÃculos desplazados a la periferia y con el resto de signos arriba mencionados.
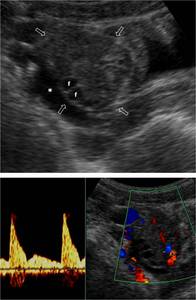
Fig. 8: TorsiÃģn ovÃĄrica sin lesiÃģn predisponente en niÃąa de 10 aÃąos. Dolor agudo centrado en FID de unas horas de evoluciÃģn. El ovario derecho (flechas) estÃĄ aumentado de tamaÃąo, con pequeÃąos folÃculos (f) desplazados perifÃĐricamente y estroma levemente heterogÃĐneo. En su interior se identifica flujo arterial de alta resistencia, lo cual no solo no descarta la existencia de torsiÃģn, sino que lo apoya. Hay una cantidad discreta de lÃquido peritoneal (*).
2.3.2. TorsiÃģn ovÃĄrica con lesiÃģn predisponente
Las que con mÃĄs frecuencia se asocian a torsiÃģn son lesiones benignas,
fundamentalmente quistes de entre 5-10 cm y teratomas ovÃĄricos.
Hasta un 15% de los teratomas se presentan clÃnicamente con torsiÃģn,
hasta el punto de que la apariciÃģn de dolor en una paciente con un teratoma conocido,
o la identificaciÃģn de un teratoma en una paciente con dolor deben hacer sospechar una complicaciÃģn de ÃĐste,
bien sea la torsiÃģn o la rotura.
Es mucho mÃĄs raro que la lesiÃģn subyacente sea maligna,
en cuyo caso la edad suele ser mayor.
Son mÃĄs frecuentes en el lado derecho.
A los hallazgos comentados de forma general se aÃąade el de la masa predisponente dentro del ovario,
con sus caracterÃsticas particulares.
Puede haber un cambio en ÃĐstas,
sobre todo en forma de cambio de posiciÃģn y engrosamiento de las paredes del quiste o el componente quÃstico del teratoma.
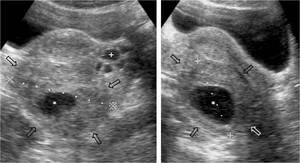
Fig. 9: TorsiÃģn ovÃĄrica derecha sobre quiste folicular. Aumento de tamaÃąo del ovario derecho (flechas), que estÃĄ en situaciÃģn retrouterina y presenta una lesiÃģn quÃstica de pared fina (*) y estroma predominantemente hiperecogÃĐnico. CompÃĄrese con el ovario izquierdo normal, con pequeÃąos folÃculos (+).
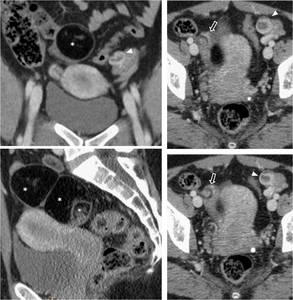
Fig. 10: TorsiÃģn ovÃĄrica derecha sobre teratoma quÃstico maduro. Mujer de 36 aÃąos con dolor hipogÃĄstrico de doce horas de evoluciÃģn. Masa multiquÃstica con contenido graso (*), situada a la derecha y sobre el Útero, en relaciÃģn con un teratoma, coincidente con el punto doloroso. Entre esta masa y el fundus uterino se ve el giro del pedÃculo vascular caracterÃstico de la torsiÃģn (flechas huecas). No hay datos de sospecha de necrosis ovÃĄrica (pedÃculo vascular permeable, ausencia de cambios en la grasa perifÃĐrica). La paciente se recuperÃģ de lo que probablemente fuera una torsiÃģn incompleta y fue intervenida de su teratoma un mes mÃĄs tarde. Hallazgo marginal: quiste lÚteo contralateral (cabezas de flecha).
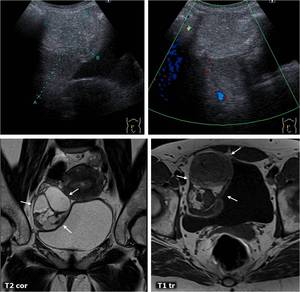
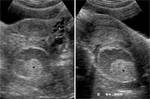
Fig. 11: TorsiÃģn anexial derecha sobre teratoma ovÃĄrico maduro. Estudio basal. Masa ecogÃĐnica en regiÃģn anexial derecha. En la RM se comprueba la existencia de ÃĄreas quÃsticas, algunas de ellas con hiperintensidad en T1. La paciente estÃĄ inicialmente asintomÃĄtica.
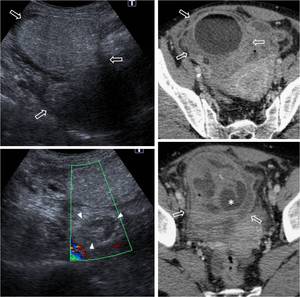
Fig. 12: TorsiÃģn anexial derecha sobre teratoma ovÃĄrico maduro. La misma paciente que en la figura anterior acude tres meses despuÃĐs a urgencias con dolor abdominal intenso y generalizado, sobre todo focalizado en FID, con peritonismo y signos clÃnicos de suboclusiÃģn intestinal. EcogrÃĄficamente se identifica la masa anexial conocida (flechas huecas), pero con una pared externa mÃĄs gruesa y rodeada de cambios inflamatorios. AdemÃĄs, entre ella y el Útero se ve una imagen de pedÃculo torsionado sin flujo. En la TC se aprecia la masa (flechas huecas), con presencia de grasa emulsionada y sobrenadante en el componente quÃstico, rodeada de una pared engrosada y de grasa con densidad aumentada. En la parte inferior se interpone la trompa ipsilateral dilatada (*). La presencia de un pedÃculo vascular torsionado sin flujo y los cambios en la grasa perifÃĐrica sugieren ausencia de viabilidad ovÃĄrica, que se comprobÃģ quirÚrgica y anatomopatolÃģgicamente.
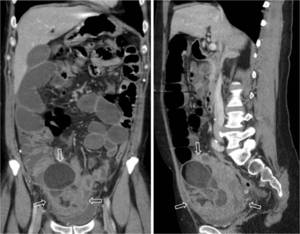
Fig. 13: TorsiÃģn anexial derecha sobre teratoma ovÃĄrico maduro. La misma paciente que en la figura anterior. ExistÃa ademÃĄs dilataciÃģn intestinal hasta el Ãleon terminal, probablemente por intenso Ãleo adinÃĄmico.
2.3.3. TorsiÃģn tubÃĄrica aislada
Es excepcional la torsiÃģn de la trompa sin participaciÃģn del ovario,
estimÃĄndose su incidencia en 1/1,5 millones de mujeres al aÃąo.
Como la torsiÃģn espontÃĄnea ovÃĄrica,
es mÃĄs frecuente en adolescentes.
Se identifica en la regiÃģn dolorosa una estructura tubular plegada sobre un eje ecogÃĐnico y tumefacto central o excÃĐntrico,
que corresponde al mesosÃĄlpinx,
en general sin detecciÃģn de flujo en su interior.
Para poder realizar el diagnÃģstico preciso debe verse el ovario normal ajeno a esta estructura.
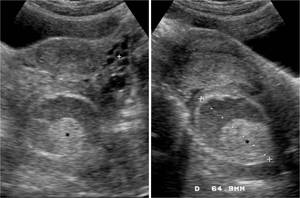
Fig. 14: TorsiÃģn tubÃĄrica aislada. EcografÃa transabdominal en cortes transversal (izquierda) y longitudinal (derecha). Masa retrouterina en una mujer de 13 aÃąos con intenso dolor hipogÃĄstrico de inicio sÚbito. La masa estÃĄ compuesta por una estructura tubular con contenido lÃquido con ecos y un centro sÃģlido ecogÃĐnico (*), que en la cirugÃa correspondieron a la trompa dilatada y ocupada por sangre, torsionada en torno a su meso. En la imagen transversal se ve un ovario izquierdo con pequeÃąos folÃculos (+).
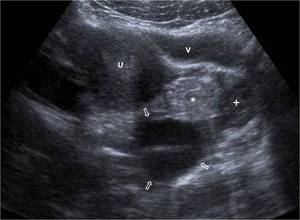
Fig. 15: TorsiÃģn tubÃĄrica aislada. Mujer de 15 aÃąos con dolor sÚbito e intenso en el lado izquierdo de la pelvis. EcografÃa transabdominal en corte transversal. Estructura plegada con contenido lÃquido (flechas huecas) y, mÃĄs anterior, otra estructura sÃģlida ecogÃĐnica (*). Por fuera de ellas estÃĄ el ovario ipsilateral, de aspecto normal (+) y por delante parte del ligamento ancho. U: Útero. V: vejiga. En la cirugÃa se identificÃģ una trompa dilatada y ocupada por sangre, torsionada de forma aislada con su meso en situaciÃģn excÃĐntrica. El ovario era normal.
2.3.4. TorsiÃģn de quiste paraovÃĄrico
Los quistes paraovÃĄricos constituyen hasta el 10-20% de las masas anexiales.
Son lesiones quÃsticas de mesotelio pÃĐlvico o de tejido paramesonÃĐfrico,
en general uniloculares y de pared fina.
Pueden diagnosticarse cuando se identifican claramente como ajenos a ambos ovarios.
No responden a estÃmulos hormonales y por lo tanto permanecen estables.
Pueden presentarse de forma aguda tanto por su rotura como por su torsiÃģn,
manifestÃĄndose con dolor.
En un caso que diagnosticamos mediante RM y que se comprobÃģ tras cirugÃa identificamos lÃquido libre y una clara restricciÃģn de la difusiÃģn del agua en la pared del quiste,
aunque aÚn fina.
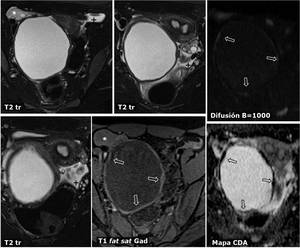
Fig. 16: TorsiÃģn de quiste paraovÃĄrico. Mujer de 15 aÃąos con dolor agudo en FID. En RM se encuentra una masa quÃstica de pared fina que realza con el contraste y muestra restricciÃģn de la difusiÃģn del agua (flechas abiertas), manifestÃĄndose como hiperintensa en difusiÃģn con valores altos de B e hipointensas en el mapa de coeficiente de difusiÃģn aparente. Su contenido es puramente lÃquido, sin restricciÃģn de la difusiÃģn. Esta lesiÃģn estÃĄ por detrÃĄs y a la derecha de un Útero septado, y es ajena al ovario derecho, normal (*). Hay una pequeÃąa cantidad de lÃquido peritoneal (+). En la cirugÃa se confirmÃģ la sospecha de quiste paraovÃĄrico torsionado, con su pared congestiva y con infiltrado hemorrÃĄgico en el estudio patolÃģgico.
2.4. ROTURA DE GESTACIÃN ECTÃPICA
Tiene una incidencia aproximada de un 2% y es responsable del 9% de las muertes maternales.
Se presenta con dolor agudo y sangrado en el primer trimestre de una gestaciÃģn,
conocida o no.
Salvo inestabilidad hemodinÃĄmica debe confirmarse antes de someterse a pruebas de imagen si la paciente estÃĄ embarazada,
en cuyo caso las alternativas diagnÃģsticas son el embarazo normal (a veces la implantaciÃģn es dolorosa y puede acompaÃąarse de sangrado),
el aborto espontÃĄneo y el embarazo molar.
Se trata de una situaciÃģn que en la mayor parte de los entornos es manejada por los ginecÃģlogos.
Asà y todo,
puede haber excepciones en las que el radiÃģlogo deba enfrentarse a un reto no habitual.
Aumentan su riesgo: gestaciÃģn ectÃģpica previa,
enfermedad tubÃĄrica,
portar un DIU,
antecedente de EPI y tratamiento de infertilidad (con incidencia de hasta un 5%).
Por orden descendente de frecuencia,
las posibles localizaciones de un embarazo ectÃģpico son: tramo ampular de la trompa (75-80%),
istmo tubÃĄrico (10%),
fimbrias (5%),
intersticial o cornual (2-4%).
Es excepcional en otras localizaciones: abdominal (donde en ocasiones puede llegar a tÃĐrmino,
aunque con grandes riesgos),
cervical,
cicatricial y ovÃĄrica (0,5%).
En casos de rotura el cuadro clÃnico puede ser grave,
incluso con inestabilidad hemodinÃĄmica,
en cuyo caso puede ser necesario prescindir de la confirmaciÃģn del embarazo para estudiar a la paciente o hasta de diagnÃģstico de imagen para tratarla quirÚrgicamente.
En estos casos a los signos de gestaciÃģn ectÃģpica que se describen debajo se suma el hallazgo del hemoperitoneo en mayor o menor cuantÃa,
y en ocasiones con demostraciÃģn del sangrado activo.
El tratamiento,
que puede ir desde la observaciÃģn estrecha hasta la cirugÃa abierta,
pasando por el metrotrexate intramuscular,
las inyecciones percutÃĄneas en el saco gestacional o la cirugÃa laparoscÃģpica,
tiende a ser lo mÃĄs conservador posible en tÃĐrminos de repercusiÃģn en fertilidad,
morbilidad y econÃģmicos.
El endometrio en el embarazo ectÃģpico
El signo mÃĄs precoz de embarazo intrauterino (4,5 semanas) es el signo intradecidual: pequeÃąa colecciÃģn lÃquida excÃĐntrica con anillo ecogÃĐnico.
A las 5 semanas se ve el signo del doble saco decidual,
mÃĄs especÃfico de embarazo intrauterino,
y a las 5,5 semanas el saco vitelino dentro del saco gestacional.
La identificaciÃģn de alguno de estos signos,
o incluso de un embriÃģn intraÚtero,
sin embargo,
no descarta completamente la posibilidad de embarazo extrauterino coincidente (gestaciÃģn heterotÃģpica).
Se trata de una situaciÃģn excepcional (1/30000 embarazos),
no tanto en tratamientos de inducciÃģn de la ovulaciÃģn.
En el endometrio de una mujer con una gestaciÃģn ectÃģpica pueden verse quistes deciduales,
que tambiÃĐn pueden aparecer en embarazos normales,
a menudo mÚltiples,
de pared fina (lo que los diferencia del signo intradecidual o el doble saco decidual) y situados entre endo y miometrio.
TambiÃĐn puede verse un seudosaco gestacional,
que consiste en una colecciÃģn lÃquida central (en la propia luz endometrial),
correspondiente a sangre o detritus,
a veces mÃģvil.
El ovario en el embarazo ectÃģpico
Dentro del ovario,
aunque a veces exofÃtico,
puede verse un quiste lÚteo,
cuya pared puede ser relativamente gruesa e hiperecogÃĐnica,
pero siempre menos que la de un saco gestacional.
En casos en que se planteen dudas es de gran importancia confirmar la dependencia ovÃĄrica de la lesiÃģn (para lo que puede ser Útil una exploraciÃģn bimanual que confirme el movimiento simultÃĄneo entre la lesiÃģn y el ovario),
pues la situaciÃģn de embarazo ectÃģpico ovÃĄrico es ciertamente excepcional.
La trompa en el embarazo ectÃģpico
El hallazgo de un saco gestacional con un embriÃģn vivo en la trompa es 100% especÃfico de embarazo ectÃģpico,
pero es infrecuente.
Le sigue en especificidad el hallazgo de un anillo tubÃĄrico con embriÃģn y saco vitelino,
sÃģlo con saco vitelino y sÃģlo de un anillo tubÃĄrico.
En este Último caso es vital confirmar que la lesiÃģn es ajena al ovario.
Hasta en 1/3 de los casos la implantaciÃģn tubÃĄrica se produce en la trompa opuesta al ovario con el cuerpo lÚteo.
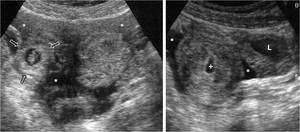
Fig. 17: GestaciÃģn ectÃģpica tubÃĄrica rota. Anillo tubÃĄrico derecho (flechas huecas) con embriÃģn vivo en su interior (especificidad del 100% de embarazo ectÃģpico). Hemoperitoneo abundante (*), sobre todo regional. El Útero presenta un pequeÃąo seudosaco gestacional (+) en el centro de la luz endometrial. El ovario contralateral contiene un quiste lÚteo (L), con una pared menos gruesa y ecogÃĐnica que la del saco gestacional ectÃģpico.
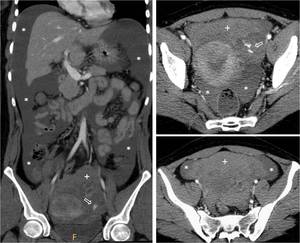
Fig. 18: GestaciÃģn ectÃģpica rota. Mujer de 34 aÃąos. Acude con dolor y distensiÃģn abdominal e hipotensiÃģn. Ante la gravedad clÃnica se realiza TC sin contar con prueba de embarazo. Se aprecia un hemoperitoneo masivo (*), con focos de coÃĄgulo centinela en la pelvis (+), con densidades en torno a 100 UH. En la regiÃģn anexial izquierda hay un foco de extravasaciÃģn activa del sangrado. Se sugiere probable gestaciÃģn ectÃģpica tubÃĄrica izquierda rota y con abundante sangrado, que se comprueba en cirugÃa urgente.
2.5. ENFERMEDAD PÃLVICA INFLAMATORIA
En general se adquiere por vÃa ascendente y se considera de transmisiÃģn sexual,
pero a veces puede producirse por vÃa hematÃģgena o por contigÞidad.
Los gÃĐrmenes implicados en 2/3 de los casos son la Neisseria gonorrhoeae y la Chlamydia trachomatis,
aunque no es raro que se trate de infecciones polimicrobianas.
Supone el 24% de las visitas de urgencia a ginecologÃa,
aunque la situaciÃģn raramente es de emergencia.
ClÃnicamente se manifiesta con dolor,
que se exacerba a la movilizaciÃģn cervical,
con o sin exudado vaginal maloliente.
La clÃnica suele iniciarse 7-10 dÃas tras la menstruaciÃģn.
En general el primer paso es el de la cervicitis,
que no tiene traducciÃģn radiolÃģgica.
Sucesivamente la infecciÃģn puede pasar por las fases que se relatan a continuaciÃģn.
2.5.1. Endometritis
Engrosamiento endometrial,
con mala definiciÃģn de los lÃmites entre endometrio y miometrio,
y a veces de los propios mÃĄrgenes uterinos.
En ecografÃa hay engrosamiento heterogÃĐneo de la banda endometrial,
con focos ecogÃĐnicos en su interior que pueden representar gas o detritus,
y aumento de vascularizaciÃģn.
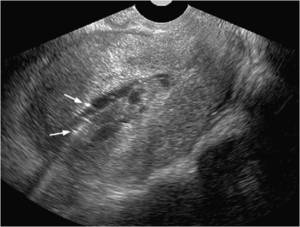
Fig. 19: Endometritis. EcografÃa endovaginal. Fiebre y exudado vaginal. DilataciÃģn de la luz endometrial y ocupaciÃģn por material heterogÃĐneo, incluyendo dos focos ecogÃĐnicos (flechas) correspondientes a burbujas de gas.
References: Cicchiello LA, Hamper UM, Scoutt LM. Ultrasound evaluation of gynecologic causes of pelvic pain. Obstet Gynecol Clin North Am. 2011;38:85-114.
2.5.2. Salpingitis,
hidro-piosÃĄlpinx
DilataciÃģn de la trompa,
plegada sobre sà misma,
tortuosa,
aperistÃĄltica en ecografÃa,
con afilamiento de sus bordes.
El hidrosÃĄlpinx sin contenido purulento puede aparecer tambiÃĐn en ausencia de EPI,
por adherencias previas o endometriosis,
entre otras causas,
a veces con aspecto arrosariado.
Cuando contiene ecos finos o nivel,
o muestra realce aumentado,
puede hablarse de piosÃĄlpinx.
Es frecuente que la dilataciÃģn pueda ser importante,
con borramiento parcial de los pliegues tubÃĄricos que deja en las paredes unas caracterÃsticas protrusiones de pequeÃąo tamaÃąo hacia la luz,
que le confieren un aspecto descrito como âen rueda dentadaâ.
En RM hemos encontrado restricciÃģn de la difusiÃģn del agua en las paredes de la trompa y en estas plicas tubÃĄricas en casos de piosÃĄlpinx.
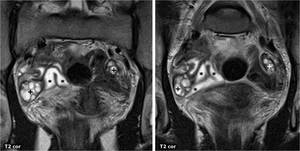
Fig. 20: HidrosÃĄlpinx sin enfermedad pÃĐlvica inflamatoria. DilataciÃģn tubÃĄrica con contenido lÃquido (*) en mujer asintomÃĄtica. +: ovarios normales.
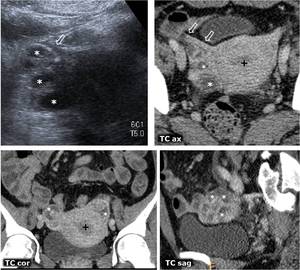
Fig. 21: Endometritis y piosÃĄlpinx. Mujer de 50 aÃąos con dolor hipogÃĄstrico, fiebre, exudado vaginal maloliente y leucocitosis. DilataciÃģn de ambas trompas (*), mÃĄs evidente en la derecha, muy plegada sobre sà misma y desplazando anteriormente el ligamento redondo (flechas huecas), con realce mural. Endometrio prominente y mal definido (+). PresentÃģ buena respuesta al tratamiento antibiÃģtico.
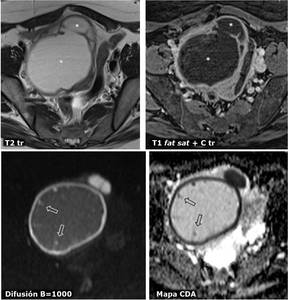
Fig. 22: PiosÃĄlpinx. Mujer de 49 aÃąos. Gran dilataciÃģn de una estructura tubular elongada con cambios de calibre, que corresponde a la trompa (*), con realce perifÃĐrico, especialmente del tramo ampular. Se aprecia marcada restricciÃģn de la difusiÃģn e la pared de la trompa y en las plicas parietales (flechas huecas): aspecto âen rueda dentadaâ. RequiriÃģ abordaje quirÚrgico por mala respuesta al tratamiento mÃĐdico.
2.5.3. Absceso tubo-ovÃĄrico
Masa compleja de forma irregular,
con paredes captantes y lÃquido de ecogenicidad variable en su interior,
que no siempre es fÃĄcil de delimitar del piosÃĄlpinx acompaÃąante,
en general bilateral.
Produce desplazamiento anterior de ligamentos anchos y redondos,
lo que permite en general su diagnÃģstico diferencial con abscesos pÃĐlvicos de otro origen,
sobre todo intestinal.
En todo caso,
la afectaciÃģn no siempre se circunscribe al ÃĄmbito ginecolÃģgico,
y puede acompaÃąarse de signos clÃnicos y de imagen de afectaciÃģn del peritoneo regional o a distancia (la afectaciÃģn del peritoneo perihepÃĄtico se denomina sÃndrome de Fitz-Hugh-Curtis).
La TCMD permite reconstrucciones multiplanares que pueden ser muy Útiles para definir la anatomÃa.
La RM es probablemente,
sin embargo,
la herramienta mÃĄs exacta para delimitar las peculiaridades de la afectaciÃģn.
Se ha descrito una restricciÃģn en la difusiÃģn del agua tanto en las paredes como en el contenido de los abscesos.
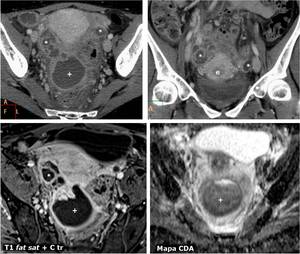
Fig. 23: Endometritis, piosÃĄlpinx y absceso tubo-ovÃĄrico. Mujer de 44 aÃąos. Endometrio mal definido (e), dilataciÃģn tubÃĄrica bilateral arrosariada con hiperrealce perifÃĐrico (*) y absceso en fondo de saco de Douglas (+), con restricciÃģn de la difusiÃģn del agua tanto en su pared como en su contenido purulento. MejorÃģ con antibiÃģticos, sin requerir cirugÃa.
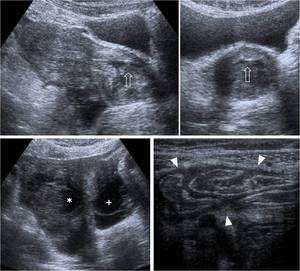
Fig. 24: Enfermedad pÃĐlvica inflamatoria secundaria a himen imperforado. Mujer de 16 aÃąos con tratamiento previo de himen imperforado, que acude con fiebre, dolor en hipogastrio y fosas iliacas. En ecografÃa se aprecia dilataciÃģn y ocupaciÃģn vaginal con material complejo que foma nivel (flecha hueca), dilataciÃģn tubÃĄrica (*) y colecciones lÃquidas retrouterinas, sospechosas de abscesos tubo-ovÃĄricos (+). AdemÃĄs hay engrosamiento difuso del peritoneo visceral en torno a tramos pÃĐlvicos de intestino delgado (puntas de flecha), que traduce cambios inflamatorios peritoneales regionales. Se realizÃģ retratamiento de la imperforaciÃģn del himen y terapia antibiÃģtica intensiva, con buen resultado.
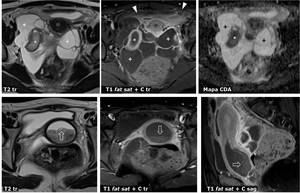
Fig. 25: Enfermedad pÃĐlvica inflamatoria secundaria a himen imperforado. Misma paciente que en la figura previa, estudiada por RM. DilataciÃģn vaginal con nivel lÃquido (flechas huecas), dilataciÃģn tubÃĄrica con paredes captantes y con restricciÃģn de la difusiÃģn del agua (*), colecciones lÃquidas retrouterinas con tabiques y paredes captantes (+), en relaciÃģn con abscesos tubo-ovÃĄricos. TambiÃĐn se ven los cambios inflamatorios regionales en el peritoneo visceral (puntas de flecha).
AdemÃĄs,
la RM es la Única herramienta diagnÃģstica de imagen que permite el diagnÃģstico fidedigno de endometriosis ovÃĄrica complicada o coexistente con enfermedad pÃĐlvica inflamatoria.
Como ya se comentÃģ antes,
la peculiaridad de la implicaciÃģn mÃĄs habitual de la Escherichia coli y diferencias epidemiolÃģgicas sugieren que es mÃĄs plausible la hipÃģtesis de la sobreinfecciÃģn que la de la coexistencia en la mayor parte de estos,
por otro lado,
infrecuentes casos.

Fig. 6: Endometriosis y EPI. Mujer de 38 aÃąos. A la izquierda, estudio basal de RM. Se aprecia una masa ovÃĄrica derecha compleja, con loculaciones lÃquidas (*) hiperintensas en T1 con supresiÃģn grasa, algunas de las cuales son marcadamente hipointensas en T2, en relaciÃģn con sangrado de cronologÃas diversas. Este hallazgo es diagnÃģstico de endometriosis ovÃĄrica. Meses despuÃĐs la paciente acude con exacerbaciÃģn subaguda del dolor pÃĐlvico y fiebre. Tanto en ecografÃa como en TC se identifican estructuras tubulares tortuosas y plegadas (+), con contenido ecogÃĐnico y realce perifÃĐrico con el contraste, en relaciÃģn con piosÃĄlpinx bilateral y abscesos tubo-ovÃĄricos. Tras cirugÃa se comprobÃģ extenso absceso tubo-ovÃĄrico bilateral con focos de endometriosis ovÃĄrica y tubÃĄrica.
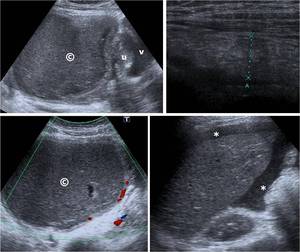
Fig. 26: Endometriosis infectada y peritonitis difusa. Mujer de 26 aÃąos con dolor abdominal, aumento del perÃmetro abdominal y masa palpable, afebril. Se identifica una gran masa quÃstica suprauterina con paredes gruesas y contenido ecogÃĐnico, que se acompaÃąa de ascitis abundante con finos ecos en su interior y cambios inflamatorios en el peritoneo visceral perihepÃĄtico (sÃndrome de Fitz-Hugh-Curtis) y en el epiplon mayor. En la cirugÃa se identifica una gran masa quÃstica con contenido purulento, dependiente del ovario derecho, rota, con gran cantidad de pus en la cavidad peritoneal y peritonitis difusa. La anatomÃa patolÃģgica de la masa ovÃĄrica demostrÃģ que se trataba de un gran endometrioma sobreinfectado.
2.6. SÃNDROME DE HIPERESTIMULACIÃN OVÃRICA
Puede verse en fases precoces del embarazo o en la fase lÚtea del ciclo en mujeres sometidas a tratamiento de inducciÃģn de la ovulaciÃģn.
Un 0,5-5% de los casos alcanzan cierta gravedad,
manifestÃĄndose con dolor,
que puede llegar a ser importante,
y datos de acumulaciÃģn de lÃquidos en tercer espacio (incluyendo ascitis y en ocasiones derrame pleural),
que puede degenerar en oliguria,
taquipnea e hipotensiÃģn.
Se aprecia un aumento de tamaÃąo de ambos ovarios,
con abundantes folÃculos dispersos y habitualmente ascitis.
TambiÃĐn estÃĄ incrementado el riesgo de torsiÃģn anexial,
por otro lado difÃcil de diagnosticar por el aspecto que de por sà presentan los ovarios en esta entidad.
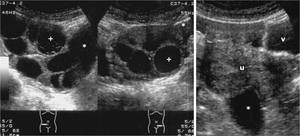
Fig. 27: SÃndrome de hiperestimulaciÃģn ovÃĄrica. Dolor hipogÃĄstrico relativamente intenso y progresivo en paciente sometida a tratamiento de inducciÃģn de la ovulaciÃģn. Aumento de tamaÃąo de ambos ovarios, con mÚltiples folÃculos de tamaÃąo considerable (+), algunos de los cuales contienen ecos en su interior, y acompaÃąados de ascitis (*).
2.7. SÃNDROME DE MEIGS O SEUDOMEIGS.
HIPERTENSIÃN ABDOMINAL Y SÃNDROME COMPARTIMENTAL ABDOMINAL
El sÃndrome de Meigs es la asociaciÃģn de un fibroma o fibrotecoma ovÃĄrico con ascitis y derrame pleural,
mientras que el seudosÃndrome es la asociaciÃģn de otros tumores ovÃĄricos benignos con ascitis y derrame pleural.
En estos casos y en otros en los que se dÃĐ un importante conflicto de espacio en la cavidad abdominal puede llegar a producirse una situaciÃģn de aumento de la presiÃģn abdominal (que incluso puede monitorizarse transvesicalmente),
con distensiÃģn y dolor,
que a su vez puede degenerar en el llamado sÃndrome compartimental abdominal,
que puede acompaÃąarse de fallo renal y multiorgÃĄnico.
Tanto ecografÃa como TC permiten una aproximaciÃģn adecuada a la naturaleza y la magnitud de la ocupaciÃģn abdominal.
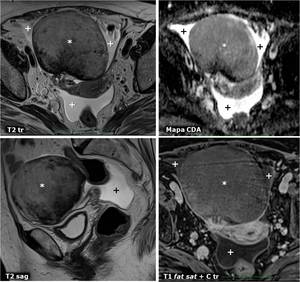
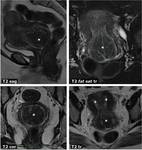
Fig. 28: SÃndrome de Meigs. Masa sÃģlida ovÃĄrica (*) con intensidad de seÃąal en general baja en T2, sin realce significativo con el contraste (estudio en fase tardÃa, en el que se aprecia realce lineal del peritoneo parietal pÃĐlvico) ni gran restricciÃģn de la difusiÃģn del agua, salvo en zonas donde la intensidad de seÃąal en T2 es mÃĄs baja. Se acompaÃąa de ascitis (+) y tambiÃĐn de discreto derrame pleural. El diagnÃģstico de confirmaciÃģn anatomopatolÃģgico fue de fibrotecoma ovÃĄrico. En este caso no habÃa sÃndrome de hipertensiÃģn abdominal, que puede ser el que se manifieste de forma aguda, siendo su extremo el sÃndrome compartimental abdominal.
3. CAUSAS UTERINAS
3.1. LEIOMIOMAS UTERINOS COMPLICADOS
Se estima que hasta un 40% de las mujeres mayores de 30 aÃąos tienen miomas uterinos.
Se trata de proliferaciones circunscritas de mÚsculo liso sensibles a la estimulaciÃģn estrogÃĐnica,
que por lo tanto no tienden a crecer tras la menopausia.
Su localizaciÃģn mÃĄs frecuente es intramural,
seguida de subserosa y submucosa.
Pueden presentarse de forma aguda con dolor cuando sufren degeneraciÃģn hemorrÃĄgica,
quÃstica o mixoide.
Esto puede suceder en circunstancias en que su crecimiento rebasa a la capacidad de aporte vascular,
por ejemplo,
en las primeras 10 semanas del embarazo.
AdemÃĄs del dolor es posible el sangrado o exudado vaginal y no es raro que se acompaÃąe de febrÃcula y leucocitosis.
RadiolÃģgicamente se identifica un foco mÃĄs o menos amplio e irregular de contenido lÃquido en el seno de una tumoraciÃģn sÃģlida que,
si se dispone de estudios previos,
habrÃĄ crecido notablemente en un corto margen de tiempo.
Si la lesiÃģn es submucosa puede acceder parte del contenido del ÃĄrea degenerada de la lesiÃģn hasta la luz endometrial,
cervical y vaginal.
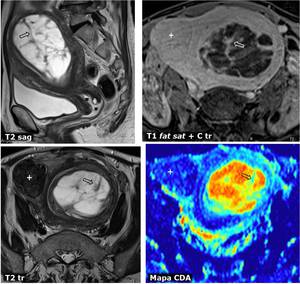
Fig. 29: Mioma uterino submucoso con degeneraciÃģn mixoide. Mujer de 55 aÃąos con dolor hipogÃĄstrico y exudado vaginal. En RM se aprecian varias formaciones nodulares uterinas sugerentes de miomas (+). La lesiÃģn de mayor tamaÃąo muestra contenido hiperintenso en T2, con tabiques que realzan (flechas huecas) y en los que la difusiÃģn del agua estÃĄ mÃĄs retringida, siempre mucho menos que en los miomas de aspecto mÃĄs habitual. Esta tumoraciÃģn desplaza el endometrio y en algÚn punto entra en contacto con ÃĐl. En la imagen sagital (arriba a la izquierda) se aprecia paso de parte del material mixoide del leiomioma submucoso al canal cervical y la vagina (*).
Otra posible complicaciÃģn aguda es la extrusiÃģn de un mioma uterino submucoso y pediculado,
que puede llegar a prolapsarse por el cÃĐrvix produciendo un compromiso de su aporte vascular y provocando su necrosis y posible sobreinfecciÃģn.
La clÃnica suele ser de dolor pÃĐlvico y menorragia,
sumÃĄndose a la evidencia de la masa transcervical.
Ãsta puede plantear dudas con el pÃģlipo endometrial,
aunque suele ser mÃĄs amplio y esfÃĐrico.
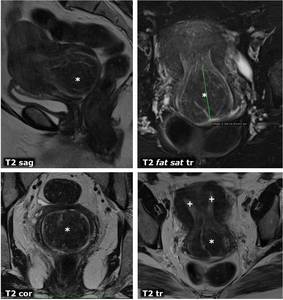
Fig. 30: Mioma uterino extruido. Mujer de 51 aÃąos con dolor hipogÃĄstrico, menorragia y protrusiÃģn de una masa sÃģlida por el exocÃĐrvix a la exploraciÃģn fÃsica. La RM muestra una masa sÃģlida hipointensa en T2 que se estÃĄ prolapsando por el canal cervical hasta la vagina (*). AdemÃĄs, Útero septado (+).
4. COMPLICACIONES PUERPERALES
En la mayor parte de los casos se diagnostican en el ÃĄmbito ginecolÃģgico,
quizÃĄ con la excepciÃģn de la trombosis de vena ovÃĄrica,
que se demuestra con mayor facilidad y fiabilidad mediante TC.
4.1. ENDOMETRITIS
Se manifiesta con dolor,
fiebre y exudado vaginal posparto.
Es mÃĄs frecuente tras cesÃĄrea,
parto largo o rotura precoz de membranas.
El diagnÃģstico suele ser clÃnico,
pues el Útero puerperal normal estÃĄ aumentado de tamaÃąo y muestra mala definiciÃģn de su endometrio,
incluso con presencia de gas hasta 3 semanas tras el parto.
4.2. RETENCIÃN DE PRODUCTOS DE LA GESTACIÃN
Manifestado con dolor y sangrado posparto,
con posibilidad de sobreinfecciÃģn y sepsis.
Puede persistir elevada la Ã-hCG.
EcogrÃĄficamente se identifica desde una banda endometrial de mÃĄs de 10 mm de grosor,
heterogÃĐnea,
con flujo âde aspecto trofoblÃĄsticoâ hasta una masa excÃĐntrica con claros restos placentarios y/o fetales.
4.3. ROTURA UTERINA
MÃĄs frecuente tras parto vaginal en una mujer con antecedente previo de cesÃĄrea.
Se identifica por la presencia de un defecto en la pared uterina con hemorragia intraluminal y hematoma perifÃĐrico.
4.4. TROMBOFLEBITIS DE VENAS OVÃRICAS
Se da en menos de un 2% de los casos,
casi siempre entre 2-10 dÃas tras el parto.
Es mÃĄs frecuente en el lado derecho (80-90%) y tras cesÃĄrea.
Se manifiesta con fiebre y dolor.
Puede complicarse con tromboembolismo pulmonar.
Puede alcanzarse el diagnÃģstico con ecografÃa,
pero la TC facilita su visualizaciÃģn.
Se aprecia un defecto de repleciÃģn,
que puede extenderse desde las venas anexiales periuterinas hasta la vena ovÃĄrica y su desembocadura en la cava inferior.
Puede acompaÃąarse de engrosamiento anexial edematoso.
Tiende a resolverse con cambios posflebÃticos,
en forma de circulaciÃģn colateral.
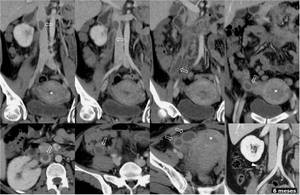
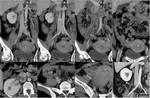
Fig. 31: Trombosis puerperal de vena ovÃĄrica derecha. Mujer de 31 aÃąos. DÃa 11 tras cesÃĄrea sin incidencias. Fiebre, dolor en FID y fosa renal derecha. La TC muestra defectos de repleciÃģn en la luz expandida de la vena ovÃĄrica derecha, hasta introducirse en su desembocadura en la cava inferior (flechas huecas). Endometrio prominente y mal definido (*), normal en el puerperio. A los seis meses se realiza otro estudio de TC por una apendicitis epiploica, apreciÃĄndose resoluciÃģn de la trombosis de vena ovÃĄrica derecha en forma de trayectos tortuosos paralelos.
BIBLIOGRAFÃA
- Coutinho A Jr,
Bittencourt LK,
Pires CE,
Junqueira F,
Lima CM,
Coutinho E,
et al.
MR imaging in deep pelvic endometriosis: a pictorial essay.
Radiographics.
2011;31:549-67.
- ChamiÃĐ LP,
Blasbalg R,
Pereira RM,
Warmbrand G,
Serafini PC.
Findings of pelvic endometriosis at transvaginalUS,
MR imaging,
and laparoscopy.
Radiographics.
2011;31:E77-100.
- Cicchiello LA,
Hamper UM,
Scoutt LM.
Ultrasound evaluation of gynecologic causes of pelvic pain.
Obstet Gynecol Clin North Am.
2011;38:85-114.
- Potter AW,
Chandrasekhar CA.USand CT evaluation of acute pelvic pain of gynecologic origin in nonpregnant premenopausal patients.
Radiographics.
2008;28:1645-59.
- Heverhagen JT,
Klose KJ.
MR imaging for acute lower abdominal and pelvic pain.
Radiographics.
2009;29:1781-96.
- Levine D.
Ectopic pregnancy.
Radiology.
2007;245:385-97.
- Cano Alonso R,
Borruel Nacenta S,
DÃez MartÃnez P,
MarÃa NI,
IbÃĄÃąez Sanz L,
ZabÃa GalÃndez E.
Role of multidetector CT in the management of acute female pelvic disease.
Emerg Radiol.
2009;16:453-72.
- Kim MY,
Rha SE,
Oh SN,
Jung SE,
Lee YJ,
Kim YS,
et al.
MR Imaging findings of hydrosalpinx: a comprehensive review.
Radiographics.
2009;29:495-507.
- Vandermeer FQ,
Wong-You-Cheong JJ.
Imaging of acute pelvic pain.
Clin Obstet Gynecol.
2009;52:2-20.
- Peparini N,
Di Matteo FM,
Silvestri A,
Caronna R,
Chirletti P.
Abdominal hypertension in Meigs' syndrome.
Eur J Surg Oncol.
2008;34:938-42.
- Hiller N,
Appelbaum L,
Simanovsky N,
Lev-Sagi A,
Aharoni D,Sella T.
CTfeatures of adnexal torsion.
AJR Am J Roentgenol.
2007;189:124-9.
- Nishino M,
Hayakawa K,
Iwasaku K,
Takasu K.
Magnetic resonance imaging findings in gynecologic emergencies.
J Comput Assist Tomogr.
2003;27:564-70.
- Kamaya A,
Shin L,
Chen B,
Desser TS.
Emergency gynecologic imaging.Semin Ultrasound CTMR.
2008;29:353-68.