Trasfondo
El cuerpo calloso es la comisura del prosencéfalo más prominente que se extiende por gran parte de los lóbulos frontal y parietal desde la comisura anterior rostralmente, hasta la comisura posteriormente. Está formado por fibras neuronales distribuidas topográficamente con diferentes calibres que interconectan las áreas homólogas de los hemisferios cerebrales.
El cuerpo calloso debe su nombre a su naturaleza compacta, y ello constituye una barrera para el flujo de edema intersticial y diseminación tumoral. De esta manera, sólolos tumores congénitos o agresivos pueden afectarlo (lipoma, glioblastoma multiforme, y linfoma). Esta característica también condiciona una mayor susceptibilidad para lesiones axonales agudas en los traumatismos craneales.
La composición de los axones mielinizados lo convierte en un blanco para las enfermedades desmielinizantes,
tanto primarias como la esclerosis múltiple y secundarias,
como la leucoencefalopatía multifocal progresiva (LMP) encefalomielitis diseminada aguda (ADEM),
o la enfermedad de Marchiafava-Bignami (EMB).
Por otra parte,
el cuerpo calloso es menos sensible a la isquemia ya que no está compuesto por materia gris,
de modo que los sucesos isquémicos son raros y suelen formar parte del territorio vascular en accidentes cerebrovasculares grandes vasos.
También se han descrito hemorragias en el cuerpo calloso.
Anomalías del desarrollo
Agenesia del cuerpo calloso
El cuerpo calloso (CC) empieza a desarrollarse alrededor de la 8º-12º semanas de gestación en la lámina reuniens de His en la región de la rodilla y progresa en dirección cráneo-caudal hasta el esplenio. La última parte es el desarrollo de el rostrum,
que finalmente cierra el sulcus medianus telencephali medii cerca de la 18º-20º semanas de gestación.
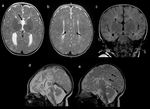
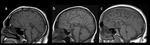
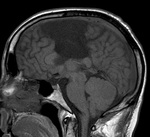
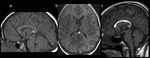
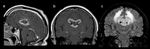
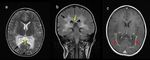
Dependiendo del tiempo de gestación en la cual se produce una noxa, las anomalías en el desarrollo de la CC pueden variar desde la agenesia completa ( Fig. 1 ) hasta diferentes grados de agenesia parcial ( Fig. 2 ). De esta forma,
la agenesia parcial implica a los elementos posteriores del CC, y la presencia de rostrum convierte esta posibilidad en improbable.
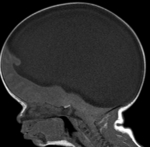
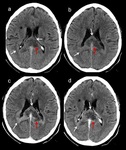
La holoprosencefalia ( Fig. 3 ) es una excepción a esta regla y suele conservar las partes posteriores de CC . Oba y Barkovich (1995) hipotetizaron que la presencia de fisura interhemisférica es necesaria para la formación del cuerpo calloso, y la presencia de un quiste dorsal en esta patología puede interferir en ella.
La agenesia del CC (ACC) se asocia comúnmente con colpocefalia y con haces de fibras atípicas (haces de Probst) que discurren paralelas y lateralmente a la cisura interhemisférica.
Informes actuales colocan la ACC en 1:4000 nacidos vivos y 3-5% de los pacientes quese habían sometido a una técnica de imagen debido a trastornos del neurodesarrollo.
La ACC se asocia a síndromes y malformaciones tales como el lipoma, el espectro Dandy-Walker , heterotopias, esquizencefalia ( Fig. 4 ), lisencefalia, malformación de Chiari II, síndrome de Aicardi (tríada de espasmos infantiles, ACC y lagunas coriorretinianas que son patognomónicas),
etc.
En imagen ( Fig. 1 ) se visualizan ventrículos laterales paralelos con las astas occipitalesa menudo dilatadas (colpocefalia) . En cortes coronales, las astas anteriores se disponen en forma de tridente, semejantes a un "casco vikingo" o "cabeza de alce" y los tractos de sustancia blanca compactos orientados longitudinalmente,
que son más brillantes que la mielina en otras localizaciones en T1WI constituyen los haces de Probst. Las circunvoluciones paramedianas están orientadas radialmente apuntando altercer ventrículo en las imágenes sagitales.
El diagnóstico diferencial debe establecerse con patologías que pueden conducir a la destrucción del cuerpo calloso (trauma, callosotomía), encefalopatía hipóxico-isquémica,
infartos y las enfermedades metabólicas como la enfermedad de Marchiafa-Bignami con necrosis.
Lipoma
Los lipomas pericallosos constituyen hasta un 65% de los lipomas intracraneales y se consideran lesiones del desarrollo del sistema nervioso central halladas en 2,500 de 25,000 autopsias. Pueden representar un hallazgo casual pero la asociación con convulsiones es frecuente (alrededor del 50%) y con frecuencia están asociados con anomalías del cuerpo calloso.
El diagnóstico se realiza con TC o RM que muestra una lesión redondeada u ovoide,
homogénea y bien definida con características de grasa (hipoatenuación en TC e hiperintensidad alto en T1 y T2 y con disminución de la señal en las secuencias con supresión grasa ) y ausencia de realce ( Fig. 5 ).
El diagnóstico diferencial incluye lesiones con componentes graso,
tales como grasa intracraneal en la hoz cerebral,
quistes dermoides,
teratomas y restos lipídicos de medios de contraste de mielografías anteriores hiperintensas en T1.
Neoplasias
Glioblastoma multiforme
El glioblastoma multiforme (GBM) (OMS astrocitoma de grado IV) es el tumor maligno primario más frecuente del cerebro, que representa el 12% -15% de todas las neoplasias intracraneales y el 50% de los astrocitomas. Por lo general se encuentran en la materia blanca supratentorial de los hemisferios cerebrales de los adultos entre 45 y 70 años de edad, y generalmente se propaga a través de extensión directa a través de tractos de sustancia blanca,
como el cuerpo calloso (dando la apariencia de mariposa clásica) para afectar al hemisferio contralateral.
Clínicamente,
los pacientes pueden presentar déficits neurológicos focales, por aumento de síntomas la presión intracraneal o convulsiones.
convencional con gadolinio La RM es la técnica estándar para la evaluación del glioblastoma y por lo general muestra una gran masa heterogénea,
con necrosis central,
hemorragia, con gruesos márgenes irregulares con realce y edema circundante ( Fig. 6 ).
El diagnóstico diferencial incluye linfoma primario del sistema nervioso central (SNC),
la toxoplasmosis en el SIDA y las metástasis (raro,
más frecuente como diseminación secundaria regional de un foco metastásico adyacente).
Linfoma
Los linfomas primarios del sistema nervioso central (LPSNC) son neoplasias raras agresivas del cerebroy representan sólo el 1% de los tumores del SNC malignos.
Aproximadamente el 2-6% de los pacientes con VIH desarrollarán LPSNC hecho que demuestra una fuerte asociación con el VIH / SIDA y los estados de inmunodepresión.
Son casi siempre de células B no Hodgkin tipo y las localizaciones más comunes sonel cuerpo calloso la sustancia blanca periventricular y la materia gris profunda.
El TC suele mostrar lesiones generalmente múltiples con alta atenuación y prácticamente todas las lesiones muestran realce homogéneo ( Fig. 7 ). En la RM,
las lesiones están claramente delineadas apareciendo isointensas - hipointensas en T1 y relativamente hipointensas en T2 con menos edema peritumoral que el GBM. En raras ocasiones se puede ver necrosis,
formación de quistes, calcificaciones y hemorragia.Es característica su "desvanecimiento" después de la administración de esteroides.
La toxoplasmosis en el SIDA, GBM y la encefalomielitis aguda diseminada (ADEM) se encuentran entre los diagnósticos diferenciales.
Trauma
Daño axonal difuso
El daño axonal difuso (DAI) es una consecuencia de la mayoría de las formas de lesión cerebral traumática, especialmente en resultado del cerebro moviéndose adelante y atrás en el cráneo como consecuencia de la aceleración o desaceleración rotacional.
Histológicamente,
el DAI se caracteriza por extensos daño en los axones en varias regiones del cerebro,
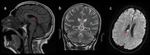
incluyendo la interfase sustancia gris-blanca de los hemisferios cerebrales, la cara dorsolateral del tronco cerebral rostral, y el cuerpo calloso (por lo general en el cuerpo posterior y esplenio).
El DAI clínicamente se presenta como pérdida de consciencia en el momento del accidente. En la TC se pueden observar focos de hemorragia,
pero la RM ( Fig. 8 ) es mucho más sensible para identificar lesiones tisulares,
como intensidades de señal elevadas en T2 y secuencias FLAIR. Después de 4 días, las lesiones hemorrágicas se visualizan mejor en T1 como focos hiperintensos, y T2 * es la mejor secuencia para buscar productos de degradación de hemoglobina crónicos. Las lesiones también se pueden clasificar como edema vasogénico, edema citotóxico o hemorragia central mediante Difusión. La espectroscopia por RM puede mostrar una lesión en el cerebro que parece normal en las imágenes y es útil para predecir el pronóstico a largo plazo.
El diagnóstico diferencial con los ictus debe basarse en la historia de trauma y ladistribución de las lesiones en el cuerpo calloso.
Enfermedades desmielinizantes inflamatorias
Esclerosis múltiple
La esclerosis múltiple (EM) es una enfermedad crónica y recurrente adquirida desmielinizante que afecta al sistema nervioso central y es,
por definición, diseminada en el espacio y también en el tiempo. La EM generalmente afecta a mujeres jóvenes con diferentes patrones longitudinales de la enfermedad. Los pacientes afectados pueden sufrir los síntomas motores o sensitivos,
incluyendo los nervios craneales.
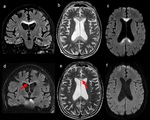
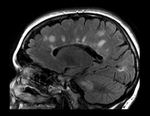
Las placas ( Fig. 9 ) suelen ser pequeñas y ovaladas, y se caracterizan por afectar a la sustancia blanca periventricular dispuestas perpendicularmente a los ventrículos laterales (dedos de Dawson),
cápsula interna,
cuerpo calloso y la interfase callososeptal (altamente sensible y específica para MS),
y puente. Las lesiones se pueden encontrar en cualquier parte de la sustancia blanca y mucho menos comúnmente en la materia gris. La afectación del cuerpo calloso en la resonancia magnética se ha reportado hasta en un 93%, y la atrofia puede coexistir en la EM delarga evolución. La TC es inespecífica,
pero en el escenario clínico apropiado, zonas típicas hipodensas en una distribución típica puede sugerir el diagnóstico. La RM constituye la técnica radiológica óptima para el diagnóstico y el seguimiento de la EM.
Las lesiones descritas son iso u hipointensas en T1, hiperintensas en FLAIR, T2 y las lesiones agudas pueden mostrar realce y difusión restringida.
El diagnóstico diferencial de las lesiones del cuerpo calloso se hace con otras enfermedades desmielinizantes como la MBD.
Leucoencefalopatía multifocal progresiva
La LMP es una enfermedad desmielinizante progresiva que resulta de los oligodendrocitos infectados por el virus JC en estados de inmunosupresión,
especialmente en el SIDA (prevalencia del 5% en las autopsias). LMP conduce a un declive progresivo neurológico que consiste en deterioro cognitivo, alteración del estado mental y cambios de personalidad que solía producir la muerte en el 90% de los casos en el plazo de 1 año sin tratamiento.
Las lesiones son típicamente confluentes,
bilaterales,
asimétricas, afectando la sustancia blanca supratentorial con frecuente afectación de las fibras subcorticales en U y en el pedúnculo cerebeloso medio,
pero las lesiones pueden ser unilaterales o únicas. Los sitios menos frecuentes de afectación son el cuerpo calloso, tronco encefálico,
cápsula interna y externa o la materia gris,
incluso en el tálamo y los ganglios basales.
En la TC,
las lesiones pueden ser vistas como áreas hipodensas en las regiones mencionadas,
que se muestran como hipointensas en T1 e hiperintensas en T2 y FLAIR. Comúnmente no hay realce,
pero realce periférico leve se puede ver o incluso aumentar tras la administración del tratamiento antirretroviral (síndrome inflamatorio de reconstitución inmune). En Difusión,
las lesiones agudas puede observarse un borde periférico incompleto de restricción, que representa infección activa.
El diagnóstico diferencial se hace con accidentes cerebrovasculares para las lesiones únicas, encefalopatía por VIH (distribución más simétrica) o incluso el linfoma o el GBM cuando se observa realce.
Encefalomielitis diseminada aguda
ADEM es una grave enfermedad inflamatoria desmielinizante monofásica de la sustancia blanca,
generalmente después de una infección viral o una vacunación.
Clínicamente se presenta con una aparición abrupta de déficits neurológicos multifocales inespecíficos que con frecuencia afecta a los niños,
sin embargo ADEM puede ocurrir en cualquier edad.
Las lesiones desmielinizantes están mal definidos,
son bilaterales, confluentes y asimétricas y suelen ubicarse en la sustancia blanca subcortical y central,
pero la participación de la interfase calloseptal es inusual. Al igual que otras lesiones desmielinizantes,
aparecen como áreas hipodensas en TC, hipointensas en T1 e hiperintensas en T2 y FLAIR. Los informes de realce con gadolinio son inconsistentes,
por lo que debe ser variable.
El diagnóstico diferencial más importante debe hacerse con la EM y ha habido muchos intentos para diferenciar ambas enfermedades mediante técnicas de imagen. Así,Brass et al. (2003) reportaron que la participación del cuerpo calloso y la sustancia blanca periventricular en los niños es más frecuente en la EM que en ADEM. Por otro lado,
se han utilizado técnicas tales como espectroscopía de protones, donde Sira et al. (2010) encontraron patrones específicos en ADEM (reducción de mioinositol en la fase aguda y sus cambios a a través del tiempo). Callen et al. (2009) además propuso criterios diagnósticos de EM en pacientes pediátricos con RM (dos de ausencia de un patrón de lesión difusa bilateral,
la presencia de agujeros negros, y la presencia de dos o más lesiones periventriculares). El diagnóstico diferencial puede incluir también el síndrome de Susac, una microangiopatía rara que afecta al cerebro,
la retina y la cóclea.
Enfermedades desmielinizantes metabólicas
Enfermedad de Marchiafava-Bignami
La EMB es una rara enfermedad tóxico-metabólica descrita en alcohólicos crónicos que conduce a la desmielinización primaria del cuerpo calloso. EMB aguda puedepresentar confusión mental,
desorientación, déficits neurocognitivos y convulsiones,
mientras que EMB crónica se caracteriza por demencia. Aunque la patogenia es desconocida, los agentes tóxicos presentes en el vino tino de baja calidad asociado a deficiencias de vitamina del complejo B se han postulado como posibles causas.
Histológicamente EMB incluye necrosis por capas,
degeneración en diferentes grados desde la preservación de los axones hasta la necrosis y cavitación quística. También ha sido descrita la afectación cortical como necrosis laminar cortical y gliosis,
principalmente en la tercera capa, asociado con las lesiones del cuerpo calloso, y probablemente secundaria a la misma.
La desmielinización EMB se visualiza como áreas de hipoatenuación en la TC,
hipointensidad en T1 e hiperintensidad en T2 y secuencias FLAIR, y afecta típicamente al cuerpo del cuerpo calloso,
seguido de la rodilla y,
finalmente, el esplenio. La desmielinización aguda puede asociar difusión restringida debido a edema citotóxico en la fase aguda. En la fase crónica,
el cuerpo calloso aparece atrófico y las lesiones pueden llegar a ser quísticas y bien delimitadas ( Fig. 10 ). Ocasionalmente puede ser reversible.
El diagnóstico diferencial radiológico incluye la esclerosis múltiple, daño axonal difuso y el infarto del cuerpo calloso.
Adrenoleucodistrofia ligada al X
La adrenoleucodistrofia ligada al cromosoma X (ALD) es un trastorno raro del metabolismo secundario a la disfunción de una enzima peroxisomal que conduce de ácidos grasos de cadena muy larga (AGCML) al depósito en el SNC,
las glándulas suprarrenales y los testículos. Se ha reportado una alta variación en la incidenciadesde1/20.000 hasta 1/200.000, y clásicamente afecta a varones jóvenes.
De acuerdo a la edad de inicio de los síntomas y los órganos involucrados, ALD ha sido clasificado en cerebral infantil ALD (37%), de la adolescencia ALD cerebral ligada al cromosoma X, adrenomieloneuropatía (32%), del adulto ALD cerebral ligada al cromosoma X,
enfermedad de Addison y asintomática.
El diagnóstico se realiza mediante el análisis AGCML en el suero,
pero la RM es una herramienta importante para detectar lesiones en el SNC precoces y diferenciar ALD cerebral de otras formas. Diferentes patrones de afectación se han descrito,
pero la clásica (y la más común) afecta a la sustancia blanca peritrigonal en los lóbulos parieto-occipital y esplenio del cuerpo calloso. En la RM,
estas áreas lesionales se visualizan como hipointensas en T1 e hiperintensas en T2 y FLAIR,
con un realce característico periférico que representa desmielinización inflamatoria activa ( Fig. 11 ).
El diagnóstico diferencial se puede hacer con leucodistrofia periventricular,
hipoglucemia neonatal,
enfermedad de la sustancia blanca con lactato, leucodistrofia metacromática y enfermedad de Alexander.
Enfermedad vascular
Infarto
Como se mencionó antes,
el cuerpo calloso es un tracto compactado de sustancia blanca,
por lo que es menos sensible a la lesión isquémica que la materia gris y por lo tanto, el infarto es poco frecuente.
El cuerpo calloso está irrigado principalmente por las arterias pericallosa anterior y posterior,
ramas de las arterias cerebrales anteriores y posteriores,
respectivamente.
También se han demostrado arterias subcallosas o medianas del cuerpo calloso que se originan en la arteria comunicante anterior. Las áreas centrales están irrigadas por arteriolas penetrantes cortas a diferencia del centro semioval y los ganglios basales,
que están irrigados por arterias largas. Por lo tanto,
el infarto lacunar del cuerpo calloso es raro y cuando se ve afectado por la isquemia,
es en el contexto de accidentes cerebrovasculares de grandes vasos formando parte del territorio tributario. Se ha reportado afectación cuerpo calloso en la arteriopatía cerebral autosómica dominante con infartos subcorticales y leucoencefalopatía (CADASIL) y en la arteritis de células gigantes. Epelman et al. (2011) también publicó afectación del cuerpo calloso en los recién nacidos con daño hipóxico-isquémico.
En imagen no difiere de lesiones isquémicas en otras regiones y se presentándose como lesiones hipodensas en TC, hipointensas en T1,
hiperintensas en T2 y FLAIR asociando restricción de la difusión en fase aguda.
El diagnóstico diferencial debe hacerse con infartos lacunares de otras entidades tales como trauma o procesos desmielinizantes basado en el grado de afectación, así en las lesiones isquémicas, todo el espesor del cuerpo calloso se ve afectado,
mientras que en las enfermedades desmielinizantes de la lesión se extiende en dirección caudo-craneal.
Hemorragia
La hemorragia en el cuerpo calloso puede ser secundaria a ruptura de un aneurisma de la arteria comunicante anterior,
de la arteria cerebral anterior de distal o a un sangrado por una malformación arteriovenosa del cuerpo calloso. Generalmente se asocian con hemorragia subaracnoidea o intraventricular,
y los estudios de imagen presentan las mismas características que la hemorragia en otras localizaciones.
Yatrogenia
Hemos repasado muchas enfermedades de diferentes etiologías que afectan al del CC,
pero se puede ver afectado además por otro tipo de patologías o tratamientos. De este modo,
podemos encontrar lesiones del CC en las enfermedades que no esperariamos,
y debemos ser conscientes de ellos para interpretarlas correctamente. En este contexto,
podemos distinguir las lesiones del CC secundarias a radioterapia, quimioterapia y por drenaje ventricular.
La necrosis cerebral inducida por terapia (NCT) es secundaria a la radioterapia con o sin quimioterapia,
que se asocian comúnmente como tratamiento neoadyuvante y como tratamiento paliativo en el SNC o tumores extra-SNC. Los factores de riesgo para el desarrollo de NCT son el método de administración de la radiación,
la dosis total,
tamaño de la fracción,
el volumen de tratamiento, edad del paciente y la quimioterapia concomitante.
Rogers et al. (2011) revisaron de forma retrospectiva 44 pacientes que se sometieron a este tipo de tratamiento y evaluaron los diferentes modelos de NCT histológicamente probada. De esta forma,
encontraron que tanto las lesiones corticales como de la sustancia blanca en NCT mostraban captación de contraste,
sobre todo en este último,
en la región periventricular / subependimaria y el cuerpo calloso. También reportaron que la morfología más frecuente de realce periférico fue en "frente de onda de propagación",
y en el realce interior fue en "queso suizo / pompas de jabón",
lo que representa el 93% de las lesiones con efecto de masa. Como todas las lesiones mostraron realce,
es importante diferenciar NCT de la recidiva,
ya que tienen un manejo terapéutico diferente.
Los pacientes con drenaje ventricular también pueden sufrir lesiones del CC después de la colocación del catéter,
aparte de los producidos por los daños directos. Lane et al. 2001 revisó reportes anteriores,
y también contribuyó con una serie de 9 pacientes y encontró que no había cambios en la señal (hiperintensidad en T2 e hipointensidad en T1) en la parte anterior y posterior del cuerpo en la hidrocefalia obstructiva de larga evolución después de la derivación. La hipótesis que presentaron es que estos cambios son secundarios a la compresión de larga duración en las fibras del CC contra la superficie inferior de la hoz. Estas lesiones no tienen repercusión clínica aparente.
Miscelánea
Lesiones focales reversibles
Las lesiones focales reversibles del esplenio,
recientemente llamada síndrome de lesión reversible del esplenio (RESLES) por García-Monco et al. (2008), se han hecho descrito en las crisis comiciales,
retirada de fármacos antiepilépticos, trastornos metabólicos (hipoglucemia o hipernatremia),
la encefalitis / encefalopatía por influenza,
edema cerebral de altitud,
meningitis estafilocócica, enfermedad del legionario, fiebre hemorrágica,
desnutrición, radioterapia y neoplasias como leucemia linfocítica aguda,
melanoma meníngeo espinal y el cáncer de esófago.
García-Monco et al. postula que RESLES es un síndrome distinto clinico-radiológico de etiología variada y de curso benigno,
excepto en aquellos pacientes con un trastorno subyacente grave, cuyos mecanismos aún no están claros.
RESLES presenta las mismas características en la RM en las diferentes patologías: hiperintensidad en T2 y FLAIR,
ligeramente hipointensa en T1 e hiperintensidad en difusión con bajo ADC.