1.-Epidemiología,
factores de riesgo y tipos de tumores.
La patología tiroidea es un problema clínico frecuente,
siendo la frecuencia de los nódulos palpables del 5% en mujeres y 1% en varones,
y en el que se aprecia una prevalencia en alza de las lesiones neoplásicas (aumento de 2.9 veces entre 1988 y 2002).
Este último aspecto se debe en gran medida al incremento en el uso de las exploraciones ecográficas que detectan nódulos tiroideos hasta en un 67% de la población.
Sin embargo las neoplasias tiroideas son poco frecuentes,
el 1% del total de las neoplasias, y aparecen en aproximadamente el 5-13% de los nódulos detectados por ecografía independientemente de su tamaño.
Así mismo algunos estudios han demostrado la presencia en autopsias de hasta un 6% de pequeños,
ocultos e indolentes,
focos de tumores papilares.
Lo cual es consistente y acorde con la historia y la evolución natural de las neoplasias papilares,
que son con mucho las más frecuentes,
y que en general presentan un lento desarrollo y elevados índices de supervivencia.
Los factores de riesgo conocidos para el desarrollo de tumores tiroideos,
y que hay que tener en cuenta de cara a estratificar la posibilidad de malignidad de los pacientes candidatos a realización de Paaf.-eco,
y determinadas formas de presentación clínica,
predicen una mayor probabilidad de malignidad.

Fig. 1: Factores predictores de malignidad para el desarrollo de tumores tiroideos
La mayoría de los nódulos tiroideos se corresponden con nódulos hiperplásicos de carácter benigno.
A continuación se muestra una tabla con las estirpes y tipos de tumoraciones malignas,
su frecuencia de distribución y sus índices de supervivencia.

Fig. 2: Tumores tiroideos: tipos, frecuencia de distribución, y supervivencia
2.-Características ecográficas de los nódulos tiroideos e indicaciones de realización de Eco-Paaf.
Un nódulo tiroideo es una lesión discreta que es diferente del resto del tejido que lo rodea,
y que puede ser palpable o no,
llegando en este último caso a su diagnóstico a través de US,
o incidentalmente mediante TC,
RM o PET-TC.
La enfermedad tiroidea puede ser nodular,
uni o multinodular,
o difusa debida a enfermedades de tipo Gaves-Basedow o Hashimoto,
pudiendo aparecer en estas últimas también patología de tipo nodular.
La obtención de material para estudio citológico guiada bajo control de US obtiene un mayor rendimiento que la punción directa,
siendo los que siguen los resultados de sensibilidad,
especificidad,
falsos positivos y falsos negativos de la misma.

Fig. 3: Resultados globales de los estudios citológicos de la Eco-Paaf
En los casos de enfermedad multinodular la elección del nódulo que debe ser aspirado depende de las diferentes características ecográficas de cada nódulo,
y no sólo de su tamaño.
De hecho el tamaño,
el número de nódulos y el intervalo de crecimiento no son características específicas.

Fig. 4: Características no específicas de los nódulos tiroideos
Ninguna de las características ecográficas por separado presenta una especificidad suficiente,
apreciándose un importante grado de solapamiento entre los nódulos benignos y malignos.
No obstante la combinación de varias de ellas predice una mayor posibilidad de malignidad.

Fig. 5: Características ecográficas de los nódulos tiroideos que predicen una mayor probabilidad de malignidad, especialmente la combinación de varias de ellas
Recientemente se ha propuesto el establecimiento de un sistema de estratificación de riesgo similar al que se utiliza en los estudios monográficos (Bi-rads),
atendiendo a la presencia de la suma de varias de las citadas características (Ti-rads).
Ilustramos los citados hallazgos con casos valorados en nuestro centro.
Cabe destacar una significativa mayor especificidad en los casos donde existen adenopatías o en los que se observa invasión o infiltración de estructuras vecinas,
así como la presencia de microcalcificaciones.
-2.1.
Presencia de adenopatías: es uno de los más específicos,
apareciendo en hasta el 19,4% de los tumores.
En los papilares se presentan en un 40% de los adultos y en el 90% de los casos infantiles.
Es raro en tumores foliculares y aparecen de forma temprana en los medulares.
Las características de alerta son las siguientes: El tamaño del eje corto mayor de 5 mm,
la pérdida de la morfología y del hilio graso,
los márgenes irregulares,
el aspecto heterogéneo,
la presencia de calcificaciones y de áreas quísticas,
y la vascularización intensa.
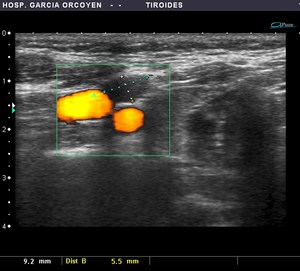
Fig. 6: Adenopatía contralateral en paciente con Ca. papilar: pérdida del hilio graso. Paaf positiva, tiroglobulina negativa. Confirmada tras IQ (23 ganglios bilaterales afectados)
- 2.2.
Invasión e infiltración de estructuras vecinas: es también un hallazgo muy específico.
La presencia de disnea,
disfonía,
molestias locales y disfagia son formas de presentación con alta sospecha diagnóstica,
que son más frecuentes en carcinomas anaplásicos,
linfomas y sarcomas.
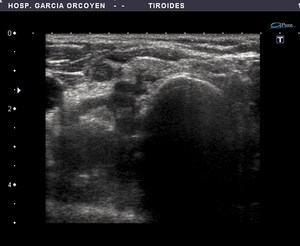
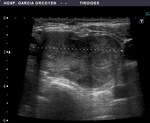
Fig. 7: Ca. anaplásico: debut clínico con disfonía. Lesión muy sólida, heterogenea, con infiltración de planos profundos y extensión a través de los bordes anterior y posterior de la cápsula. Se realizó Paaf y Tru-cut
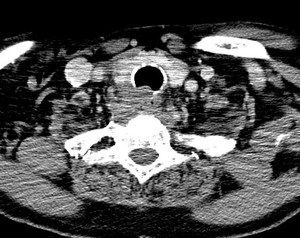
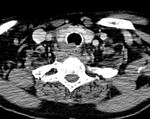
Fig. 8: Ca. anaplásico: CT, invasión de planos profundos
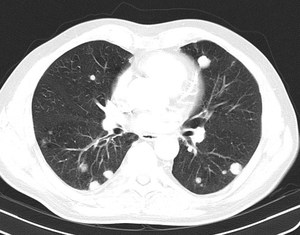
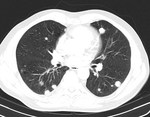
Fig. 9: Ca. anaplásico: CT, afectación metastásica pulmonar, suelta de globos
- 2.3.
Microcalcificaciones: Entre el resto de las características que se citan a continuación muestra una mayor especificidad,
85-95%,
con un valor predictivo positivo de 41-94%,
estando presentes en el 29-59% de los tumores,
sobretodo en papilares.
Aunque también se describen en foliculares,
anaplásicos,
adenomas,
y en tiroidopatía de Hashimoto.
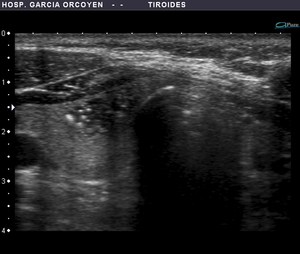
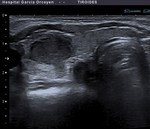
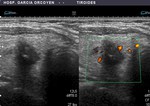
Fig. 10: Ca. papilar: nódulo sólido, mal delimitado, sin halo y con numerosas microcalcificaciones
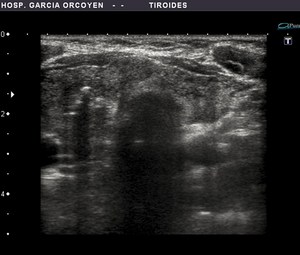
Fig. 11: Nódulo con microcalcificaciones: Paaf con resultado citológico de bocio adenomatoso
- 2.4.
Calcificaciones grandes o distróficas,
laminares,
y periféricas: son más frecuentes en el BMN,
aunque no excluyen malignidad.
Las groseras o amorfas pueden también estar presentes en ciertos tumores,
siendo más frecuentes en los medulares que en los tumores papilares.
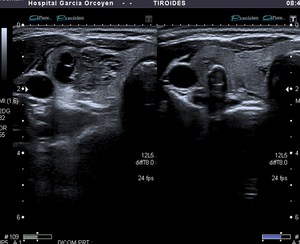
Fig. 12: Bocio coloide parcialmente quistificado y con calcificación grosera
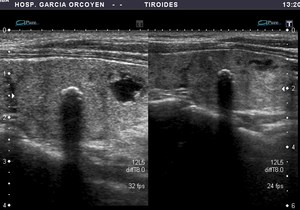
Fig. 13: Bocio coloide con calcificación laminar
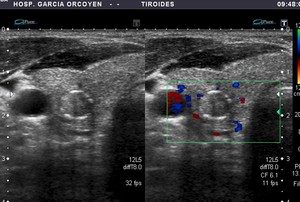
Fig. 14: Bocio coloide con calcificación periférica
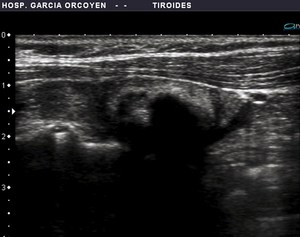
Fig. 15: Ca. medular: calcificación grosera
- 2.5.
Halo completo: es muy sugestivo de benignidad (especificidad del 95%) y traduce la formación de una pseudocápsula,
aunque puede estar ausente hasta en el 50% de los nódulos benignos.
Así mismo los tumores papilares pueden presentar halo completo o incompleto (10-24%).
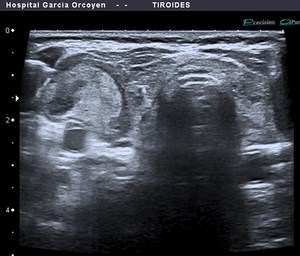
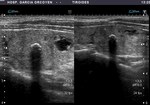
Fig. 16: Bocio adenomatoso: halo periférico grueso
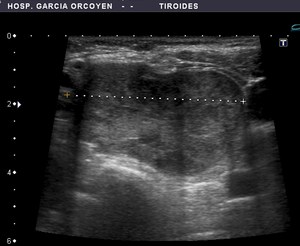
Fig. 17: Ca. papilar: ausencia de halo
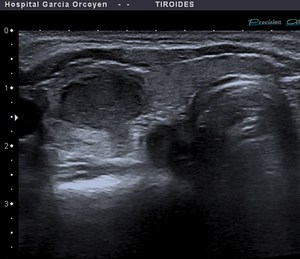
Fig. 18: Ca.folicular: halo irregular e incompleto (digitación tumoral a través de un área de interrupción del halo)
- 2.6.
Márgenes mal delimitados o irregulares: traducen infiltración en vez de formación de pseudocápsula,
aunque este hallazgo es poco fiable.
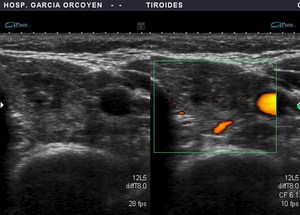
Fig. 19: Ca. papilar: márgenes irregulares y mal definidos. Presencia de microcalcificaciones
- 2.7.
Forma del nódulo: los nódulos que muestran un diámetro anteroposterior mayor que el trasverso se asocian a una mayor probabilidad de malignidad con una especificidad del 93%.
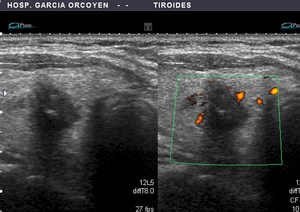
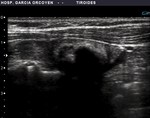
Fig. 20: Ca. papilar: diámetro anteroposterior mayor que el transverso. Muy sólido y marcadamente hipoecoico, con microcalcificaciones
- 2.8.
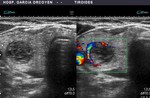
Vascularización: el tipo y la intensidad es otra de las consideraciones a tener en cuenta.
El 69-74% de los tumores muestran vascularización intrínseca o central.
Los nódulos benignos presentan con mayor frecuencia de vascularización de tipo periférico,
aunque esta última puede estar presente hasta en un 22% de los tumores malignos.
Es de destacar que la ausencia de vascularización indica una alta probabilidad de benignidad.
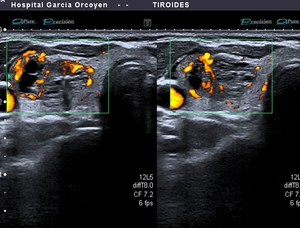
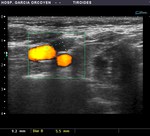
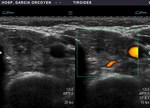
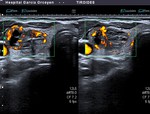
Fig. 21: Bocio coloide parcialmente quistificado con vascularización de predominio periférico
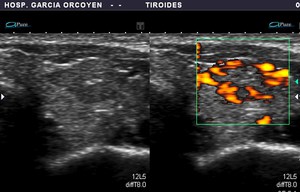
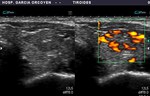
Fig. 22: Ca. papilar: vascularización de predominio periférico
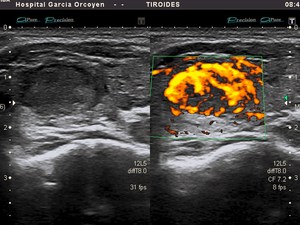
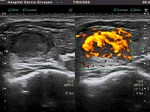
Fig. 23: Ca. folicular: vascularización intensa mixta
- 2.9.
La combinación de nódulo sólido y marcadamente hipoecoico muestra una sensibilidad del 87% y una especificidad del 15-27% (ver figura 20) .
-¿qué nódulo debe ser aspirado?-
En resumen,
la elección del nódulo es la clave para rentabilizar el procedimiento.
Además de las características más específicas ya citadas,
y de la presencia de adenopatías y/o la infiltración de estructuras vecinas,
estos son algunos de los patrones que resultan de gran ayuda para estratificar el posible riesgo de malignidad.

Fig. 24: Qué nódulo aspirar: patrones ecográficos sospechosos
-¿qué nódulo NO aspirar?-
A la hora de la realización del estudio ecográfico preliminar,
además de identificar las características que sugieren malignidad en cada nódulo,
que en ocasiones resulta difícil dado el solapamiento descrito,
puede resultar de gran ayuda la caracterización de los nódulos con claro aspecto de benignidad de manera que podamos excluirlos durante el proceso diagnóstico.
Algunas de las características de los nódulos tiroideos apoyan la presencia de benignidad correspondiéndose con alta probabilidad con nódulos hiperplásicos foliculares y confiriendo a los mismos un aspecto típicamente “coloideo”.

Fig. 25: Qué nódulo NO aspirar: patrones ecográficos benignos
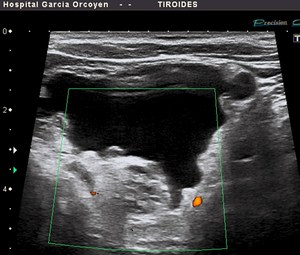
Fig. 26: Bocio coloide quistificado: deposito de coloide denso (área ecogenica declive, avascular)
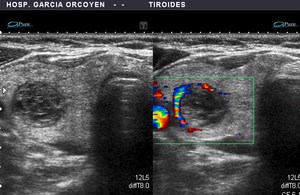
Fig. 27: Bocio coloide "espongiforme", con vascularización periférica
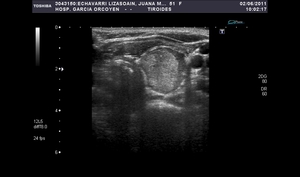
Fig. 28: Bocio coloide: nódulo hiperecogénico
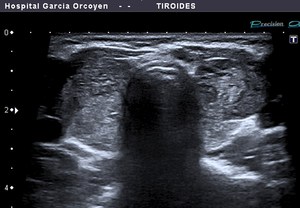
Fig. 29: Tiroiditis de Hashimoto: patrón en "jirafa". Septos hiperecogénicos entremezclados con áreas hipoecoicas
-Posibles dificultades en el diagnóstico y pitfalls -
Además del elevado indice de solapamiento entre las características que sugieren benignidad o malignidad en los nódulo tiroideos,
conviene tener en cuenta la presencia de polos sólidos vascularizados en los nódulos de predominio quístico.
También es importante la correcta identificación de las microcalcificaciones, considerar la posibilidad de tumores infiltrativos difusos (no nodulares),
y la presencia de adenopatías quistificadas o con calcificaciones,
o con diferentes características que el primario (típico de ca.
papilares).
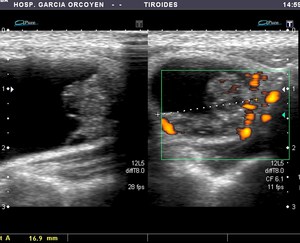
Fig. 30: Bocio coloide: Nódulo parcialmente quistificado con polo vascular
3-.Resultados citológicos: ¿cómo los interpretamos?
De ellos dependerá la actitud y el manejo subsiguiente del enfermo de cara a la planificación quirúrgica o al control clínico y radiológico,
tanto en la valoración de un nuevo estudio citológico en los casos en los que la muestra sea insuficiente,
o para determinar el control y seguimiento mediante US y/o la realización de un nuevo estudio en casos de crecimiento del nódulo.
Los resultados del procedimiento dependen en gran medida de la elección del nódulo y de la experiencia del operador,
así como del método de guía,
la visualización de la punta durante el procedimiento y el aspirado,
el calibre de la aguja,
la técnica de aspiración y la presencia o ausencia de citólogo in situ para corroborar la idoneidad de la muestra.
Los criterios establecidos para considerar las muestras citológicas como adecuadas son la presencia de al menos seis grupos de células foliculares que contienen cada una de 10-15 células y que han sido obtenidas mediante al menos dos aspirados de cada nódulo.
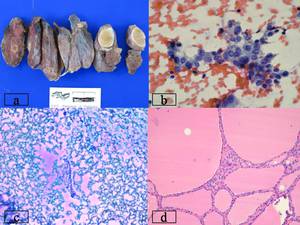
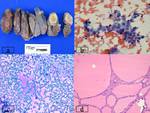
Fig. 31: a)Tiroidectomía total. En el nódulo tiroideo derecho , nódulo de 0,6 cm, encapsulado (carcinoma papilar), en el lóbulo tiroideo izquierdo zona superior nódulo de 1,8cm encapsulado de color pardo claro ( Carcinoma folicular bien diferenciado).
b)Extensión con grupo de células con núcleo claro con pseudoinclusión nuclear, algunas hendiduras. (Papanicolaou, x60)
c)Extensión con una placa de células foliculares de núcleos pequeños redondos, con coloide y hematíes en el fondo (Diff-Quick, x10)
d)Corte microscópico de tiroides normal. Folículos de diferentes tamaños con células pequeñas y coloide en su interior (H-E, x20)
El informe citológico,
además de determinar la idoneidad de la muestra,
indica la presencia de hallazgos citológicos benignos,
sugestivos de lesión folicular de significado indeterminado,
sospechosos de malignidad,
o malignos.
Dichos resultados asocian la probabilidad de malignidad tras el procedimiento quirúrgico.
En caso de resultado de benignidad se realizará seguimiento ecgográfico durante 6-18 meses.
Sí el nódulo permanece estable tras este periodo se controlará por US durante 3-5 años,
y sí presenta crecimiento se procederá a la relización de nuevo estudio citológico.

Fig. 32: Informe citológico: categorías diagnósticas, relación con la probabilidad de malignidad, y actitud de seguimiento en caso de resultado citológico benigno
4.-Nuestra experiencia en la implantación del procedimiento en un hospital comarcal: evaluación preliminar tras 10 meses.
-Implantación y metodología-
Se procedió a implantar por parte del servicio de radiología del HGO,
que cuenta con 4 radiólogas,
el procedimiento de Paaf-eco en nuestro hospital comarcal (con 95 camas y que abarca una población de 63.498 habitantes),
animados por el tiempo de demora de las listas de espera y la posible mejora en el manejo de la patología tiroidea.
La puesta en marcha del procedimiento se llevó a cabo de acuerdo con la dirección del centro y el servicio de endocrinología de nuestro hospital,
y con el servicio de anatomía patológica del Complejo Hospitalario de Navarra,
centro terciario de referencia al que acudían anteriormente los pacientes y al que se remitirían las muestras.
Se estableció la realización de un número de estudios aproximado de 3 o 4 pacientes por semana,
lo que se adecuaba al número de pacientes en nuestra lista de espera inicial,
al número estimado de solicitudes habituales,
y a la disponibilidad de la sala y de radiólogo.
El procedimiento se lleva a cabo con el paciente en decúbito supino y con hiperextensión cervical,
utilizando como guía una sonda lineal de 8Mhz.
Tras una ecografía tiroidea y un rastreo de las cadenas laterocervicales,
elegimos el nódulo a puncionar,
lo cual se realiza mediante visualización directa y técnica de mano libre,
empleando aguja de 23 o 25 G.

Fig. 33: Planificación del procedimiento de Eco-Paaf
Al carecer de anatomopatólogo en nuestro centro procedemos de forma estándar a obtener tres aspirados,
que de forma electiva realizamos por capilaridad aunque en ocasiones,
si la muestra es aparentemente escasa,
aspiramos con ayuda de un soporte de pistola de tipo Cameco.

Fig. 34: Procedimiento Eco-Paaf: número y técnica de aspirado
Fig. 35: Técnica de visión directa ecográfica del procedimineto de punción y del proceso de aspirado por capilaridad
Tras cada aspirado se extienden las muestras en los portas,
procediendo a enviar la mitad de ellas en seco,
para la tinción de Giemsa-Diff-Quick,
y fijando la otra mitad con alcohol para tinción de Papanicolau (ambas se realizan y analizan en el servicio de anatomía patológica del CHN).
Fig. 36: Material utilizado en la Eco-Paaf
Los casos con diagnóstico de malignidad y los sospechosos de malignidad se presentan y discuten en el comité de patología tiroidea del Complejo Hospitalario de Navarra (compuesto por cirujanos,
patólogos,
endocrinólogos y radiólogos) de cara a su planteamiento quirúrgico-terapeútico.
-Problemas y mejoras-
Inicialmente enviábamos un mayor número de extensiones y la mitad de las muestras fijadas con un spray de base alcohólica,
pero la calidad resultaba deficiente llegando defectuosas o artefactadas al centro de referencia.
Por lo tanto ideamos un sistema de envío adecuado mediante cartuchos donde se introducen las muestras en seco y de cestillas con cierre que permiten la llegada correcta de las muestras sumergidas en alcohol.
En la actualidad enviamos 4 extensiones de cada pase y la jeringa que se usa en cada aspirado,
para optimizar cada estudio,
siguiendo las indicaciones del servicio de anatomía patológica de CHN.

Fig. 37: Sistema de envío: cartuchos para las muestras en seco y cestillas con alcohol
De esta manera se intenta compensar el hándicap que supone la imposibilidad de contar con citólogo in situ. Así mismo y de forma ocasional se remite líquido de aspirado de los nódulos quísticos y material para determinación de tiroglobulina.
-Resultados preliminares-
A lo largo de estos últimos diez meses se ha realizado Paaf bajo control de ultrasonidos en 85 nódulos,
75 pacientes,
3 Paaf de adenopatías sospechosas (una de ellas positiva para ca.
papilar)) y una biopsia tru- cut tiroidea (en un caso de ca.
anaplásico).

Fig. 38: Resultados globales obtenidos
Se han obtenido 72 muestras diagnósticas - válidas (84%) y 13 con resultado citológico de muestra inadecuada para el diagnóstico - insuficiente (16%).
Entre las muestras suficientes para el diagnóstico se informaron,
desde el servicio de anatomía patológica del Complejo Hospitalario de Navarra,
como sigue: 3 casos con citología compatible con malignidad (ca.
papilares),
5 sospechosos de malignidad (3 ca.
papilares,
1 ca.
anaplásico,
1 ca.
medular,
y 1 ca.
folicular),
8 casos de proliferación folicular de significado indeterminado,
y 56 casos con citologías benignas.
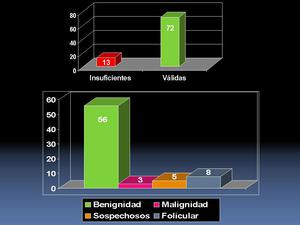
Fig. 39: Distribución de los resultados obtenidos
En total se han diagnosticado 9 nódulos malignos: 6 ca.
papilares,
un tumor anaplásico,
un ca.
medular y un ca.
folicular.
De las 3 paaf realizadas sobre adenopatías cervicales se confirmó la presencia de malignidad (en cadena laterocervical contralateral) en un caso de ca.
papilar,
aunque la determinación de tiroglobulina de la muestra resultó negativa.
Las otras 2 se realizaron sobre un paciente que tenía citología positiva de ca.
papilar siendo el resultado en ambos de linfadenitis inespecífica.
El único tru-cut realizado se llevó a cabo bajo control ecográfico directo y confirmó la presencia de ca.
anaplásico sobre el que se había realizado previamente estudio citológico (sospechosa de ca.
anaplásico).
Se ha apreciado una buena tolerancia de los pacientes durante la prueba,
no habiendose producido incidencias significativas durante o tras el procedimiento,
siendo sólo destacable algunos pequeños sangrados intraquísticos o subcapsulares,
autolimitados en todos los casos.