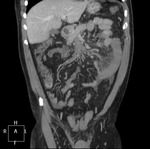
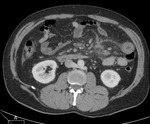
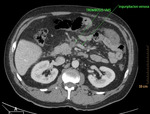
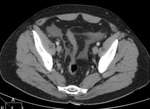
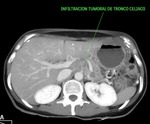
La isquemia intestinal aparece cuando el flujo sanguíneo del territorio mesentérico resulta insuficiente para satisfacer los requerimientos del intestino.
A diferencia de las formas crónicas en las que el desarrollo progresivo de colaterales impide la necrosis intestinal,
en las formas de instauración aguda,
la viabilidad del intestino puede quedar comprometida,
abocando a una situación de riesgo vital para el enfermo.
Es una causa infrecuente de abdomen agudo,
que representa una emergencia vascular potencialmente fatal,
con una alta tasa de morbi-mortalidad,
que requiere un diagnóstico precoz y una intervención rápida que permita restaurar el flujo sanguíneo mesentérico,
previniendo de esta forma la necrosis intestinal.
Se ha descrito una tasa de mortalidad del 50-90%1.
Dicha tasa elevada está directamente relacionada con el escaso tiempo que transcurre desde la disminución del flujo vascular a las asas intestinales y la instauración de la necrosis intestinal irreversible y con la forma de presentación clínica,
con síntomas inespecíficos y un examen físico relativamente anodino,
que conducen a un bajo índice de sospecha,
retrasando el diagnóstico.
ANATOMÍA Y FISIOLOGÍA DE LA CIRCULACIÓN VISCERAL:
El territorio esplácnico es perfundido a través de 3 vasos: el tronco celíaco (TC),
la arteria mesentérica superior (AMS) y la arteria mesentérica inferior (AMI),
que nacen en la cara anterior de la aorta a la altura de T12,
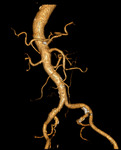
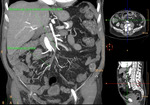
L1 y L3 respectivamente (Fig.1).
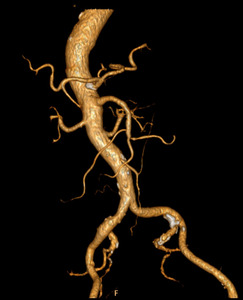
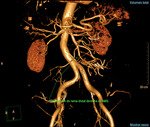
Fig. 1: Volume Rendering (VR) de aorta abdominal y sus ramas principales. Aorta elongada y tortuosa, de calibre normal, con placas ateromatosas calcificadas, destacando una de gran tamaño en la salida del tronco celíaco.
Existen conexiones anatómicas normales entre los tres troncos,
que cumplen un rol fundamental como fuente de flujo colateral ante la eventual oclusión de uno de ellos26.
Las vías colaterales más relevantes entre TC y AMS son las arcadas pancreático-duodenales.
Entre la AMS y la AMI son la arteria marginal de Drummond y la arcada de Riolano.
Entre la AMI y el territorio hipogástrico existen comunicaciones a través del plexo hemorroidal.
De los tres vasos,
el más importante es la AMS,
responsable de la irrigación de intestino delgado a partir del ángulo de Treitz y del colon hasta el ángulo esplénico.
El tronco celíaco se encarga de la irrigación del duodeno,
hígado,
páncreas y bazo y la AMI de la irrigación del colon desde el ángulo esplénico hasta el recto superior.
Las venas mesentéricas superior e inferior discurren paralelas a las arterias y drenan las respectivas partes del intestino.
La vena mesentérica inferior desemboca en la vena esplénica que se une a la vena mesentérica superior para formar la vena porta.
Las venas mesentéricas comparten numerosos vasos colaterales,
los cuales también mantienen varias conexiones con la circulación venosa sistémica.
Estas conexiones incluyen anastomosis con las venas esofágicas,
gástricas,
renales,
lumbares y pélvicas.
Los vasos entran en el tubo digestivo por el borde mesentérico.
Desde ese punto,
se distribuyen en forma circunferencial hacia el borde anti-mesentérico y luego atravesando la capa muscular se constituye un verdadero plexo en el plano submucoso,
que nutre la extensa superficie mucosa.
Hay que tener en cuenta,
que existen unas zonas de menor vascularización,
que corresponden a las áreas límites entre ambas circulaciones:
- Flexura esplénica.
- Unión íleo-cecal.
- Unión recto-sigma.
CLASIFICACIÓN ETIOLÓGICA DE LA ISQUEMIA MESENTÉRICA AGUDA (IMA):
1.-Oclusión arterial mesentérica: embólica o trombótica.
2.-Oclusión venosa mesentérica: trombosis.
Tiene mejor pronóstico que la arterial y se beneficia del tratamiento anticoagulante oral.
3.
Isquemia mesentérica no oclusiva: estados de bajo gasto cardíaco (producidos por infartos,
arritmias,
hipovolemia,
etc..).
4.-Otras causas infrecuentes: algunas vasculitis como la panarteritis nodosa,
lupus eritematoso,
etc.
1.-Isquemia mesentérica aguda de origen arterial
A) Embolia de la arteria mesentérica superior
Representa el 50% de las IMA.
La mayoría de los émbolos se localizan cercanos a una bifurcación o distales a la arteria cólica media,
mientras que los trombos se localizan cerca del origen de las arterias mesentéricas.
Las arritmias son el factor precipitante más común y con menor frecuencia la cardioversión y el cateterismo.
Un dolor abdominal de comienzo súbito en este contexto debería despertar la sospecha de embolia de la arteria mesentérica superior.
A menudo existe una historia previa o concomitante de embolismos en otras localizaciones.
Cuando el émbolo se aloja por encima de la bifurcación de la arteria ileocólica se denomina "embolia mayor" mientras que si se localiza por debajo de esta bifurcación se habla de "embolia menor"; distinción importante de cara al manejo terapéutico.
Factores predisponentes:
- Arritmias cardíacas
- Valvulopatías
- Infarto de miocardio
- Aneurisma de aorta torácico
Factores que afectan al grado de afectación intestinal:
- Proximal: Cuando la isquemia se instaura de forma brusca por un émbolo proximal tiene peor pronóstico que la de un émbolo localizado distalmente,
ya que aquél se relaciona con la extensión del intestino afectado.
- Distal: Cuando el émbolo afecta a segmentos distales de la AMS,
sobre todo distalmente a la arteria cólica media,
el intestino afectado es más corto y en algunos casos se observan segmentos aislados de afectación.
- Otros factores que influyen en la viabilidad del segmento intestinal afectado:
- La existencia de colaterales suficientes para mantener el flujo sanguíneo al asa intestinal afectada.
- El vasoespasmo favorecido por la acidosis metabólica.
Por ello,
el control de la acidosis es una de las medidas precoces más importantes para garantizar la viabilidad intestinal.
B) Trombosis de la arteria mesentérica superior
Representa el 20-30% de los casos de IMA y afecta a pacientes de edad avanzada con una marcada arteriosclerosis.
No es infrecuente que el enfermo refiera una historia de angina intestinal en las semanas o meses que preceden al episodio trombótico.
Debido a ello,
las arterias tienen disminuido el flujo y han desarrollado circulación colateral.
La trombosis suele ocurrir en la porción proximal de la AMS o del tronco celíaco y sus efectos suelen ser devastadores al afectar extensas áreas del intestino,
desde el duodeno hasta el colon transverso.
Por ello,
la trombosis aunque es menos frecuente que la embolia,
tiene peor pronóstico que ésta,
ya que,
a pesar de que la circulación colateral es capaz de mantener cierto flujo,
el territorio afectado es muy extenso.
Factores predisponentes:
- Arterioesclerosis
- Cardiopatía isquémica
- Estados de hipercoagulabilidad (déficit de antitrombina III,
déficit de proteínas S y C).
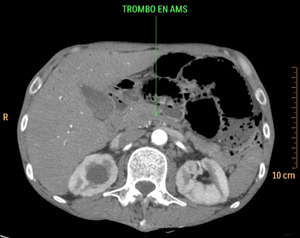
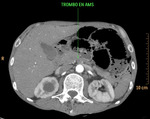
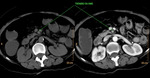
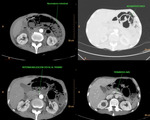
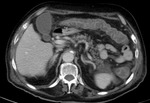
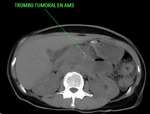
Fig. 2: Isquemia intestinal de causa oclusiva arterial trombótica. Se visualiza un defecto de repleción en los primeros centímetros de la AMS, compatible con trombosis. Esta imagen corresponde al paciente nº3 de la figura 18 y 19.
2.-Isquemia mesentérica aguda de origen venoso
Es una causa infrecuente,
que representa menos del 10% de los casos.
Ha de afectarse de forma muy severa el eje porto-esplénico-mesentérico e incluso en estos casos es excepcional que una trombosis venosa produzca un infarto intestinal agudo.
El pronóstico es mejor que el de la trombosis o embolia arterial.
Puede ser primaria (cuando se debe a un trastorno de la coagulación) o secundaria a hipertensión portal,
infección o puede asociarse con varios estados de hipercoagulabilidad (Fig. 3)4 .
Aunque la mayoría tienen factores predisponentes claros,
la sintomatología es inespecífica y la sospecha clínica es baja.
Cuando existe una oclusión venosa mesentérica,
la imposibilidad del retorno venoso produce edema y aumento de la presión venosa que cuando se iguala a la arterial produce isquemia e infarto hemorrágico.
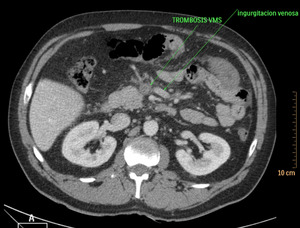
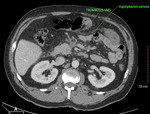
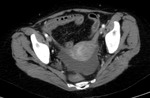
Fig. 4: Isquemia mesentérica aguda de causa oclusiva venosa trombótica. Defecto de repleción en vena mesentérica superior, que se encuentra aumentada de calibre, compatible con trombosis venosa. Esta imagen corresponde al paciente nº2 de la figura 13.
3.-Isquemia mesentérica no oclusiva (IMNO)
Es responsable del 20-30% de los episodios de IMA y surge como consecuencia del vasoespasmo originado por la liberación de sustancias vasoactivas en respuesta a una situación de bajo.
Es importante conocer que esta complicación puede no ser inmediata y aparecer horas o incluso días después de haber desaparecido el factor causal.
Factores predisponentes:
- Shock cardiogénico,
shock hipovolémico,
shock séptico.
- Arritmias; fallo cardíaco.
- Deshidratación,
stress.
- Cirugía reconstructiva de la aorta abdominal.
- IRC en hemodiálisis.
- Drogas (cocaína,
digoxina,
antihipertensivos).
- Feocromocitoma
Últimamente ha disminuido su incidencia debido a una mejor monitorización de los pacientes en las Unidades de Cuidados Intensivos y a la rápida corrección de las anomalías hemodinámicas.
4.-Mecánico:
Obstrucción en asa cerrada,
distensión pronunciada,
colitis isquémica por endoscopia o enemas.
( Fig. 26 ,
Fig. 27 Fig. 28 , Fig. 29 y Fig. 30)
5.-Inflamatorio:
Pancreatitis,
diverticultitis,
apendicitis,
peritonitis.
6.-Otras:
Irradiación,
traumatismos,
inmunosupresión,
quimioterapia, adyacente a tumores intestinales,
etc.
(Fig. 32 ,
Fig. 33 ,Fig. 34 ,
Fig. 35 y Fig. 36).
FISIOPATOLOGÍA
Al igual que en otras áreas de la economía,
el flujo sanguíneo del intestino está sujeto a mecanismos de autorregulación.
Al menos,
un 75% del flujo intestinal se distribuye a la mucosa y submucosa,
porciones de elevado requerimiento metabólico por sus funciones de absorción y excreción.
El resto del flujo corresponde a las túnicas musculares,
responsables de la propulsión del contenido intestinal.
Con independencia del mecanismo que desencadena la isquemia,
en todos los casos aparece una misma secuencia de acontecimientos.
Éstos son,
debidos tanto a la isquemia propiamente dicha,
como a la reperfusión del órgano cuando se restablece el flujo vascular.
El cese o la disminución de la perfusión intestinal,
bajo los niveles de autorregulación fisiológicos,
desencadena una secuencia de eventos que de no ser revertida,
llevará a la necrosis o a la atrofia de la pared intestinal desde la mucosa hacia la serosa.
Por el contrario,
si se mantiene una presión de perfusión límite que permita un aporte de O2 de acuerdo con la demanda metabólica de la pared intestinal,
aún ante la obstrucción completa de uno de los vasos viscerales o sus ramas,
no se alterará la función celular ni la integridad tisular8.
Inicialmente,
el daño isquémico de la pared intestinal puede variar desde una afectación leve,
con necrosis superficial limitada a la mucosa (con o sin afectación de la submucosa y áreas focales de la muscularis) hasta la necrosis continua de todas las capas de la pared intestinal,
conocido como infarto transmural.
La lesión puramente isquémica inicial induce un daño local en la microcirculación con activación celular leucocitaria-endotelial,
que perpetúa el proceso de liberación de citoquinas y radicales libres,
que dañan y contribuyen a la necrosis de la pared intestinal.
En una fase avanzada de daño parietal intestinal,
la barrera mucosa se rompe,
pierde su capacidad aislante,
permitiendo la libre translocación bacteriana,
con liberación de gas en la propia pared (neumatosis) que posteriormente pasa a los vasos mesentéricos y a la vena porta (gas porto-mesentérico),
conduciendo a la bacteriemia y a la sepsis.
Por último,
la incorporación de citoquinas y de neutrófilos activados a la circulación general acaba provocando daño en otros órganos a distancia como el hígado o el pulmón,
en el contexto de un síndrome de respuesta inflamatoria sistémica con fallo multiorgánico.
Se han descrito tres fases en la IMA en función de la afectación de las distintas capas:
-Fase I: Enteritis o colitis reversible: necrosis de la mucosa,
erosión y ulceración de la submucosa y/o hemorragia.
Puede resolverse espontáneamente sin dejar secuelas.
-Fase II: Extensión a la pared intestinal con necrosis de la submucosa y muscular.
Con la reparación local puede haber cambios fibróticos.
-Fase III: Necrosis transmural de la pared intestinal,
asociado a un aumento de la mortalidad.
Requiere una intervención quirúrgica urgente.
CLÍNICA:
La sospecha clínica es la base del diagnóstico y se establece ante un paciente con un perfil de riesgo definido (antecedente de enfermedad cardiovascular,
arritmias,
insuficiencia cardíaca mal controlada,
infarto de miocardio reciente,
hipotensión,
diálisis,
estado de hipercoagulabilidad,
etc.),
que a primera vista impresiona de gravedad y presenta DOLOR ABDOMINAL SEVERO,
acompañado de forma más o menos frecuente de distensión abdominal,
nauseas,
vómitos,
diarrea y/o rectorragia.
Llama la atención la NORMALIDAD DE LA EXPLORACIÓN FÍSICA,
sin signos de irritación peritoneal,
en contraste con la gran intensidad del dolor.
Todo ello,
dificulta su diagnóstico precoz dada la similitud con otros procesos intraabdominales tales como pancreatitis,
diverticulitis aguda u obstrucción intestinal.
1.
Embolia Arterial: el dolor es de comienzo brusco y localización periumbilical.
2.
Trombosis Arterial: inicio gradual del dolor,
incluso de días de evolución,
con aumento progresivo de la intensidad y localización difusa.
3.
Trombosis Venosa Mesentérica: dolor variable según la extensión de la trombosis,
habitualmente difuso de instauración progresiva e intensidad más leve que en las de causa arterial.
4.
IMNO: el dolor abdominal es difuso y de rápida instauración,
aunque en ocasiones,
por la patología desencadenante son pacientes graves que se encuentran en cuidados intensivos y seudoanalgesiados en los que el dolor no es valorable.
Se sospecha cuando existe episodio reciente de bajo gasto e hipotensión mantenida y aparece fiebre y leucocitosis,
distensión abdominal o sangrado digestivo no explicados por otra causa.
Si se produce la necrosis completa de la pared intestinal aparecen defensa abdominal y signos de irritación peritoneal con hiperperistaltismo primero y luego silencio abdominal total.
Son pacientes inquietos,
sudorosos y que no se dejan explorar por la gran intensidad del dolor.
Aparecen también signos de deterioro hemodinámico: taquicardia,
hipotensión,
oligoanuria,
etc.
DIAGNÓSTICO:
1.- Pruebas de laboratorio:
Inicialmente inespecífica,
salvo discreta leucocitosis.
Posteriormente aparece:
• Gran leucocitosis,
normalmente por encima de 20000 y con gran desviación izquierda.
• Acidosis metabólica severa y/o coagulopatía que en este contexto de dolor abdominal sugieren isquemia o sepsis grave.
• Hiperamilasemia y elevación de CPK,
LDH,
GOT y GPT que reflejan la presencia de importante destrucción celular.
• Puede aparecer hemoconcentración por presencia de importante edema y tercer espacio abdominal o anemia en los casos que cursan con importante sangrado digestivo.
2.- Técnicas de imagen:
La radiografía simple de abdomen puede ser normal o inespecífica.
Su principal papel consiste en excluir otras causas identificables de dolor abdominal agudo,
incluyendo la perforación y la oclusión intestinal.
Es importante considerar que una radiografía normal no permite excluir el diagnóstico de IMA.
El hallazgo de asas dilatadas y la visión de impresiones dactilares (thumbprinting, debido al engrosamiento mural focal secundario a la hemorragia submucosa) reflejan la presencia de infarto y una mortalidad elevada (> 70%).
Algunos signos como la neumatosis o la presencia de gas en el territorio portal conllevan un pronóstico muy grave.
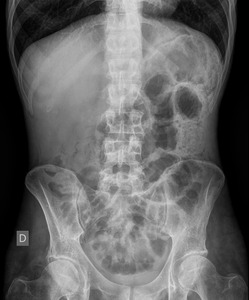
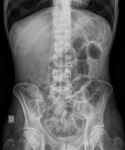
Fig. 5: Rx simple de abdomen. Patrón de neumatosis intestinal. Neumoperitoneo. Liquido en pelvis. Hallazgos radiológicos en el contexto de isquemia intestinal, con necrosis de la pared intestinal y perforación. Esta imagen corresponde al paciente nº3 de las figuras 18 y 19.
Aunque ha demostrado ser útil en identificar signos de trombosis venosa esplenoportal o mesentérica,
su utilización para diagnosticar una IMA de origen arterial se ve limitada por su incapacidad para detectar estenosis más allá de los segmentos proximales de la AMS y tronco celíaco.
Ante la sospecha de una isquemia intestinal,
la prueba inicial deber ser un estudio abdominal con TC helicoidal.
Representa la prueba de elección al tratarse de una técnica rápida,
reproducible,
fácil de realizar,
ampliamente disponible y con una alta sensibilidad (del 64-96%,
comparable a la angiografía) y especificidad (92-100%)9,10.
1.-Protocolo de adquisición:
El protocolo de estudio radiológico incluye la realización de un TCMD basal sin administración de contraste i.v. y tras la administración del mismo,
en fase arterial y venosa.
El uso de contraste oral para preparar el intestino,
puede facilitar la detección de pequeñas alteraciones de la perfusión mural y permite valorar adecuadamente el grosor de la pared.
No obstante ,
dada la severidad del cuadro y las implicaciones del retraso en el diagnóstico, está prácticamente desechado.
De usarlo,
utilizaremos 500-750 ml de un contraste oral negativo (fundamentalmente agua) ya que el contraste positivo dificulta la valoración de la captación de la pared e interfiere en el post-procesado de las imágenes.
TC basal (sin contraste i.v.): permite valorar la existencia de calcificaciones vasculares y detectar la presencia de un coagulo intravascular hiperdenso o de hemorragia submucosa, intramural o luminal.
TC tras la administración de contraste i.v.: permite identificar la presencia de émbolos o trombos en las arterias mesentéricas,
trombos en las venas mesentéricas,
realce anormal de la pared intestinal y la presencia de embolismo o infarto de otros órganos,
así como excluir otras causas de abdomen agudo.
Incluye 2 fases:
- Angio-TC de arterias mesentéricas: utilizando sistemas de detección automática de de contraste (bolus Tracking) con ROI localizado en la aorta abdominal a la altura del tronco celíaco y 100 UH de umbral.
La cantidad total de contraste yodado no iónico oscila entre 100 y 120 ml.
La utilización de flujos altos de contraste ( 3-5 ml/s) así como colimaciones finas de 0,75 -1,5 mm y Pitch de 1,5,
nos permiten realizar reconstrucciones 3D de alta calidad mejorando la visualización de las arterias mesentéricas distales.
- Estudio en fase venosa (60 s).
2.-Técnicas de postprocesado (3D)
Una vez adquiridas las imágenes,
se requiere su análisis en una estación de trabajo,
para realizar reconstrucciones del tipo:
- MIP (máxima intensidad de proyección): Puede ser una herramienta valiosa en la valoración de las ramas distales de los vasos,
sin embargo se pierde la relación espacial (Fig.6).
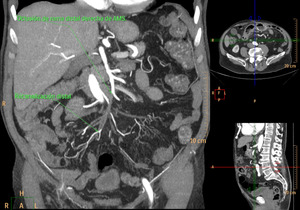
Fig. 6: Reconstrucción MIP en el plano coronal. Oclusión de la rama distal derecha de la AMS de causa tromboembólica, con repermeabilización distal.
- Volumen rendering: Incorpora todos los datos relevantes en la imagen resultante (nivel y amplitud de ventana, atenuación y brillo).
Los parámetros pueden ser ajustados para optimizar la visualización de la captación de la pared intestinal o pueden ser modificados para obtener una imagen similar a un tránsito o una enteroclisis. El volumen rendering es un herramienta muy útil para valorar la angiografía-CT de los vasos mesentéricos ,
siendo su mayor ventaja la capacidad para valorar tanto los vasos como las estructuras adyacentes y,
a diferencia de la MIP, preserva la relación espacial.
La calidad de los angiogramas-CT obtenidos se considera similar a los estudios angiográficos convencionales (Fig.7).
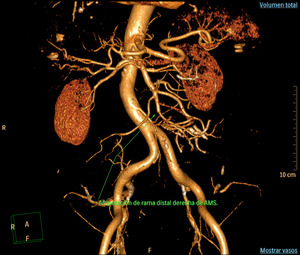
Fig. 7: Volume Rendering (VR). Mismo paciente que la figura anterior. Se visualiza la amputación de la rama distal derecha de la AMS.
3.-Hallazgos radiológicos
Los hallazgos en TC varían ampliamente dependiendo de la causa,
de la fisiopatología subyacente,
del momento del diagnóstico (en fase inicial,
antes del infarto intestinal,
o en fase tardía,
tras el establecimiento del mismo),
de la severidad (afectación mucosa superficial o infarto transmural),
la localización (intestino delgado y/o grueso),
la extensión (segmento corto o largo),
la distribución (difusa y/o localizada; segmentaria y/o focal),
del grado de hemorragia mural,
sobreinfección y/o perforación de la pared intestinal.
3.1.
Signos intestinales de la isquemia mesentérica aguda:
1.-Engrosamiento de la pared del asa: Debido a edema mural,
hemorragia de la submucosa o sobreinfección de la pared intestinal.
Representa el hallazgo radiológico más común,
estando presente en un 26%-96% de los casos11.
Es más frecuente en los casos de colitis isquémica (94%) e isquemia mesentérica reversible (80%),
mientras que es mucho menos frecuente en los casos de infarto mesentérico (26-38%)12-15.
Sin embargo,
es el hallazgo menos específico,
ya que puede ser observado en una variedad de condiciones no isquémicas que afectan al intestino delgado o grueso16,17.
Fig. 8
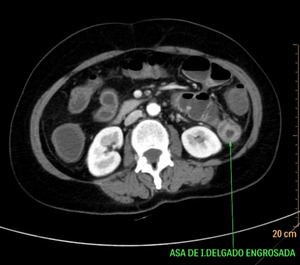
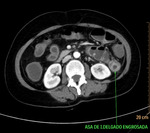
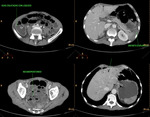
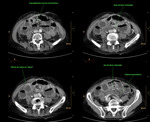
Fig. 9: Isquemia mesentérica aguda de causa oclusiva arterial trombótica. Se objetiva un engrosamiento concéntrico de las paredes de un asa de intestino delgado localizado en flanco izquierdo, con realce tras la administración de contraste i.v. Esta imagen corresponde al paciente nº1 de la figura 8.
El engrosamiento de la pared intestinal no difiere de acuerdo a la patogénesis oclusiva de la no oclusiva y por tanto,
no ayuda a diferenciarlas.
Sin embargo,
se ha observado que es más frecuente en la isquemia intestinal causada por oclusión venosa mesentérica que por oclusión arterial,
al menos debido a que el edema y la hemorragia intramural están ausentes en este segundo grupo18-19.
(Fig. 13 y Fig. 15 )
En ocasiones,
la pared engrosada puede adoptar una apariencia en capas ("target sign"),
alternando capas hipodensa (que refleja el edema de la submucosa) e hiperdensa (que sugiere hemorragia intramural).
En la isquemia de causa arterial,
cuando se establece la necrosis intestinal,
la pared del asa es fina y se dibuja a tiralíneas.
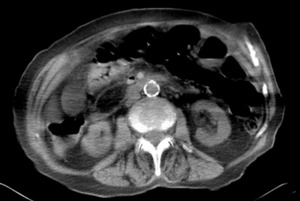
Fig. 12: Adelgazamiento parietal y ausencia de realce de las paredes de las asas intestinales y gas en el interior de la vena mesentérica superior. Signos predictores de mal pronóstico de la isquemia intestinal.
La presencia y el grado de engrosamiento de la pared intestinal no se correlaciona con la severidad de la IMA.
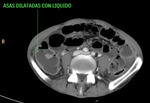
2.-Dilatación de asas intestinales focal o difusa: Debido a una interrupción del peristaltismo normal del intestino (íleo adinámico).
Se visualizan asas llenas de liquido o con niveles hidroaéreos.
Es un hallazgo bastante frecuente en el infarto intestinal (56%-91% de los casos) y menos común en la isquemia intestinal reversible (40%) y en la colitis isquémica superficial ya que en estos dos últimos casos,
la pared intestinal mantiene las contracciones espásticas12-15.(Fig. 18 ,
Fig. 19)
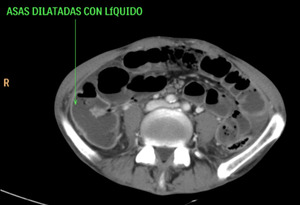
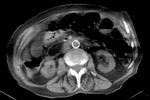
Fig. 23: Distensión de asas de intestino delgado con liquido y algún nivel hidroaéreo que traducen íleo paralítico. Esta imagen pertenece al paciente nº3 de las figuras 18 y 19.
Aunque es inespecífico,
puede ser la clave para sugerir el diagnóstico en un contexto clínico adecuado y en ausencia de otras causas que lo justifiquen,
como oclusión intestinal,
pancreatitis y otros procesos inflamatorios.
3.-Alteraciones de la atenuación/patrón de realce de la pared intestinal: La atenuación de la pared intestinal debe ser siempre evaluada tanto en el TC sin contraste i.v.
como tras la administración del mismo,
para evitar errores diagnósticos al malinterpretar una hiperdensidad de la pared intestinal,
como una hiperemia intramural tras la administración de contraste i.v.,
en aquellos casos de hemorragia intramural.
- En el TC sin administración de contraste i.v.:
- Hipodensidad de la pared intestinal: normalmente homogénea e indica edema mural,
el cual ocurre típicamente en casos de isquemia intestinal de causa oclusiva arterial reperfundida,
en la isquemia intestinal de causa oclusiva venosa,
en la obstrucción intestinal en asa cerrada y en la colitis isquémica3,11,20-22.
- Hiperdensidadde la pared intestinal,
en cambio,
es debida a hemorragia intramural e infarto hemorrágico3,11,20-22.
Puede observarse tanto en la isquemia no oclusiva como en la oclusiva arterial y venosa.
- En el TC tras la administración de contraste i.v.: El realce normal de la pared intestinal refleja la viabilidad del intestino y es un signo de buen pronóstico.
Existen distintas anomalías de este patrón de realce con implicaciones pronósticas:
- Realce aumentado de algunos segmentos de las asas intestinales: Es un signo precoz de isquemia y refleja un aumento de la presión capilar o ingurgitación venosa.
La hiperperfusión e hiperemia del intestino tienen una sensibilidad del 33% y una especificidad del 71% para el diagnóstico de IMA9 y se manifiestan como un realce aumentado de la pared.
Se considera un factor de buen pronóstico ya que se asocia a viabilidad de la pared.
Fig. 8 )
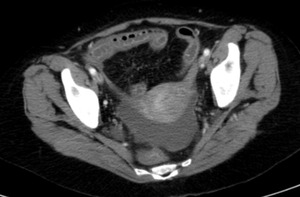
Fig. 11: Isquemia intestinal mesentérica aguda de causa oclusiva arterial trombótica. Se visualiza hiperemia de la mucosa de un asa de íleon localizada en FID. Signo de viabilidad de la pared intestinal. Liquido libre en fondo de saco de Douglas. Esta imagen corresponde al paciente nº1 de la figura 8.
La hiperemia sin hiperperfusión es más característica de la oclusión venosa mesentérica,
por obstrucción del flujo.
La hiperperfusión se observa en casos de reperfusión tras falta de aporte sanguíneo de cualquier etiología o por inflamación como resultado de una infección.
En ocasiones,
se visualiza una apariencia en capas,
"signo de la diana" o "signo del halo",
que es debido a la hiperemia e hiperperfusión asociada a edema mural alrededor.
Se ha observado tras la reperfusión de una isquemia intestinal de causa oclusiva arterial,
en la isquemia intestinal de causa no oclusiva,
en la oclusiva de causa venosa,
en la obstrucción intestinal en asa cerrada y en la colitis isquémica3,20-23.(Fig. 26)
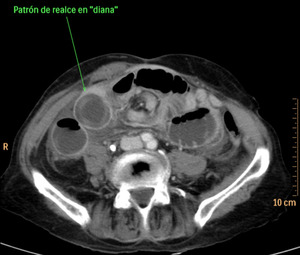
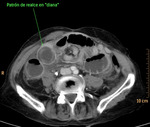
Fig. 27: "Signo de la diana" en un asa de íleon localizada en flanco derecho, con realce de las capas mucosa y serosa y edema de la submucosa. Hallazgo en el contexto de un paciente con obstrucción mecánica de intestino delgado complicada con volvulación de un asa de íleon y signos de isquemia intestinal. Esta imagen pertenece al paciente nº5 de la figura 26.
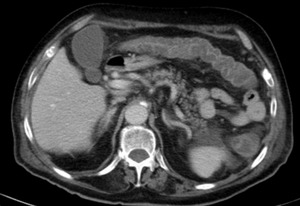
Fig. 31: Paciente nº6. Varón de 86 años que al 10º día de ingreso hospitalario (por aumento progresivo de su disnea habitual hasta hacerse de reposo), presenta un dolor abdominal intenso.
TC con contraste i.v.: Se objetiva un engrosamiento difuso de aspecto edematoso, de las paredes del colon transverso y descendente, con realce de las capas mucosa y serosa y edema submucoso ("signo de la diana"), compatible con colitis isquémica.
También puede observarse una captación prolongada del contraste por reducción de la perfusión arterial y venosa,
sobre todo,
en casos de obstrucción en asa cerrada,
isquemia de causa no oclusiva y asa en shock.
- Ausencia y/o disminución del realce del asa.
Es un signo altamente específico de isquemia o infarto intestinal (con una especificidad del 96%) e indica asa no viable3,9,13.
(Fig. 32)
Una pobre captación del borde antimesentérico del asa es sugestivo de isquemia no oclusiva.
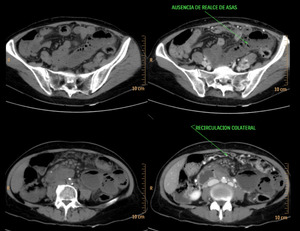
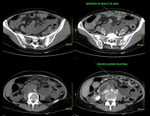
Fig. 33: TC sin y tras la administración de contraste i.v.: Distensión de asas intestinales con liquido en su interior, principalmente en flanco izquiedo, que refleja íleo paralítico. Ausencia de realce parietal de dichas asas. Signo predictor de mal pronóstico, altamente específico de infarto intestinal, que indica asas no viables. Estas imágenes pertenecen a la paciente nº7 de la figura 32.
4.- Estriación de la grasa,
presencia de liquido mesentérico y ascitis:Son hallazgos inespecíficos y su presencia depende de la causa,
la fisiopatología y la severidad de la isquemia,
así como de su localización en el intestino delgado o grueso.
Consisten en un transudado de líquido en el mesenterio o en la cavidad peritoneal causado por la elevación de la presión venosa mesentérica,
que comúnmente se observa en la obstrucción intestinal en "asa cerrada" y en la isquemia intestinal de causa venooclusiva.
En estos casos,
tienen un valor limitado para estimar la severidad de la isquemia intestinal.
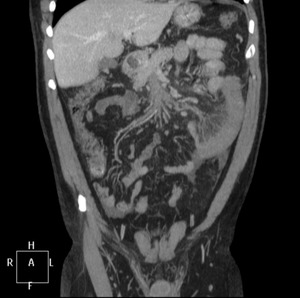
Fig. 14: Reconstrucción MPR en el plano coronal. Extenso defecto de repleción hipodenso en vena mesentérica superior y sus ramas, compatible con trombosis venosa. Engrosamiento de la pared de un asa de intestino delgado localizado en flanco izquierdo. Estriación de la grasa y edema mesentérico. Pequeña cantidad de liquido libre intraperitoneal. Esta imagen corresponde al paciente nº2 de la figura 13.
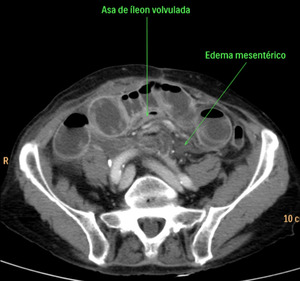
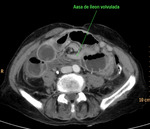
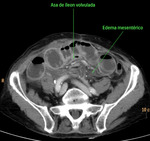
Fig. 30: Asa de íleon volvulada. Se acompaña de edema mesentérico y liquido libre. Hallazgos en el contexto de una obstrucción intestinal mecánica con volvulación de un asa de íleon y signos de isquemia intestinal. Esta imagen pertenece al paciente nº5 de la figura 26.
En cambio,
en la isquemia intestinal de causa oclusiva arterial,
solamente están presentes cuando se ha instaurado la necrosis transmural,
pudiendo este hallazgo ser útil para valorar la severidad del daño intestinal.
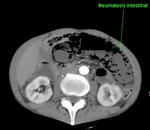
5.- Neumatosis intestinal y gas porto-mesentérico: Son los hallazgos menos frecuentes (estando presentes en un 6-28% y en un 3-14% de los casos respectivamente) pero los más específicos12-15.
La neumatosis se puede visualizar como burbujas de aire aisladas dentro de la pared intestinal isquémica o como un anillo lineal más prominente de aire que diseca la pared intestinal en dos capas.
El gas venoso porto-mesentérico puede consistir únicamente en pequeñas inclusiones de gas dentro de las venas mesentéricas o bien pueden extenderse a las ramas intrahepáticas de la vena porta,
que típicamente se localizan en la periferia del hígado24.
Son signos que aparecen tardíamente,
específicos de necrosis transmural del asa,
que reflejan una discontinuidad de la pared con paso del aire intraluminal hasta las capas externas de la pared y al sistema venoso.
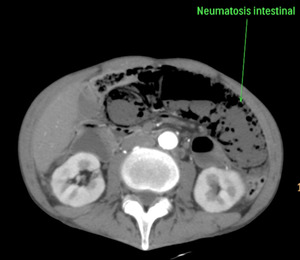
Fig. 22: Importante neumatosis intestinal. Signo tardío y específico de isquemia intestinal, que sugiere necrosis transmural del asa. Esta imagen pertenece al paciente nº3 de las figuras 18 y 19.
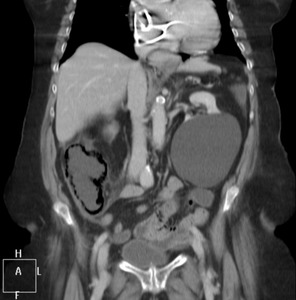
Fig. 25: Paciente nº4, con isquemia instestinal de causa no oclusiva (por bajo gasto), se visualiza un anillo de aire que diseca la pared del colon derecho y ciego, compatible con neumatosis intestinal. Posteriormente, se interviene al paciente, resecándole el colon derecho, con diagnóstico anatomopatológico de necrosis isquémica de dicha pared.
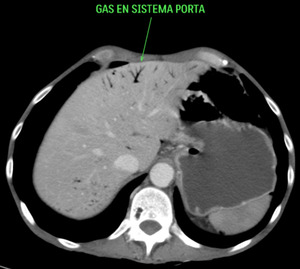
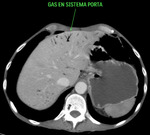
Fig. 20: Se visualiza gas en el interior del sistema portal intrahepático, de predominio periférico, a diferencia de la neumobilia. También se visualiza dilatación gástrica en el contexto del íleo paralítico. Esta imagen corresponde al paciente nº3 de las figuras 18 y 19.
Aunque estos dos signos tienen una especificidad cercana al 100% en el diagnóstico de la isquemia y/o necrosis intestinal,
en ocasiones,
también pueden visualizarse en otras patologías no isquémicas con discontinuidad de la mucosa,
como patología inflamatoria-infecciosa (colangitis,
diverticulitis,
apendicitis,
sepsis,…),
traumatismo abdominal,
neoplasias,
lesión yatrogénica de la mucosa,
asma,
Pneumatosis cystoides coli,
etc.
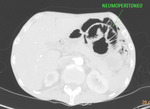
6.-Neumoperitoneo o aire libre en la cavidad peritoneal:Es un signo de mal pronóstico ya que indica perforación de un segmento de intestino con necrosis transmural.
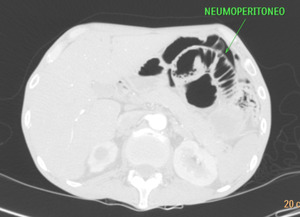
Fig. 24: TC abdominal con ventana de pulmón: Neumoperitoneo. Es un signo de mal pronóstico que indica perforación de un segmento de intestino con necrosis transmural. Esta imagen pertenece al paciente nº3 de las figuras 18 y 19.
3.2.- Signos vasculares de la isquemia mesentérica aguda:
En muchas ocasiones el TC será de gran ayuda a la hora de determinar la causa de la isquemia,
ya que esta técnica permite demostrar la vascularización mesentérica y sus posibles alteraciones como: ateromatosis calcificada,
trombos,
oclusión,
invasión tumoral y traumatismos.
Dentro de los signos vasculares se incluyen:
1.- Embolia arterial de la arteria mesentérica superior: se visualiza como una densidad de partes blandas intraarterial.
La mayoría de los émbolos se localizan cercanos a una bifurcación vascular.
La gravedad del cuadro es mayor cuanto mas proximal se localice el émbolo.
Si el episodio embólico es agudo,
el émbolo aumentará discretamente el diámetro vascular,
mientras que la cronicidad del episodio se acompaña de una disminución del diámetro del mismo.
(Fig. 6)
2.-Trombosis arterial de la arteria mesentérica superior: Típicamente se localiza cerca del origen de las arterias mesentéricas.
El trombo se visualiza como una densidad de partes blandas asociado a lesiones arterioesclerosas difusas de las arterias viscerales.
Es muy importante valorar la permeabilidad del árbol arterial distal a la oclusión,
debido a la existencia de flujo retrógrado,
a través de vasos colaterales,
que actúa como mecanismo de defensa ayudando a mantener la viabilidad de las asas intestinales.
Este hecho indica que el vasoespasmo aún no se ha establecido.
( Fig. 10 )
3.-Trombosis venosa de las venas mesentéricas: densidad de partes blandas,
trombo,
en las venas mesentéricas,
normalmente en la vena mesentérica superior.
Se visualizan como defectos de repleción intraluminales hipodensos rodeados de un anillo periférico de realce de la pared de la vena (Fig. 40).
Generalmente se acompañan de circulación colateral,
ingurgitación de las venas mesentéricas y edema mesentérico.
El trombo venoso al igual que el arterial,
puede aumentar el calibre del vaso si es de instauración reciente y disminuye a medida que se cronifica.
( Fig. 13,
Fig. 37 y Fig. 38 ).
La fase arterial del estudio no es útil para valorar la trombosis venosa debido a la mezcla de sangre opacificada y no opacificada que da lugar a artefactos de flujo laminar que simulan un trombo.
Por ello,
es muy importante planificar una fase venosa en el protocolo de estudio.
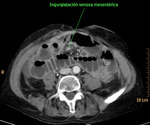
4.-Ingurgitación de las venas mesentéricas: producida por congestión secundaria al estasis del flujo venoso.
Se observa típicamente en la isquemia intestinal de causa venooclusiva y en la obstrucción intestinal en asa cerrada.
( Fig. 16 y Fig. 28 )
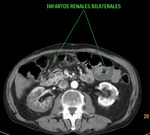
3.3.- Infarto en otros órganos (riñones,
bazo o hígado): por la falta de flujo sanguíneo.
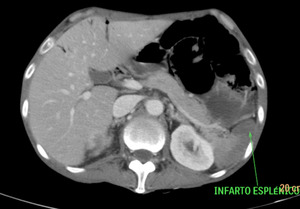
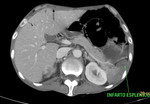
Fig. 21: Imagen hipodensa en la periferia del bazo, compatible con infarto esplénico por falta de flujo sanguíneo, en el contexto de una isquemia intestinal de causa oclusiva arterial trombótica, con necrosis de la pared intestinal y perforación. Esta imagen corresponde al paciente nº3 de las figuras 18 y 19.
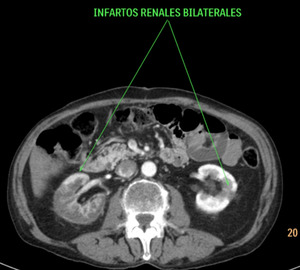
Fig. 39: En otro paciente distinto, con isquemia intestinal de causa no oclusiva por bajo gasto.
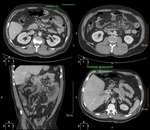
TC con contraste i.v.: Se observan ambos riñones con captación heterogénea del contraste, con extensa zona hipocaptante que afecta a los dos tercios superiores del riñón derecho y otra pequeña zona hipocaptante de base periférica en el riñón izquierdo. Además la lesión derecha presenta una captación periférica subcapsular ("signo del anillo"). Hallazgos compatibles con infartos renales bilaterales.
En resumen,
aunque los hallazgos radiológicos generalmente son heterogéneos e inespecíficos,
al igual que los hallazgos clínicos y analíticos,
existen una serie de signos en TC con una especificidad mayor del 95% para el diagnóstico de IMA,
que incluyen: la oclusión de la AMS,
la oclusión de la VMS,
neumatosis intestinal,
gas porto-mesentérico,
ausencia de realce de la pared intestinal e isquemia de otros órganos abdominales.
Signos predictores de mal pronóstico por imagen en la isquemia intestinal:
1.-Localización y extensión del segmento afectado por infarto transmural.
2.-Adelgazamiento de la pared intestinal y ausencia de realce tras la administración de contraste i.v.
3.-Neumatosis y gas porto-mesentérico.
4.-Neumoperitoneo.
5.-Signos de obstrucción intestinal en "asa cerrada".
6.-Ascitis en los casos de isquemia intesinal de causa oclusiva arterial aguda y afectación del intestino delgado.
La trombosis de la AMS y la isquemia no oclusiva tienen peor pronóstico,
con una mortalidad quirúrgica del 77% frente al 54% de la embolia arterial y al 32% de la trombosis venosa.
Todo ello,
confiere una enorme importancia al diagnóstico por la imagen,
ya que la adecuada elección del tratamiento afectará al pronóstico y a la supervivencia global de estos pacientes.
Presenta una alta sensibilidad en el diagnóstico de estenosis u oclusión en el origen de la AMS o del tronco celíaco,
así como para la identificación de una trombosis venosa mesentérica (sensibilidad del 100%,
especificidad del 98%).
Sin embargo,
no es útil para el diagnóstico de las formas no oclusivas o para la identificación de oclusiones en las ramas distales.
Su principal ventaja frente al TC es la ausencia de toxicidad renal,
al no precisar contrastes yodados.
Entre los inconvenientes destaca su baja disponibilidad en la urgencia.
- Arteriografía convencional
Aunque clásicamente se la ha considerado la técnica gold-estándar para el diagnóstico de la IMA,
actualmente se la ha relegado a un segundo plano ya que se trata de una prueba invasiva,
de elevado coste y que requiere tiempo para una correcta exploración.
Además no es capaz de excluir diagnósticos alternativos,
ni evaluar la viabilidad de la pared intestinal.
Entre sus ventajas destacaría que:
- Permite distinguir entre formas oclusivas y no oclusivas.
Ello es importante porque la IMNO puede beneficiarse de un tratamiento conservador.
- Permite la infusión de vasodilatadores como la papaverina y también de agentes trombolíticos.
- Proporciona un mapa quirúrgico idóneo para cualquier procedimiento de revascularización.
Aunque la angiografía ha contribuido a disminuir la mortalidad de la IMA,
debe considerarse que no siempre se dispone de un angiografista experto y que,
en determinadas circunstancias,
puede contribuir a retrasar el acto quirúrgico.
Por este motivo,
si el paciente presenta inestabilidad hemodinámica o signos claros de peritonitis,
es preferible optar por la laparotomía,
precedida en lo posible por una técnica de imagen (ecografía-Doppler,
TCMD).