Repasar las características ecográficas,
el comportamiento y la anatomía patológica de los tumores testiculares en la edad adulta.
Epidemiología:
Las neoplasias testiculares son las lesiones tumorales malignas más frecuentes en los varones jóvenes (edad promedia 15-34 años),
aunque constituyen sólo el 1% de todas las neoplasias en el sexo masculino.
Dentro de estas lesiones,
las neoplasias de células germinales (originadas de células espermatogénicas) agrupan el 95% del total de las neoplasias.
Los tumores primarios de células no germinales derivan de los cordones sexuales (células de Sertoli) y del estroma testicular (células de Leydig) y sólo representan el 5 % (de las cuales resultan malignas únicamente un 10%).
El linfoma,
las metástasis y la leucemia pueden manifestarse también como masas testiculares.
En los últimos años la incidencia del carcinoma testicular ha aumentado de forma considerable (incremento del 100% de la prevalencia con respecto al número de casos reportados desde 1936),
sin que se conozcan los factores causantes de esta tendencia.
El 90% de los pacientes que desarrollan un carcinoma testicular son de raza blanca,
y sólo un 3% son afroamericanos.
Existe una curva de incidencia bifásica,
con un pico máximo en el rango etario comprendido entre los 25-35 años; en el grupo de edad comprendido entre los 71-90 años se incluyen linfomas y metástasis como causas de afectación neoplásica testicular.
A todo esto se añade que la tasa de supervivencia global para los pacientes con carcinoma testicular ha aumentado de un 79% a un 95% en los últimos 30 años.
En algunos casos,
las neoplasias testiculares son infradiagnosticadas y catalogadas inicialmente como una orquitis; las manifestaciones clínicas son variables y con frecuencia poco floridas,
salvo por la presencia de una masa escrotal,
casi siempre palpable (la mayoría de los pacientes describen dolor mal definido en hipogástrico-región perineal,
hinchazón abdominal o pesadez),
pero no dolor agudo.
Por este motivo,
el papel del radiólogo es fundamental en el diagnóstico inicial,
desarrollando su función primordial en la caracterización de las masas escrotales mediante ecografía y en la realización de las pruebas diagnósticas pertinentes para un correcto estadiaje.
En la evaluación inicial mediante ecografía,
excepto raras excepciones,
una masa sólida intratesticular debe ser considerada maligna.
En esta revisión,
nos centraremos únicamente en la caracterización de las masas intratesticulares,
más concretamente de los tumores malignos derivados de células germinales (TCG),
tanto de estirpe seminomatosa como no seminomatosa.
Esta clasificación es,
según la clasificación adaptada de la WHO,
la siguiente:
v Lesiones precursoras:
- Neoplasia intratubular de células germinales (Carcinoma in situ).
v Tumores de un solo tipo histológico (TCG seminomatosos y no seminomatosos):
- Seminoma.
- Carcinoma embrionario.
- Yolk sac tumour (tumor del seno endodérmico).
- Coriocarcinoma.
- Teratoma (en sus variantes maduro,
inmaduro y con áreas de transformación maligna).
v Tumores de más de un tipo histológico (TCG mixto): presentan dos o más tipos histológicos combinados,
y pueden asociar o no componente seminomatoso.
Recuerdo embriológico:
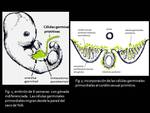
La gónada indiferenciada de un embrión de 6 semanas está compuesta por tres tipos celulares distintos: células mesenquimales,
células mesoteliales y células germinales.
De las células mesenquimales (derivadas del epitelio celómico) se origina el cordón sexual primitivo,
y de éste los túbulos seminíferos y células de Sertoli (que secretan factor inhibidor antimülleriano).
Las células mesenquimales (condensación del mesénquima embrionario) forman la cresta genital embrionaria; de estas células mesenquimales se originará el intersticio o estroma testicular formado por las células de Leydig (productoras de testosterona).
Finalmente,
tiene lugar la migración de las células germinales primordiales,
que son extraembrionarias y se forman en la pared del seno endodérmico (saco de Yolk) desde donde migran acompañando al intestino posterior y a la raíz dorsal del mesenterio hasta alcanzar la cresta genital e incorporarse al cordón sexual primitivo,
dando lugar en su evolución posterior a las espermatogonias (Figs.
1 y 2).
Recuerdo anatómico y características histológicas:
Los túbulos seminíferos están densamente empaquetados en lóbulos (existen del orden de 200-300 lóbulos en un teste adulto normal) separados por septos finos,
rodeados en conjunto por una cápsula fibrosa que es la túnica albugínea.
Ésta,
a su vez,
está rodeada por una capa aplanada de células mesoteliales,
la túnica vaginalis.
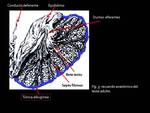
Los túbulos seminíferos confluyen en los túbulos rectos en la parte posterior del testículo,
que drenan en la rete testis en el mediastino testicular.
La rete testis converge posteriormente formando 15-20 ductos eferentes que forman la cabeza del epidídimo,
donde continúan su trayecto,
cada vez menos enrevesado,
a lo largo del cuerpo y cola del epidídimo,
dando lugar a un único tubo que abandona el epidídimo y sale del saco escrotal,
que es el conducto deferente (Fig.
3).
Los túbulos seminíferos están compuestos por células de Sertoli y células germinales (que es la población celular predominante) en distintos estadio evolutivos (espermatogonias,
espermatocitos,
espermátides y espermatozoides).
Las células de Sertoli no sufren mitosis y ayudan en la espermatogénesis ya que conforman una estructura de soporte para la correcta maduración de las células germinales; también ejercen una función de fagocitosis de aquéllas células germinales que han degenerado.
Las uniones celulares herméticamente establecidas entre ellas son las responsables de la barrera hematotesticular.
El espacio que queda entre los túbulos seminíferos es el intersticio testicular,
derivado del mesénquima embrionario; incluye tejido conectivo,
linfáticos,
estructuras vasculares,
mastocitos y células de Leydig,
que son la principal fuente de producción de testosterona.
En la ecografía,
que debe ser la primera prueba de imagen en la caracterización de las lesiones testiculares,
ya que es fácilmente reproducible y ha demostrado una sensibilidad cercana al 100% en la identificación de las masas escrotales,
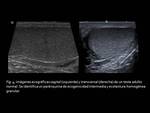
un teste normal de un varón adulto debe mostrar una ecotextura granular homogénea,
de ecogenicidad intermedia (Fig.
4); la túnica albugínea generalmente no se ve (pero sí podemos identificar el área de engrosamiento e invaginación que realiza a nivel de hilio testicular y que conforma el mediastino testicular,
fácilmente valorable).
Las estructuras epididimarias sí son visualizadas con facilidad.
Ante una masa escrotal,
debemos describir primero su localización (intra- o extratesticular),
sus características (sólida o quística,
patrón vascular –los tumores de mayor tamaño tienden a ser más vasculares-,
calcificaciones,
hiper- o hipoecoica con respecto al parénquima testicular sano –si queda parénquima restante-,
tamaño,…) y su morfología.
Tumores de células germinales:
Existen varias teorías que postulan que la neoplasia de células germinales intratubular es una lesión precursora de los carcinomas testiculares (equivaldría a un carcinoma in situ),
pues el 50% de los pacientes diagnosticados mediante biopsia de neoplasia intratubular desarrollan un tumor invasivo en unos 5 años.
Se cree que este grupo de células intratubulares anormales puede evolucionar hacia una línea celular gonadal unipotencial (y desarrollarse un seminoma) o hacia una línea celular totipotencial (y originar tumores no seminomatosos,
dependiendo del grado de diferenciación en su evolución).
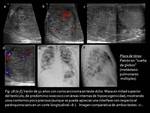
Las metástasis de los TCG pueden diseminar por vía linfática o por vía hematógena (siendo el primer órgano de asiento visceral el pulmón).
La extensión directa a través de la túnica albugínea afectando a la piel escrotal es un hallazgo raro y puede ocurrir en estadios muy avanzados de la enfermedad y en neoplasias altamente agresivas.
La mayoría de los tumores diseminan por vía linfática en primer lugar (Fig.
5) y de forma preferente a la hematógena,
excepto el coriocarcinoma.
El patrón de diseminación ganglionar es predecible y sigue un modelo de extensión reconocido.
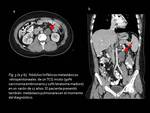
La afectación linfática retroperitoneal en el caso de tumores testiculares derechos es en cadena interaortocava a nivel de L2 (Fig.
6); mientras tanto,
el primer nivel ganglionar para tumores testiculares izquierdos es un área limitada por la vena renal izquierda,
la aorta,
el uréter y la arteria mesentérica inferior (Fig.
7).
En ocasiones,
puede existir una diseminación linfática de cadenas derechas a las izquierdas siguiendo el patrón normal de drenaje de la cisterna del quilo y del conducto torácico,
siendo la diseminación de izquierda a derecha menos probable (Fig.
8).
Cuando el tumor invade el epidídimo,
es posible entonces que disemine directamente a los ganglios ilíacos externos; si invade la piel,
puede diseminar a los ganglios inguinales (de ahí que el abordaje transescrotal esté contraindicado,
realizándose orquiectomía por abordaje inguinal).
La diseminación metastásica a órganos distantes se debe a una invasión hematógena; la afectación metastásica pulmonar es la más común para todos los TCG seguida de la afectación hepática y cerebral (Fig.
9); como dato importante,
se debe tener en cuenta que las características histológicas de los implantes metastásicos son,
en la mayoría de los casos,
diferentes de las del tumor primario testicular (indicando la naturaleza totipotencial de las células germinales).
Estadiaje:
En la actualidad,
se aboga por la clasificación TNM (tumor,
node,
metastasis) de la American Joint Committee on Cancer,
que tiene en cuenta la extensión local del tumor,
el número y tamaño de los nódulos linfáticos,
la presencia de metástasis a distancia y los marcadores séricos (Fig.
10).
*Marcadores tumorales: la determinación de los marcadores séricos desempeña un papel fundamental en el diagnóstico,
estadiaje,
pronóstico y seguimiento de los TCG,
así como para cuantificar la respuesta al tratamiento y predecir futuras recurrencias.
Sólo tres tienen un uso clínico principal:
- a-fetoproteína (AFP): proteína fabricada en fases tempranas de la gestación por el hígado fetal,
el tracto GI y el saco de Yolk.
- b-hCG: gonadotropina coriónica humana,
glicoproteína producida por el sincitiotrofoblasto placentario (elevada en seminoma y coriocarcinoma).
- LDH: lactato-deshidrogenasa,
producida por múltiples órganos y mucho menos específica,
aunque sus niveles se correlacionan muy bien con el volumen de la masa tumoral.
Tanto la AFP como la b-hCG están elevadas de forma conjunta hasta en un 80% de los pacientes con TCG no seminamatosos,
tanto mixtos como de una sola variante histológica.
Tipos histológicos de TCG:
- Seminoma: tumor de células germinales puro más frecuente (35-50% de todos los TCG).
Constituido por células que se asemejan a las células germinales primitivas; aproximadamente un 15% presentan componente de sincitiotrofoblasto (elevación de la b-hCG) que dificulta su clasificación,
aunque no afecta en general al buen pronóstico de este tumor.
En comparación con otros TCG,
el seminoma aparece en varones de mayor edad que el promedio,
en torno a los 40´5 años.
El 75% de los pacientes tiene enfermedad limitada al testículo en el momento del diagnóstico,
un 20% tiene adenopatías retroperitoneales y sólo un 5% metástasis extranodal.
El tamaño tumoral oscila entre pequeñas lesiones bien definidas hasta grandes masas que sustituyen por completo el parénquima testicular,
aunque por lo general se muestran como masas uniformemente hipoecogénicas (los de mayor tamaño suelen ser más heterogéneos),
uniformes y de contornos bien delimitados (Figs.
11 y 12),
de aspecto lobulado o multinodular (los nódulos generalmente están contiguos,
siendo extremadamente raro los casos de afectación multifocal -Fig.
13-).
Los tumores bilaterales son poco frecuente (1-5%) y casi siempre son asíncronos (los bilaterales síncronos representan un 10%).
Es un tumor extremadamente radiosensible y el tratamiento es muy satisfactorio,
incluso para estadios avanzados,
con una supervivencia global superior al 95% a los 5 años.
En muchos casos se realiza seguimiento estrecho tras la orquiectomía,
mientras que la quimioterapia se deja para el tratamiento de la enfermedad avanzada.
TUMORES DE CÉLULAS GERMINALES NO SEMINOMATOSOS (TCGNS):
- Carcinoma embrionario: compuesto de células epiteliales primitivas anaplásicas que se asemejan a las células embrionarias tempranas.
Es el segundo tipo histológico más frecuente en su forma pura (aunque sólo representa un 2-3% del total),
después del seminoma,
apareciendo en el 87% de los TCG mixtos.
Aparece a una edad más temprana que el seminoma,
generalmente entre los 25-35 años.
Suele tener un tamaño menor que el seminoma,
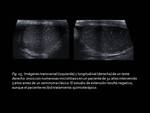
mostrando en la imagen ecográfica una ecogenicidad más heterogéna y unos bordes peor definidos (Figs.
14),
en ocasiones imposibles de diferenciar con respecto al parénquima testicular adyacente.
Su comportamiento biológico es más agresivo que el seminoma (Fig.
15).
- Yolk Sac Tumor: también conocido como tumor del seno endodérmico.
Formado por una población celular totipotencial que se ha diferenciado hacia células de membranas fetales extraembrionarias.
Es el tumor más frecuente en la población infantil,
representando hasta el 80% en menores de 2 años.
En su forma pura,
es muy raro en adultos,
mientras que aparece en el 44% de los casos de TCG mixtos.
Es característica la elevación de la AFP en suero,
en más del 90% de los casos.
Los hallazgos en la imagen no son específicos,
especialmente en los niños,
en los que muchas veces el único dato es un aumento del tamaño testicular,
sin masa definida.
Si se demuestra en la pieza de orquiectomía que el tumor está limitado al teste,
y los niveles séricos de AFP no son muy elevados,
el pronóstico es muy bueno (incluso en los niños no se realiza ningún otro tratamiento más,
salvo vigilancia estrecha,
ya que el pronóstico en estos casos es excelente).
En casos de recaída de la enfermedad,
el pulmón es el lugar habitual de metástasis.
- Teratoma: segundo en frecuencia en la población infantil,
generalmente en menores de 4 años.
En su forma pura,
es muy raro en adultos,
aunque elementos teratomatosos aparecen en aproximadamente la mitad de los casos de TCG mixtos.
Se trata de un tumor complejo en sus tres variantes (maduro,
inmaduro y con áreas de transformación maligna),
formado por una disposición desordenada de tejidos adultos y fetales que implican a las tres capas germinales (endodermo,
mesodermo y ectodermo).
El tumor dermoides,
la lesión teratomatosa más frecuente en el ovario,
constituye solo una pequeña minoría de los teratomas testiculares.
Por lo general,
en la imagen aparecen como masas complejas (Fig.
16) circunscritas que pueden contener áreas quísticas internas anecoicas o heterogéneas (contenido seroso,
mucoide,
queratina,
focos de calcificación,
fibrosis,
tejido cartilaginoso,…).
El comportamiento biológico de los teratomas es muy variable; en los testes prepuberales,
se consideran benignos incluso las formas inmaduras,
mientras que en varones adultos incluso el teratoma maduro tiene potencial maligno (todos los elementos teratomatosos,
maduros e inmaduros,
en un teste pospuberal pueden metastatizar independientemente de sus características histológicas); es más,
las lesiones metastásicas suelen contener elementos de células germinales de variante no teratomatosa.
- Coriocarcinoma: es un tumor raro,
representando menos del 1% de todos los TCG en su forma pura.
En los TCG mixtos,
aparece en un 8% de los casos.
Generalmente,
aparece en pacientes entre la 2ª y 3ª décadas de la vida.
Se trata de un tumor maligno muy agresivo,
compuesto por una mezcla de células citotrofoblásticas y sincitiotrofoblásticas.
Desde el punto de vista de la imagen ecográfica,
suelen presentarse como una masa isoecogénica de contornos poco definidos (Fig.17),
y en ocasiones puede objetivarse invasión de la túnica albugínea.
Tiene alta tendencia a la diseminación temprana por vía hematógena; los pacientes suelen presentar síntomas en relación con la afectación visceral metastásica antes que por la palpación testicular positiva.
Por orden de afectación,
los órganos más habituales de metastatización son el pulmón,
el hígado,
el tracto gastrointestinal y el cerebro,
y tanto el tumor primario como las metástasis son con frecuencia hemorrágicos (Fig.18 y 19).
Los niveles de b-hCG están muy elevados y causan ginecomastia en el 10% de los casos.
Es el TCG de peor pronóstico y suele causar la muerte del paciente aproximadamente al año del diagnóstico.
En los TCG mixtos que contienen componente de coriocarcinoma,
aunque tienen un mejor pronóstico que las formas puras,
los niveles muy altos de b-hCG (> 50.000 IU/L) predicen un peor pronóstico y una disminución de la supervivencia global a los 5 años inferior al 48%.
TUMORES DE CÉLULAS GERMINALES MIXTOS (TCG mixtos):
En este grupo de tumores se incluyen todos aquellos que están compuestos por más de un grupo celular,
tengan o no entre ellos componente seminomatoso asociado,
y puede ocurrir cualquier combinación posible; dentro de los TCG no seminomatosos,
los tumores mixtos son mucho más comunes que cualquier otra forma histológica pura,
constituyendo entre un 32-60% del total.
El carcinoma embrionario es el componente más frecuente (Fig.
20),
a menudo combinado con uno o más componentes (teratoma,
seminoma y/o yolk sac tumor).
La edad de presentación se sitúa en torno a los 30 años.
Los hallazgos en la imagen son muy variables,
reflejando la diversidad de este tipo de tumores (Figs.
20,
21 y 22).
No son radiosensibles.
Las masas retroperitoneales metastásicas (frecuentes al diagnóstico) pueden disminuir en tamaño e intensidad después del tratamiento,
aunque estos hallazgos no indican siempre necrosis tumoral (sólo un 40%),
sino que en un porcentaje alto de casos (40%) se debe a la evolución del tumor a un tiempo histológico más benigno (generalmente teratoma maduro),
mientras que un 20% tiene áreas de tumor residual.
En cualquier caso,
las masas retroperitoneales deben ser resecadas,
pues aunque contengan sólo depósitos de teratoma maduro de tipo histológico benigno pueden experimentar un crecimiento que en ocasiones es muy significativo (growing teratoma syndrome) (Fig.
23).
Tumor de células germinales involucionado o “quemado”:
Se ha descrito el fenómeno del regressed or “burned-out” germ cell tumor,
aunque no es del todo bien conocido.
En estos casos,
el paciente puede presentar enfermedad metastásica diseminada incluso cuando el tumor primario ha involucionado.
Se postula que la patogénesis de este fenómeno se debe a la alta tasa metabólica del tumor debido a su rápido crecimiento,
que sobrepasa el aporte sanguíneo,
ocasionando un defecto de perfusión tumoral y la subsecuente regresión neoplásica.
Estos tumores resultan clínicamente ocultos,
puesto que la palpación suele ser negativa y el teste puede aparecer incluso disminuido de tamaño.
La ecografía tiene un papel vital en la búsqueda del tumor primario involucionado; la apariencia ecográfica suele ser muy variable,
aunque generalmente son lesiones de pequeño tamaño,
hiper- o hipoecoicas,
o simplemente pueden manifestarse como un área de calcificación focal.
El análisis histológico revela la presencia de cantidades diminutas de tumor residual o áreas de depósitos densos de colágeno con células inflamatorias dispersas.
Tumor primario de células germinales extragonadal:
Pueden localizarse en retroperitoneo,
mediastino (Fig.
24),
área sacroccocígea y glándula pineal.
Es importante diferenciarlo del TCG involucionado con metástasis.
Su patogenia se postula que puede deberse a una migración aberrante de las células germinales desde el saco de Yolk y/o a la persistencia de células pluripotenciales en restos primitivos durante el desarrollo somático. Ante un varón joven con una masa voluminosa retroperitoneal,
el primer paso es descartar que se deba a una enfermedad metastásica de un TCG intragonadal y explorar mediante ecografía los testículos en busca de masas y del posible fenómeno del “burned-out” germ cell tumor.
Factores de riesgo:
Existen cinco situaciones que han demostrado tener una relación directa clara para el desarrollo de carcinoma testicular:
- Antecedentes de carcinoma testicular previo (riesgo relativo incrementado en 20 veces sobre la población general para el desarrollo de nuevo carcinoma en teste contralateral).
- Historia familiar positiva (incremento del riesgo relativo de 6 veces).
- Criptorquidia (hasta en el 14´5% de los pacientes con carcinoma testicular se ha documentado historia previa de criptorquidia).
La criptorquidia ha demostrado tener una fuerte asociación con el desarrollo posterior de carcinoma testicular.
En la actualidad, se cree que la ausencia de descenso de los testículos es una manifestación de un defecto generalizado de la embriogénesis,
teoría que ha cobrado importancia debido a dos observaciones clínicas relevantes,
que son el hecho de que el riesgo de carcinoma testicular no está limitado al teste criptorquídico (sino que se extiende al teste contralateral,
aunque haya descendido con normalidad) y que la orquidopexia (incluso a edades tempranas) no ha demostrado un descenso significativo del riesgo de desarrollar un carcinoma.
La mayoría de estos tumores son seminomas,
especialmente los que se desarrollan en testes no descendidos intraabdominales.
- Infertilidad.
- Estadios intersexuales.
Microlitiasis testicular:
Se trata de un hallazgo relativamente poco frecuente en la población general (aproximadamente en torno al 0´6%) y anteriormente se pensó que era un hallazgo incidental e inocuo.
En la actualidad se ha demostrado su relación con la criptorquidia,
la infertilidad,
la atrofia testicular,… y,
sobre todo,
se ha demostrado que la asociación entre microlitiasis y tumores testiculares es clara,
ya que la prevalencia de carcinoma en pacientes con microlitiasis testicular alcanza el 40%.
La aparición de microlitiasis se debe a la existencia de microcalcificaciones o cálculos en la luz de los túbulos seminíferos y se postula que su presencia es a causa de un defecto en la actividad fagocitaria de las células de Sertoli.
Lo que no está claro es si son secundarias a un testículo anormalmente conformado o,
por el contrario,
son las que inician el daño parenquimatoso.
En la imagen ecográfica,
aparecen como un punteado milimétrico hiperecogénico sin sombra acústica posterior (Fig.
25),
disperso por el parénquima testicular (que habitualmente es homogéneo).
Generalmente son bilaterales y simétricas,
y se necesita la presencia de cinco o más microlitiasis por imagen ecográfica para realizar el diagnóstico.